Silver Yoduro (AGI) struktur, egenskaper, innhenting, bruk

- 2626
- 54
- Prof. Oskar Aas
Han Sølvjodid Det er en uorganisk forbindelse dannet av et sølvatom (Ag) og en av jod (I), hvor det har en valens på -1 og sølvet på +1. Den kjemiske formelen er AGI.
Det er et lys gul krystallinsk fast stoff som blir mørkere ved å bli utsatt lenge for lys. Det er nesten uoppløselig i vann, men oppløses i nærvær av en høy ryoduro -ionekonsentrasjon (i-).
 Sølvjodid. Leiem/CC By-SA (https: // CreativeCommons.Org/lisenser/by-SA/4.0). Kilde: Wikimedia Commons.
Sølvjodid. Leiem/CC By-SA (https: // CreativeCommons.Org/lisenser/by-SA/4.0). Kilde: Wikimedia Commons. Fordi den har en krystallinsk struktur som ligner på is, har blitt brukt som et frø for å produsere regn og endre været. Denne bruken er avhørt på grunn av den potensielle skaden forårsaket av AGI når du oppløses i vannet.
Siden det nittende århundre ble det brukt i fotografering for sin evne til å mørkne med lyset. Det brukes også i antimikrobielle terapier.
Nylig har bruken blitt studert ved fjerning av radioaktivt avfalls jod produsert i generering av kjernefysisk energi. Det er nyttig i optiske fibre.
Det er en giftig forbindelse for mennesker, dyr og planter.
[TOC]
Struktur
Det er en ionisk forbindelse dannet av sølv i sin oksidasjonstilstand +1 og jod med Valencia -1. Koblingen mellom de to ionene er veldig sterk og stabil.
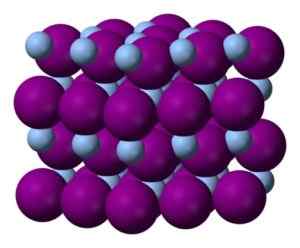 Sølv Yoduro -struktur. Blå = sølv; Fiolett = jod. Benjah-BMM27 / Public Domain. Kilde: Wikimedia Commons.
Sølv Yoduro -struktur. Blå = sølv; Fiolett = jod. Benjah-BMM27 / Public Domain. Kilde: Wikimedia Commons. Den krystallinske strukturen avhenger av temperaturen. Under 137 ° C er det i kubikk- eller gamma-form (y-Aagi), mellom 137 og 145,8 ° C er et grønngul fast eller beta (ß-agi) og over 145,8 ° C presenterer en gul farge og den er den Alpha Shape (α-Agi).
Nomenklatur
- Sølvjodid
Egenskaper
Fysisk tilstand
Lysegult fast, sekskantet eller kubikkkrystaller.
Molekylær vekt
234,773 g/mol
Smeltepunkt
558 ºC
Kokepunkt
1506 ºC
Tetthet
5,68 g/cm3
Løselighet
Praktisk talt uoppløselig i vann: 28 × 10-7 g/l a 25 ° C (0,0000028 g/l). Uoppløselig i syrer bortsett fra i iarhydriskyre (hydrogenjodidløsning i vann). Løselig i konsentrerte løsninger av alkaliske bromroer og alkaliske klorider.
Kjemiske egenskaper
Høye temperaturer konsentrerte syrer (kokende) angriper sakte den. Imidlertid påvirker ikke varme alkaliske hydroksider -løsninger det.
Det kan tjene deg: Jodosesyre (HIO2): Egenskaper og bruksområderDet er oppløst i løsninger der det er overflødig jodidion (I-) som danner et jod og sølvkompleks.
Den er følsom for lys, mørkner sakte fordi den danner metall sølv.
Å skaffe
I naturen er det i form av Yodargirita-mineralet, som er β-Agi-formen.
 Yodargirita, AGI Mineral. Rob Lavinsky, Irocks.COM-CC-BY-SA-3.0/CC By-SA (https: // CreativeCommons.Org/lisenser/by-SA/3.0). Kilde: Wikimedia Commons.
Yodargirita, AGI Mineral. Rob Lavinsky, Irocks.COM-CC-BY-SA-3.0/CC By-SA (https: // CreativeCommons.Org/lisenser/by-SA/3.0). Kilde: Wikimedia Commons. I laboratoriet kan du tilberede ved å varme opp en sølvnitratoppløsning (AGNO3) Med en løsning av et alkalisk jodid, for eksempel kaliumjodid (ki). AGI -utfellingene og vasker i fravær av lys med kokende vann.
Agno3 + Ki → AGI ↓ + KNO3
Bruk i klimamodifisering
Det brukes på skyene for å endre mengden eller typen nedbør, utløser haglprosesser, spre kald tåke og svekke orkaner.
Det er spredt som et frø i kalde skyer som inneholder overtrengt flytende vann (temperaturer under 0 ° C). Dens krystallinske struktur som ligner på frysing av overfrained vann.
 Sølvjodid brukes noen ganger til å endre været. Forfatter: Tobias Hämmer. Kilde: Pixabay.
Sølvjodid brukes noen ganger til å endre været. Forfatter: Tobias Hämmer. Kilde: Pixabay. Bivirkninger av denne bruken
Etter spredningen som et frø i skyene, er AGI inne i skyenes indre og vaskes ved nedbør.
Tilstedeværelsen av oppløselig sølvjodid i regnvann er noe å ta hensyn til, ettersom det er en giftig forbindelse for både vannlevende og terrestriske og menneskelige planter og dyr.
 AGI som brukes til å generere nedbør kan være giftig for naturlige miljøer. Forfatter: Antonies ntoumas. Kilde: Pixabay.
AGI som brukes til å generere nedbør kan være giftig for naturlige miljøer. Forfatter: Antonies ntoumas. Kilde: Pixabay. Såing av skyer repetitivt over det samme området kan føre til en kumulativ effekt av denne forbindelsen. Miljøvernbyrået, eller EPA (fra engelsk Miljøvernbyrå) Tenk på AGI et vann og jordforurensende.
I følge studier i 2013 er sølvjodidkonsentrasjonen funnet i områder der denne teknikken har blitt brukt mye større enn grensen som den er giftig for noen lavere fisk og organismer.
Bruk i fotografering
AGI er et materiale som er i stand til å reagere i nærvær av lys, så det brukes til å oppnå lysfølsomme materialer som fotografiske ruller, som krystaller gjelder.
Kan tjene deg: etylenoksid: struktur, egenskaper, risikoer og brukStørrelsen på disse krystallene, også kalt korn, er det som definerer størrelsen på lysfølsomhet. En større kornstørrelse, større lysfølsomhet og er derfor mindre nødvendig for å fange bildet.
Det fotografiske papiret har et tynt gelélag der AGI -korn er suspendert.
Virkningsmekanismen
Den krystallinske strukturen til denne forbindelsen er slik at den tillater en viss bevegelse av elektroner, så når et elektron har innvirkning eller påvirker et elektron, som er kombinert med et nært sølvion som danner metallisk sølv (AG0).
AGI + Photon Crystal → E-
AG+ + og- → Ag0
Effekten av fotoner på fotografisk emulsjon er å redusere sølvionet til metall sølv, og danne det latente bildet, som er usynlig for det blotte øye, men det har skjult forskjellene i lysstyrke i den fangede scenen.
 Dette fotografiet ble oppnådd i 1862 ved bruk av AGI. Colecao Militao Augusto de Azevedo / Treatment To negativer og lysbilder gjør Servico de Documentacao Textual and Iconography - L3 Conservaca de Collections S / S Ltda / Reproduction Digital - UM Certo Olhar Imagens and Editor Ltda Ltda. / 2011. Militão Augusto de Azevedo / Public Domain. Kilde: Wikimedia Commons.
Dette fotografiet ble oppnådd i 1862 ved bruk av AGI. Colecao Militao Augusto de Azevedo / Treatment To negativer og lysbilder gjør Servico de Documentacao Textual and Iconography - L3 Conservaca de Collections S / S Ltda / Reproduction Digital - UM Certo Olhar Imagens and Editor Ltda Ltda. / 2011. Militão Augusto de Azevedo / Public Domain. Kilde: Wikimedia Commons. Det vil si at noen områder av den fotografiske rullen har mottatt fotoner og andre ikke. For å forhindre at emulsjonen reagerer, blir materialet i lysvirkningen beskyttet, og deretter tilsettes kjemiske forbindelser for å fikse bildet og gjøre det synlig.
Sølvmetall vil skape mørke områder på grunn av fargen.
Selv om vi raskt kan skaffe fotografiske bilder med smarttelefonene våre, er kjemiske fotograferingsprosesser fremdeles en grunnleggende del av kinematografiske filmer og X -ray -film, blant andre applikasjoner.
Bruk i fjerning av radioaktivt jod
På grunn av dens uløselighet har AGI blitt foreslått i en mekanisme for å fjerne jod eller radioaktivt jodid inneholdt i vandig avfall generert av kjernekraftstasjoner.
I følge studier utført i 2019 har sølv nanopartikler med zeolit muligheten til å fjerne vannjodet. I nærvær av vann oksideres nanopartiklene av Ag som er inneholdt i zeolitten, og danner Ag2Eller da genereres agionen+ som binder seg til jodid og utfeller AGI på overflaten av zeolitten.
Kan tjene deg: Kokende: konsept, typer og eksempler Sølvjodiddannelse kan brukes til å redusere forurensningen av radioaktivt jod fra kjerneavfall. Forfatter: Dirk Rabe. Kilde: Pixabay.
Sølvjodiddannelse kan brukes til å redusere forurensningen av radioaktivt jod fra kjerneavfall. Forfatter: Dirk Rabe. Kilde: Pixabay. Andre bruksområder
Det har blitt brukt til å behandle infeksjoner av animalsk slimhinne membraner i form av kolloidale suspensjoner med 5-49 vekt%. I situasjoner med betennelse i øyne, ører og nese påføres i form av en salve eller 5% salve.
AGI -nanopartikler har blitt brukt som midler for antimikrobiell terapi. I kjemiske og biokjemiske laboratorier brukes det som et reagens og fungerer som mellomledd i fremstilling av andre sølv- og jodforbindelser.
Det har blitt studert av fysikere for å ha en strømledningsmekanisme. Det brukes i optiske fibre for infrarød laser fordi den er gjennomsiktig i midten og infrarød region av lysspekteret.
Risiko
Det er giftig for mennesket gjennom alle ruter, for eksempel dermal kontakt, innånding og inntak. Det produserer hudutslett, konjunktivitt, misfarging av grå hud, konjunktiva og indre organer, hodepine, feber, laryngitt og bronkitt.
Samhandling med kobberforbindelser kan øke det mutagene potensialet til AGI.
Det er en veldig giftig forbindelse for vannlevende og terrestrisk liv, både dyr og planter. Dens skadelige effekter kan vare på miljøet.
Referanser
- ELLER.S. National Library of Medicine. (2019). Sølvjodid. Gjenopprettet fra Pubchem.NCBI.NLM.NIH.Gov.
- Curic, m. og Janc, D. (2013). Våtforekomst av såingsmiddelet etter værmodifiseringsaktiviteter. Miljø Sci Pollut Res 20, 6344-6350 (2013). Lenke gjenopprettet.Springer.com.
- Witten, n.M. (2016). Fotograferingens kjemi. Seniormetoder. University of South Carolina. Columbia. Gjenopprettet fra Scholarcommons.SC.Edu.
- Bly, d.R. (Editor) (2003). CRC Handbook of Chemistry and Physics. 85th CRC Press.
- Tauanov, Z. Og Inglezakis, V.J. (2019). Remival of Jodide fra vann ved bruk av sølv nanopartikler-imponerte syntetiske zeolitter. Science of the Total Environment 682 (2019) 259-270. Gjenopprettet fra Scientedirect.com.
- Wikimedia Foundation. (2020). Sølvjodid. Innhentet fra.Wikipedia.org.
- Matsuura, og. (2013). Optiske fibre for medisinske applikasjoner. I lasere for medisinske applikasjoner. Gjenopprettet fra Scientedirect.com.
- « Paul Ekman -biografi, teori om følelser, kommunikasjon, fungerer
- Juridisk psykologhistorie, hvilken studie, grener, eksempler på saker »

