Alkynes
- 2856
- 437
- Markus Fredriksen
 Alvento -struktur, med en trippelkobling
Alvento -struktur, med en trippelkobling Hva er alkiner?
De Alkynes De er hydrokarboner eller organiske forbindelser som presenterer i sine strukturer en trippelkobling mellom to karbonatomer. Denne trippelkoblingen (≡) regnes som en funksjonell gruppe når du representerer et aktivt sted for molekylet, og er derfor ansvarlig for deres reaktivitet.
Selv om alkyner ikke skiller seg mye fra Alko eller Alkenes, viser de større surhet og polaritet på grunn av arten av koblingene sine. Det nøyaktige uttrykket for å beskrive denne lille forskjellen er det som er kjent som Utilhet.
Alkanene er mettede hydrokarboner, mens alkinene er de mest umettet med hensyn til den opprinnelige strukturen. Hva betyr dette? At en alkan h3C-CH3 (etan) kan være dehydrogen til H2C = Ch2 (Etene) og deretter HC≡CH (Etino, eller bedre kjent som acetylen).
Legg merke til hvordan når det dannes ytterligere koblinger blant karbonatomer, reduserer antallet hydrogener knyttet til dem. Karbon, på grunn av dets elektroniske egenskaper, søker å danne fire enkle koblinger, så jo større er tendensen til å reagere (bortsett fra aromatiske forbindelser).
På den annen side er trippelkoblingen mye sterkere enn dobbelt (=) eller den enkle (-) bindingen, men til en høy energikostnad. Derfor kan de fleste hydrokarboner (Alkans og Alkenes) danne trippelbindinger ved høye temperaturer.
Som en konsekvens av de høye energiene til disse, når de bryter, slipper de veldig varme. Et eksempel på dette fenomenet kan sees når acetylen brenner med oksygen og den intense varmen fra flammen for å sveise eller smelte metaller brukes.
Acetylen er den enkleste og mest små alkyne av alle. Andre hydrokarboner kan uttrykkes fra deres kjemiske formel ved å erstatte H med alquiliske grupper (RC≡CR '). Det samme skjer i verden av organisk syntese gjennom et stort antall reaksjoner.
Denne alkyne oppstår fra reaksjonen av kalsiumoksyd i kalksteinen og Coque, råstoff som gir de nødvendige karbonatomer inne i en elektrisk ovn:
CAO + 3C => CAC2 + Co
CAC2 Det er kalsiumkarbid, en uorganisk forbindelse som til slutt reagerer med vann for å danne acetylen:
CAC2 + 2H2O => ca (å)2 + HC≡CH
Fysiske og kjemiske egenskaper til alkiner
Polaritet
Trippelkoblingen skiller alkiner fra alkaner og alkener. De tre typene hydrokarboner er apolare, uoppløselige i vann og veldig svake syrer. Imidlertid er elektronegativiteten til dobbelt- og trippelbindingskarboner større enn for enkle karbonatomer.
I følge dette er karbonatomer ved siden av trippelbindingsutbyttet til induktiv effekt negativ belastningstetthet. Av denne grunn, hvor er C≡C- eller C = C -koblingene, vil det være større elektronisk tetthet enn i resten av det kullsyreholdige skjelettet. Som en konsekvens er det et lite dipolmoment der molekylene samhandler av dipol-dipolo-krefter.
Disse interaksjonene er veldig svake hvis dipolmomentene deres blir sammenlignet med vannmolekylet eller alkohol. Dette gjenspeiles i deres fysiske egenskaper: Alkiner har generelt høyere fusjon og kokepunkter sammenlignet med de for deres mindre umettede hydrokarboner.
Kan tjene deg: de 7 viktigste biokjemi -applikasjonenePå samme måte, på grunn av deres lave polaritet, er de mindre uoppløselige i vann, men oppløselige i apolare organiske løsningsmidler, for eksempel benzen.
Surhet
Også denne elektronegativiteten forårsaker hydrogen HC≡CR er surere enn noen som er til stede i andre hydrokarboner. Derfor er alkinene arter surere enn alkener og mye mer enn alkaner. Imidlertid forblir surheten foraktelig hvis sammenlignet med karboksylsyrer.
Siden alkiner er veldig svake syrer, reagerer de bare med veldig sterke baser, for eksempel natrium amiduro:
HC≡CR + nanh2 => Hcmerkna + nh3
Fra denne reaksjonen oppnås en løsning av natriumacetylure, råstoff for syntese av andre alkyner.
Alquino -reaktivitet
Reaktiviteten til alkynene forklares med tilsetning av små molekyler til deres trippelkobling, noe som reduserer dens umettethet. Disse kan være hydrogenmolekyler, hydrogenhallogenider, vann eller halogener.
Hydrogenering
Det lille H -molekylet2 Det er veldig unnvikende og raskt, så å øke sjansene for å bli lagt til trippelkoblingen til alkinen.
Dette er vanligvis metaller (PD, PT, RH eller Ni) fint delt for å øke overflatearealet; Og på denne måten kontakten mellom hydrogen og alquino:
RC≡CR ' + 2H2 => Rch2Ch2R '
Resultatet er at hydrogen er "anker" til karbonatomer som bryter et binding, og så videre til den tilsvarende alkanen produserer, RCH2Ch2R '. Dette metter ikke bare det innledende hydrokarbonet, men endrer også molekylstrukturen.
Tilsetning av hydrogenhalogenuros
Her tilsettes det uorganiske molekylet Hx, hvor x kan være noen av halogenene (F, CL, BR eller I):
Rc≡Cr ' + hx => rch = cxr'
Hydrering
Hydrering av alkiner er når de tilsetter et vannmolekyl for å danne et aldehyd eller en keton:
Rc≡Cr ' + h2O => rch2Cor '
Hvis R 'er en H, er det et aldehyd; Hvis det er en leie, er det en Cetona. I reaksjonen dannes en forbindelse kjent som enol (RCH = C (OH) r ') som en mellomledd.
Dette lider en konvertering av den enoliske formen (C-OH) til keton (C = O) i en balanse som kalles tautomerisering.
Tilsetning av halogener
Og med hensyn til tillegg kan de diatomiske molekylene av halogener også forankres til karbonatomer (x x2= F2, Cl2, Br2 jeg hørte2):
RC≡CR ' + 2x2 => Rcx2-CX2R '
Acetylenalkylering
Fra natriumacetylure -løsningen kan andre alkiner fremstilles ved å bruke en leiebilide:
Hcmerkna + rx => hc≡CR + nax
For eksempel, hvis det var metyljodidet, ville den resulterende alkyne være:
HC≡CNA + CH3I => hc≡CCH3 + Nax
HC≡CCH3 er riktig, også kjent som MetylAcetylen.
Kjemisk struktur av alkiner
 Kjemisk struktur av alquino
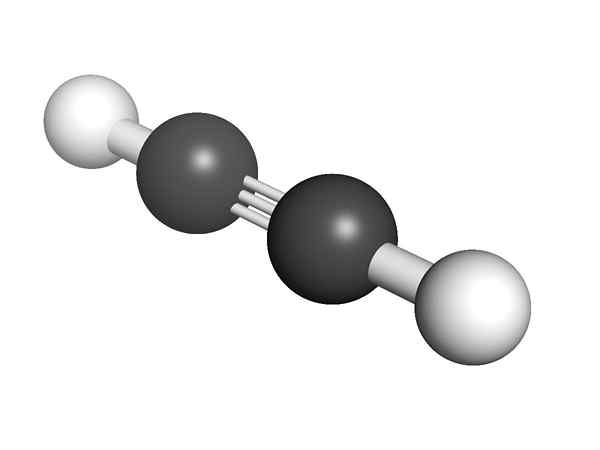
Kjemisk struktur av alquino Hva er strukturen til alkynene? I det øvre bildet vises et acetylenmolekyl. Den lineære geometrien til C≡C -lenken kan være tydelig fra den.
Derfor, der det er en trippelbinding, må molekylets struktur være lineær. Dette er en annen av de bemerkelsesverdige forskjellene mellom dem og resten av hydrokarbonene.
Det kan tjene deg: Cycopropane (C3H6)Alkanene er vanligvis representert som sikksakk, fordi de har SP -hybridisering3 og koblingene deres er atskilt 109º. De er faktisk en kovalent forent tetrahedra -kjede. Mens alkener er flate av SP -hybridisering2 av sine karbonatomer, danner mer spesifikt et trigonalt plan med separerte koblinger med 120º.
I Alkynes er orbital hybridisering SP, det vil si at de har 50% av S og 50% av en P. Det er to SP -hybride orbitaler som er knyttet til H -atomer i acetylen- eller alkyne -grupper i alkinene.
Avstanden både H eller R er 180º, i tillegg til at bare på denne måten kan de rene karbonbanene orbitaler danne trippelbindingen. Av denne grunn er lenken -c≡C- lineær. Å se strukturen til ethvert molekyl.
Avstand fra lenker og terminal almisser
Karbagon i trippelbindingen er i mindre avstand enn i dobbelt eller den enkle lenken. Med andre ord, C≡C er kortere enn C = C og at C-C. Som et resultat er lenken sterkere fordi de to π -koblingene bidrar til å stabilisere den enkle lenken σ.
Hvis trippelbindingen er på slutten av en kjede, er det en terminal alkyne. Derfor må formelen til nevnte forbindelse være HC≡CR, der H bemerker kjeden eller starten av kjeden.
Hvis det tvert imot er en trippel intern lenke, er formelen RC≡CR ', der R og R' er høyre og venstre side av kjeden.
Nomenklatur av Alquinos
Hvordan blir alkiner utnevnt i henhold til reglene diktert av IUPAC? På samme måte som Alquenos og Alkenes er utnevnt. For å gjøre dette endres suffikset -o eller -eno for suffikset -inoen.
For eksempel: HC≡CCH3 Det er utnevnt til tips, siden den har tre karbonatomer, for eksempel propan (Cho3Ch2Ch3). HC≡CCH2Ch3 Det er 1-butino, som er en terminal alkyne. Men i tilfelle av Cho3C≡CCH3 Dette er 2-butino, og i denne er trippelkoblingen ikke terminal, men intern.
Ch3C≡CCH2Ch2(Ch3)2 Det er 5-metyl-2-heksin. Karboner starter fra siden nærmest trippelkoblingen.
En annen type alkiner er cycloalquins. For dem er det nok å erstatte suffikset -ano med -ino av den tilsvarende cycloalcan. Dermed blir syklopropanen som har en trippelbinding kalt Cyclopropin (som ikke eksisterer).
Når det er to trippelkoblinger, blir prefikset DI lagt til navnet-. Det har som eksempler på HC≡C-C≡H, diacetylen eller propadin; Og til HC≡C-C-C≡H, Butadiino.
Alquinos bruker
Acetylen eller etino
Den minste av alkynene tykner det mulige antall bruksområder for disse hydrokarbonene. Fra det gjennom Alks kan andre organiske forbindelser syntetiseres. Den gjennomgår også oksidative reaksjoner for å oppnå etanol, eddiksyre, akrylsyre, blant andre.
Kan tjene deg: litiumhydrid: struktur, egenskaper, innhenting, brukAndre av bruken består i å gi varmekilden for å begeistre atomer; Mer spesifikk, e av metallkationer i bestemmelser ved atomabsorpsjonsutslipp, mye brukt spektroskopisk teknikk.
Naturlige alkiner
De eneste eksisterende metodene for å fremstille alkyner er ikke bare syntetiske eller med varmepåføring i fravær av oksygen, men også biologisk.
I disse enzymene som kalles Acetylese, som kan nekte en dobbeltbinding. Takket være dette oppnås mange naturlige kilder til alkyner.
Etter dette kan disse kildene trekkes ut giftstoffer, motgift, medisiner eller annen forbindelse som gir noen fordel; Spesielt når det gjelder helse. Alternativene er mange når du endrer sine opprinnelige strukturer og har dem som støtte for nye alkiner.
Eksempler på alkyner
Så langt er det nevnt mange eksempler på alkiner. Noen kommer imidlertid fra veldig spesifikke kilder eller har spesielle molekylære strukturer: de er polyacetyle.
Dette betyr at det kan være mer enn en trippelkobling som er en del av en veldig stor struktur, og ikke bare av en enkel kullsyreholdig kjede.
Tarirektyre
 Tarisk syrestruktur
Tarisk syrestruktur Tarirric acid kommer fra en plante som ligger i Guatemala kalt Picramnia Tariri. Den er spesielt trukket ut fra oljen fra frøene.
I sin molekylære struktur kan en enkelt trippelkobling observeres som skiller en apolar hale fra et polært hode; Derfor kan det betraktes som et amfipatisk molekyl.
Histrionicotoxin
 Histrionicotoxin Structure
Histrionicotoxin Structure Histrionicotoxin er en gift adskilt av huden til innbyggere i Colombia, Brasil og andre latinamerikanske land. Den har to trippel konjugerte koblinger med en dobbeltbinding. Begge er terminaler og er atskilt med en seks -karbonring og en syklisk amin.
Cicutoxin
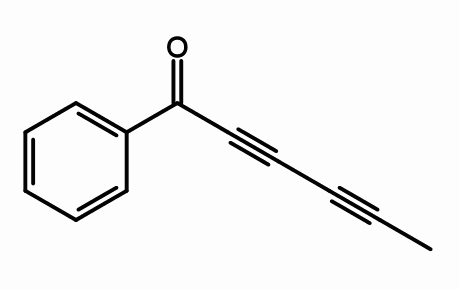 Cicutoxin Structure. Av Giorgiogp2 [CC BY-SA 3.0 (https: // creativecommons.Org/lisenser/by-SA/3.0) eller GFDL (http: // www.gnu.Org/copyleft/fdl.html)], fra Wikimedia Commons
Cicutoxin Structure. Av Giorgiogp2 [CC BY-SA 3.0 (https: // creativecommons.Org/lisenser/by-SA/3.0) eller GFDL (http: // www.gnu.Org/copyleft/fdl.html)], fra Wikimedia Commons Fra molekylstrukturen til cicutoxin, hvor er trippelkoblingene? Hvis dobbeltbindingene er flate, slik de blir sett riktig, og de enkle koblingene er tetrahedraler, som i endene, er trippelene lineære og er i skråningen (\).
Denne forbindelsen består av et nevrotoksin som hovedsakelig finnes i vannhelingsplanten.
Capillina
 Capillina -struktur. Av Klever [CC0], fra Wikimedia Commons
Capillina -struktur. Av Klever [CC0], fra Wikimedia Commons Det er en alkyne som er til stede i essensiell olje av Artemis -planter som brukes som et soppdrepende middel. To trippel påfølgende koblinger kan observeres, mer korrekt konjugert.
Hva betyr det? At trippelbindingene resonerer langs hele karbonkjeden og involverer at dobbeltbindingen C = O åpnes for C-O-.
Pargilin
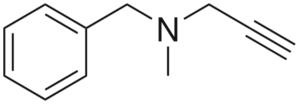 Struktur av Pargilin
Struktur av Pargilin Det er en alty med antihypertensiv aktivitet. Å analysere strukturen i deler er: en benkilokruppe til venstre, en tertiær amin i midten og en høyre -wing; det vil si en terminalegruppe.
Referanser
- Francis a. Tortoiseshell. Organisk kjemi. Karboksylsyrer. (Sjette utgave., Side 368-397). Mc Graw Hill.
- Brennan, John. (10. mars 2018). Eksempel på alkyner. Scienting. Tatt fra: Scienting.com
- Byju's. (2018). Trippelbinding i Alkynes. Hentet fra: byjus.com
- Encyclopedia of Eksempler (2017). Alkynes. Gjenopprettet fra: eksempler.co
- Kevin a. Boudreaux. Alkynes. Hentet fra: Angelo.Edu
- Robert c. Neuman, jr. Alkener og alkyner. [PDF]. Hentet fra: Chem.Ucr.Edu

