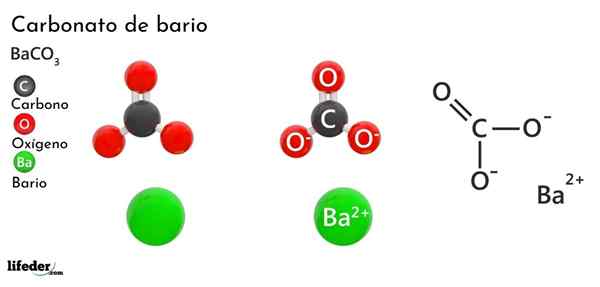
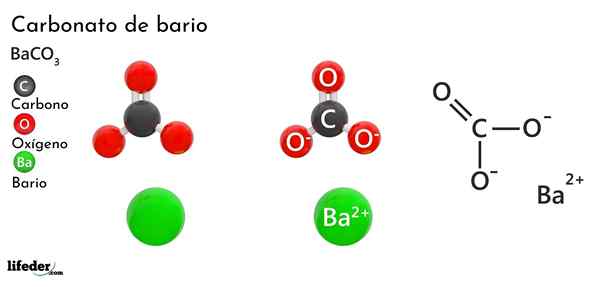
Bariumkarbonat (BACO3)
- 3355
- 887
- Marius Aasen
Hva er bariumkarbonat?
Han bariumkarbonat Det er et uorganisk salt av metallbario, nest siste element i gruppe 2 i det periodiske bordet og som tilhører de alkalinotrous metaller. Den kjemiske formelen er Bacchus3 Og det er tilgjengelig i markedet i form av hvitt krystallinsk støv.
Hvordan oppnås det? Metallbarium finnes i mineraler, for eksempel baritten (Baso4) og Whiterite (Bacchus3). Whiterite er assosiert med andre mineraler som forblir renhetsnivåer til dens hvite krystaller i bytte mot farge.
Å generere Bacchus3 av syntetisk bruk er det nødvendig å eliminere urenhetene i hvitheten, som indikert med følgende reaksjoner:
Bacchus3(s, uren) + 2nh4Cl (S) + Q (varme) => BACL2(aq) + 2nh3(g) + h2Eller (l) + co2(g)
Bacl2(aq) + (NH4)2Co3(S) => Bacchus3(S) + 2NH4CL (aq)
Barita er imidlertid den viktigste kilden til barium, og det er grunnen til at industriproduksjonene av bariumforbindelser starter fra dette. Dette mineralet syntetiserer bariumsulfid (BAS), et produkt som syntesen av andre forbindelser og bacchus strømmer3:
Bas (S) + Na2Co3(S) => Bacchus3(S) + Na2H.H)
Bas (S) + CO2(g) + h2Eller (l) => bacchus3(S) + (NH4)2S (aq)
Bario karbonategenskaper
 Bariumkarbonatstøv
Bariumkarbonatstøv Det er en støvete, hvit og krystallinsk. Det er toalett, unraveling og molekylvekten er 197,89 g/mol. Den har en tetthet på 4,43 g/ml og et ikke -eksisterende damptrykk.
Det har brytningsgrad på 1.529, 1.676 og 1.677. Witherita avgir lys når den absorberer ultrafiolett stråling: fra et sterkt hvitt lys med blålige toner, til et gult lys.
Det er svært uoppløselig i vann (0,02 g/l) og i etanol. I HCL -syreoppløsninger danner det oppløselige bariokloridsaltet (BACL2), som forklarer dens løselighet i disse sure mediene. Når det gjelder svovelsyre, utløser hvor uoppløselig saltbase4.
Kan tjene deg: Beryl Oxide (Beeo)Bacchus3(S) + 2HCl (aq) => BACL2(aq) + co2(g) + h2Eller (l)
Bacchus3(S) + H2SW4(aq) => baso4(S) + CO2(g) + h2Eller (l)
Siden det er et ionisk faststoff, er det også uoppløselig i de apolare løsningsmidlene. Bariumkarbonatet smelter ved 811 ºC; Hvis temperaturen øker rundt 1380-1400 ºC, lider den salte væsken en kjemisk nedbrytning i stedet for å koke. Denne prosessen skjer for alle metallkarbonater: MCO3(S) => MO (S) + CO2(g).
Termisk nedbrytning
Bacchus3(S) => Bao (S) + CO2(g)
Hvis ioniske faste stoffer er preget av å være veldig stabile, hvorfor bryter karbonater sammen? Endrer metallet temperaturen som faststoffet brytes ned? Ionene som utgjør bariumkarbonat er BA2+ og co32-, begge klumpete (det vil si med store ioniske radioer). Co32- Han er ansvarlig for nedbrytning:
Co32-(S) => o2-(g) + co2(g)
Oksidionet (eller2-) Metall er knyttet til metall, metalloksid. MO genererer en ny ionisk struktur der, som en generell regel, jo mer lik størrelsen på ionene er, jo mer stabil er den resulterende strukturen (nettverksentalpi). Det motsatte skjer hvis ionene m+ Jeg2- De har veldig ulik ioniske radioer.
Hvis nettverksentalpien er stor, er nedbrytningsreaksjonen energisk foretrukket, og krever lavere oppvarmingstemperaturer (lavere kokepunkter) mindre).
På den annen side, hvis Mo har liten nettverks entalpi (som for Bao, der BA2+ Den har større ionisk radio enn eller2-) Nedbrytning er mindre foretrukket og krever høyere temperaturer (1380-1400 ºC). I MGCO -tilfeller3, Tyv3 og SRCO3, De bryter sammen ved lavere temperaturer.
Kan tjene deg: magnesium: historie, struktur, egenskaper, reaksjoner, brukKjemisk struktur
Anionen co32- Den har en dobbeltbinding som resonerer mellom tre oksygenatomer, to av disse negativt ladet for å tiltrekke kation BA2+.
Mens begge ionene kan betraktes som lastede kuler, CO32- Den har en flat trigonal geometri (den flate trekanten trukket av de tre oksygenatomene), muligens er en negativ "pute" for BA2+.
Disse ionene samhandler elektrostatisk for å danne et krystallinsk arrangement av en ortorrhrombisk type, og er de overveiende ioniske bindinger.
I så fall, hvorfor er ikke bacchus løselig3 I vann? Forklaringen er ganske enkelt basert på det faktum at ioner er bedre stabilisert i det krystallinske nettverket, enn hydrert med sfæriske molekylære lag med vann.
Fra en annen vinkel gjør vannmolekyler det vanskelig å overvinne sterke elektrostatiske attraksjoner mellom de to ionene. Innenfor disse krystallinske nettverkene kan de huse urenheter som gir farge til sine hvite krystaller.
applikasjoner
Ved første øyekast, en bacchus -del3 Det kan ikke love noen praktisk anvendelse i dagliglivet, men hvis det er en krystall av det hvite mineralet, hvitt som melk, begynner det å være fornuftig hvorfor dets økonomiske etterspørsel.
Brukes til å produsere bariumglass eller som tilsetningsstoff for å styrke dem. Det brukes også i produksjonen av optisk glass.
På grunn av det store nettverket og uoppløselig entalpi, brukes det i fremstilling av forskjellige typer legeringer, gummi, ventiler, gulv av gulv, malerier, keramikk, smøremidler, plast, fett og sement.
Det brukes også som gift for mus. Oppsummert brukes dette saltet til å produsere andre bariumforbindelser, og fungerer dermed som elektroniske enheter materialer.
Kan tjene deg: sulfanyl syre: struktur, egenskaper, syntese, brukBacchus3 Det kan syntetiseres som nanopartikler, og uttrykker veldig små skalaer nye interessante egenskaper til Whiterite. Disse nanopartiklene brukes til å permeat metalloverflater, spesielt kjemiske katalysatorer.
Det har vist seg å forbedre oksidasjonskatalysatorene, og som på en eller annen måte favoriserer migrasjonen av oksygenmolekyler ved overflaten.
De anses som redskaper for å akselerere prosessene der oksygen er innarbeidet. Og til slutt er de vant til å syntetisere supramolekylære materialer.
Risiko
Bacchus3 Det er giftig på grunn av inntak, noe som forårsaker en uendelig ubehagelige symptomer som fører til død på grunn av respirasjonssvikt eller hjertestans; Av denne grunn anbefales det ikke å bli transportert ved siden av spiselige varer.
Det gir rødhet i øynene og huden, i tillegg til hoste og smerter i halsen. Det er en giftig forbindelse, selv om den lett kan manipuleres med bare hender hvis inntaket unngås for enhver pris.
Det er ikke brannfarlig, men ved høye temperaturer bryter det ned for å danne Bao og CO2, Giftige og oksiderende produkter som kan få andre materialer til å brenne.
I organismen blir barium avsatt i bein og annet vev, og erstatter kalsium i mange fysiologiske prosesser. Det blokkerer også kanalene der K -ionene reiser+, forhindrer diffusjon gjennom cellemembraner.
Referanser
- Pubchem. (2018). Bariumkarbonat. Hentet 24. mars 2018 fra Pubchem: Pubchem.NCBI.NLM.NIH.Gov
- Wikipedia. (2017). Bariumkarbonat. Hentet 24. mars 2018, fra Wikipedia: i.Wikipedia.org
- ChemicalBook. (2017). Bariumkarbonat. Hentet 24. mars 2018 fra ChemicalBook: ChemicalBook.com
- Robbins Manuel a. (1983).Robbins The Collector's Book of Fluorescent Minerals. Fluorescerende mineraler Beskrivelse, P-117.
- Shiver & Atkins. (2008). Uorganisk kjemi. I Strukturen av enkle faste stoffer (Fjerde utgave., p. 99-102). Mc Graw Hill.