Asymmetrisk karbon
- 3479
- 11
- Marius Aasen
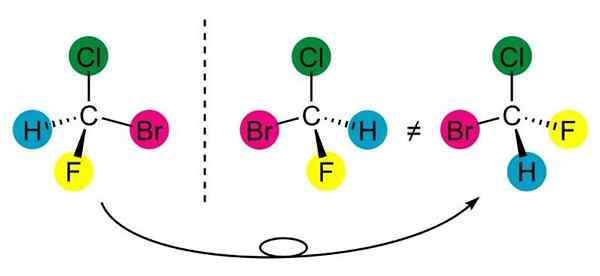
 Bromoklorofluormetan, eksempel på asymmetrisk karbon eller chiral molekyl. Kilde: Calvero., Wikimedia Commons
Bromoklorofluormetan, eksempel på asymmetrisk karbon eller chiral molekyl. Kilde: Calvero., Wikimedia Commons Hva er et asymmetrisk karbon?
EN Asymmetrisk karbon Det er et karbonatom som er knyttet til fire forskjellige kjemiske elementer fra hverandre. I denne strukturen er karbonatomet i sentrum, og kobler resten av elementene gjennom det.
Bromokloroyodometanmolekylet er et klart eksempel på asymmetrisk karbon. I dette tilfellet er karbonatomet knyttet til brom-, klor-, jod- og hydrogenatomer, gjennom unike bindinger.
Denne typen formasjoner er veldig vanlig i organiske forbindelser, for eksempel glyseraldehyd, et enkelt sukker som oppnås som et produkt av prosessen med fotosyntesen i planter.
Kjennetegn på asymmetrisk karbon
- Asymmetriske karbonatomer er tetrahedrale karbonatomer som er koblet til fire forskjellige elementer fra hverandre.
- Denne konfigurasjonen ligner en stjerne: asymmetrisk karbon fungerer som kjernen i strukturen, og resten av komponentene starter fra den for å danne de respektive grenene til strukturen.
- At elementene ikke gjentar hverandre, gir denne formasjonen konnotasjonen av asymmetrisk eller chiral.
- Hvert element må festes til asymmetrisk karbon gjennom en enkelt lenke. Hvis elementet var bundet til karbon av en dobbel eller trippelbinding, ville ikke karbonet lenger være asymmetrisk.
- Hvis en asymmetrisk struktur blir sammen med et karbonatom to ganger, kunne sistnevnte ikke være asymmetrisk.
- Hvis den i en kjemisk forbindelse har to eller flere asymmetriske karbonatomer, induseres tilstedeværelsen av qillaritet i den totale strukturen.
Quillarity er den egenskapen som objekter ikke har overlappet med bildet som reflekterer i et speil. Det vil si at begge bildene (ekte objekt kontra refleksjonen) er asymmetriske fra hverandre.
Kan tjene deg: molekylært oksygen: struktur, egenskaper, brukFølgelig, hvis du har et par strukturer med asymmetriske karbonatomer, og hvert av elementene er like, kan ikke begge strukturer overlappe hverandre.
I tillegg kalles hver struktur enantiomer eller optisk isomer. Disse strukturene har identiske fysiske og kjemiske egenskaper, de er bare forskjellige i sin optiske aktivitet, det vil si responsen de presenterer på det polariserte lyset.
Eksempler på asymmetriske karbonatomer
Denne typen strukturer er vanlig i følgende organiske forbindelser:
- Karbohydrater.
- Etylgrupper, for eksempel i strukturen til -Ch2Ch3, -OH, -Ch2Ch2Ch3, -Ch3 og -Ch2NH3.
- Asymmetriske karbonatomer er også til stede i medisiner, som tilfellet er med pseudoefedrina (C10HfemtenNei), et medisiner som brukes i behandling av nesetetthet og trykk i bihulene.
- 2-klorobutano.
- Butan-2-OC.
Referanser
- Asymmetrisk karbon, srioisomer og epimer. Hentet fra fakultetet.Une.Edu.
- Asymmetrisk karbon. Gjenopprettet fra Es.Wikipedia.org.

