Ketoner typer, egenskaper, nomenklatur, bruk, eksempler
- 4453
- 15
- Mathias Aas
De ketoner De er organiske forbindelser som har en karbonyl (-co) gruppe. De er enkle forbindelser der karbonen i karbonylgruppen er knyttet til to karbonatomer (og deres substituentkjeder)). Ketonene er "enkle" fordi de ikke har reaktive grupper som -OH eller -Cl forenet til karbon.
Anerkjent som polare forbindelser, er ketoner vanligvis løselige og flyktige, noe som gjør dem til gode løsningsmidler og tilsetningsstoffer for parfymer. I tillegg er de enkle å tilberede, relativt stabile og har høy reaktivitet, noe som har gjort dem til en nesten perfekt mellomforbindelse for å fremstille mer komplekse organiske forbindelser.
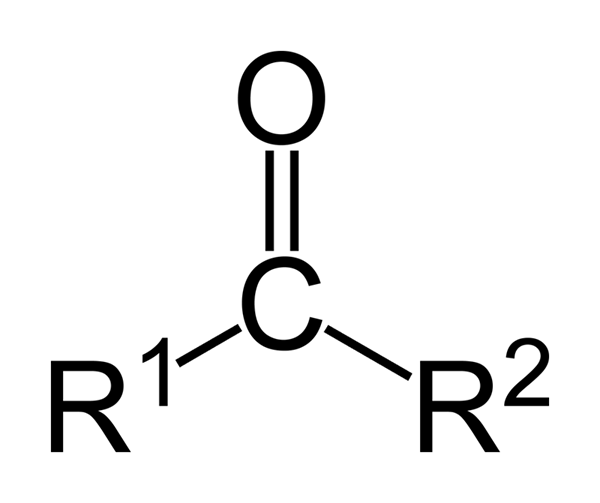
 Generell formel av ketoner
Generell formel av ketoner Endelig er eliminering av ketoner fra menneskekroppen vanligvis assosiert med et lavt sukkernivå (i diabetiker og/eller ekstreme faste tilfeller), noe som kan forårsake alvorlige helseproblemer for pasienten.
[TOC]
Generell formel av ketoner
Ketonene er karbonylforbindelser der denne gruppen er knyttet til to grupper av hydrokarboner; Disse kan være alkylgrupper, grupper av benzenringer eller begge deler.
En keton kan representeres ganske enkelt som r- (c = o) -r ', der r og r' er to kjeder av ethvert hydrokarbon (alko, alkener, alkiner, sykloalcanos, derivater av benzen og andre). Det er ingen ketoner med et hydrogen festet til karbonylgruppen.
Det er et bredt utvalg av metoder for fremstilling av ketoner i industri- og laboratoriefeltet; I tillegg er det viktig å merke seg at ketoner kan syntetiseres av forskjellige organismer, inkludert mennesker.
I bransjen involverer den vanligste metoden for syntese av ketoner oksidasjon av hydrokarboner, typisk med bruk av luft. I liten skala blir ketoner vanligvis fremstilt gjennom oksidasjon av sekundære alkoholer, noe som gir en cetona og vannprodukter som produkter.
Utover disse vanligste metodene, kan ketoner syntetiseres gjennom alkener, alkyner, salter av nitrogenforbindelser, estere og mange andre forbindelser, noe som gjør dem lett oppnådd.
Typer ketoner
Det er flere klassifiseringer for ketoner, avhengig hovedsakelig av substituenter i deres R -kjeder. De vanligste klassifiseringene for disse stoffene er utnevnt nedenfor:
I henhold til strukturen i kjeden
I dette tilfellet er ketonen klassifisert ved måten kjeden er strukturert på: alifatiske ketoner er de som har to R- og R -radikaler som har alkylradikal form (alkaner, alkener, alkiner og sykloalcanos).
Det kan tjene deg: Isoamylalkohol: Struktur, egenskaper, bruksområder og risikoerPå den annen side er de aromatiske de som danner derivater av benzen, mens de fremdeles er ketoner. Endelig er blandede ketoner de som har en alquilisk og radikal r 'aril, eller omvendt.
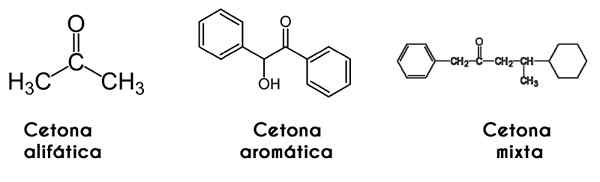 Fra venstre mot høyre: Propanona, Benzofrona og fenylmetilbutanon. Wikimedia Commons -bilder.
Fra venstre mot høyre: Propanona, Benzofrona og fenylmetilbutanon. Wikimedia Commons -bilder. I henhold til symmetrien til deres radikaler
I dette tilfellet studeres R- og R -radikaler av karbonylgruppen; Når disse er de samme (identiske) kaller ketonen seg symmetrisk; Men når de er forskjellige (som de fleste ketoner), kaller det seg asymmetrisk.
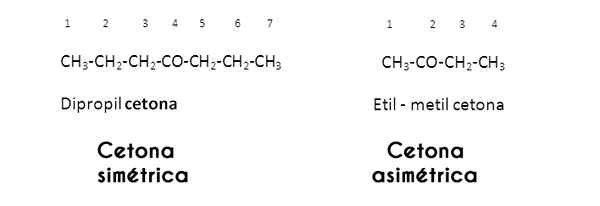 Bilder via Wikimedia Commons.
Bilder via Wikimedia Commons. I henhold til metning av dets radikaler
Ketoner kan også klassifiseres i henhold til metning av karbonkjedene; Hvis disse er i form av alkaner, kaller ketonen seg mettet keton. På den annen side, hvis kjedene er som alkener eller alkiner, kalles ketonen umettet keton.
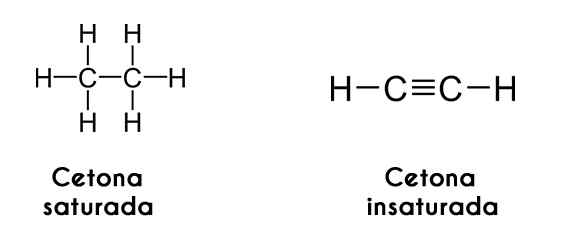 Til venstre, acetylen høyre. Bilder via Wikimedia Commons.
Til venstre, acetylen høyre. Bilder via Wikimedia Commons. Dicetoner
Dette er en klasse bortsett fra Cetona, siden kjedene til denne ketonen har to karbonylgrupper i sin struktur. Noen av disse ketonene har unike egenskaper, for eksempel en større koblingslengde mellom karbonatomer.
For eksempel er dicetoner avledet fra cykloheksanen kjent som kinoner, som bare er to: orto-benzokinon og benzokinon.
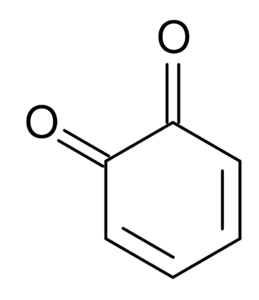 Ortho-Benzoquinone. Sør på engelsk Wikipedia / Public Domain
Ortho-Benzoquinone. Sør på engelsk Wikipedia / Public Domain Fysiske og kjemiske egenskaper til ketoner
Ketonene, som de fleste aldehydos, er flytende molekyler og har en serie fysiske og kjemiske egenskaper som varierer avhengig av lengden på kjedene. Egenskapene er beskrevet nedenfor:
Kokepunkt
Ketonene er svært ustabile, betydelig polare og kan ikke donere hydrogener for hydrogenbindinger (de har ikke hydrogenatomer bundet til karbonylgruppen), så de har høyere kokested enn alkener og etere, men lavere enn alkoholene med samme molekylvekt.
Kokepunktet til en keton øker når størrelsen på molekylet øker. Dette skyldes intervensjonen fra van der Waals og Dipolo-Dipolos styrker, som krever en større mengde energi for å skille tiltrukket atomer og elektroner i molekylet.
Løselighet
Løseligheten av ketoner har en sterk innflytelse i en del av kapasiteten til disse molekylene til å akseptere hydrogener i deres oksygenatom og danner dermed hydrogenbinding med vann. I tillegg er krefter av tiltrekning, spredning og dipol-dipol mellom ketoner og vann, som øker deres oppløselige effekt krefter.
Kan tjene deg: jern (element): egenskaper, kjemisk struktur, brukKetonene mister løselighetskapasiteten, jo større molekylet, siden de begynner å kreve mer energi for å løse opp i vann. De er også løselige i organiske forbindelser.
Surhet
Takket være karbonylgruppen deres har ketoner en sur karakter; Dette skjer på grunn av resonansstabiliseringskapasiteten som denne funksjonelle gruppen besitter, som kan gi protoner av dobbeltbindingen for å danne en konjugert base kalt enol.
Reaktivitet
Ketoner er en del av et stort antall organiske reaksjoner; Dette skjer på grunn av mottakeligheten av karbonylkarbonet mot det nukleofile tilsetningen, i tillegg til polariteten i dette.
Som nevnt ovenfor, er den store reaktiviteten til ketoner laget av et anerkjent mellomprodukt som fungerer som grunnlag for å syntetisere andre forbindelser.
Nomenklatur
Ketonene er navngitt i henhold til prioriteten eller viktigheten av karbonylgruppen i hele molekylet, så når du har et molekyl styrt av karbonylgruppen, blir ketonen navngitt ved å legge til suffikset "-ona" til navnet på hydrokarbonet.
Det tar som hovedkjeden som av større lengde som karbonylgruppen har, og deretter heter molekylet. Hvis karbonylgruppen ikke har noen prioritet fremfor de andre funksjonelle gruppene i molekylet, identifiseres den med "-oxo".
For mer kompliserte ketoner kan den funksjonelle gruppens plassering identifiseres med et tall, og i tilfelle av dicetoner (ketoner med to substituenter r og r 'identisk), er molekylet navngitt med suffikset “-Diona”.
Til slutt kan ordet "Cetona" også brukes etter å ha identifisert de radikale kjedene knyttet til karbonylfunksjonsgruppen.
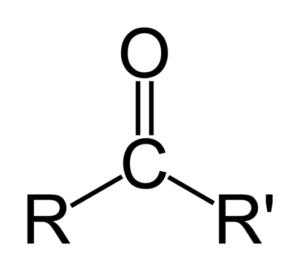
Forskjell mellom aldehydos og ketoner
Den største forskjellen mellom aldehyder og ketoner er tilstedeværelsen av et hydrogenatom festet til karbonylgruppen i aldehyder.
Dette atomet har en viktig effekt når det gjelder å involvere et molekyl i en oksidasjonsreaksjon: en aldehyd vil danne en karboksylsyre eller et salt av karboksylsyre, avhengig av om oksidasjon oppstår under syre eller basiske forhold under syre eller grunnleggende forhold.
På den annen side har en cetona ikke dette hydrogenet, så de minste trinnene som er nødvendige for oksidasjon, oppstår ikke.
Det er metoder for å oksidere en keton (med oksidasjonsmidler som er mye kraftigere enn de som vanligvis brukes), men de bryter ketonmolekylet, og skiller det først i to eller flere deler.
Kan tjene deg: ionisering i fysikk og kjemi: konsept, prosess og eksemplerIndustrielt og dagligliv bruker
I bransjen observeres ketoner i parfymer og malerier, og tar stabilisering og kondompapirer som forhindrer at andre komponenter i blandingen nedbryter; De har også et bredt spekter som løsningsmidler i de bransjene som produserer eksplosiver, malerier og tekstiler, i tillegg til farmasøytisk.
Aceton (den minste og mindre ketonen) er en veldig godt anerkjent løsningsmiddelverden.
I naturen kan ketoner vises som sukker, kalt kesuser. Ketosasene er monosakkarider som inneholder en cetona med molekyl. Den mest kjente ketosen er fruktose, sukkeret som finnes i frukt og honning.
Biosyntesen av fettsyrer som oppstår i cytoplasma av dyreceller forekommer også ved virkningen av ketoner. Til slutt, og som nevnt ovenfor, kan det være en høyde av ketoner i blodet etter faste eller i diabetiske tilfeller.
Eksempler på ketoner
Butanona (C4H8ENTEN)
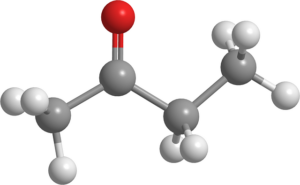 Butanonmolekyl. Kilde: Pixabay.
Butanonmolekyl. Kilde: Pixabay. Også kjent som MEK (eller MEC), produseres denne væsken i stor skala i bransjen og brukes som et løsningsmiddel.
Cyclohexanon (ca6H10ENTEN)
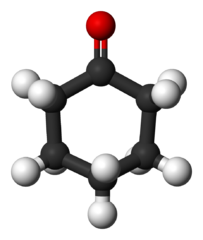 Cyclohexanon molekyl. Benjah-BMM27 / Public Domain
Cyclohexanon molekyl. Benjah-BMM27 / Public Domain Produsert i stor skala, brukes denne ketonen som en forløper for det nylonsyntetiske materialet.
Testosteron (c19H22ENTEN2)
 Testosteronmolekyl. Wikimedia Commons
Testosteronmolekyl. Wikimedia Commons Det er hovedhormonet i det mannlige kjønn og et anabole steroid, funnet i de fleste virveldyr.
Progesteron (catjueenH30ENTEN2)
 Medroxiprogesteronacetat, cyclofemin -komponent
Medroxiprogesteronacetat, cyclofemin -komponent Endogent steroid og seksuell hormon involvert i menstruasjonssyklusen, graviditet og embryogenese hos mennesker og andre arter.
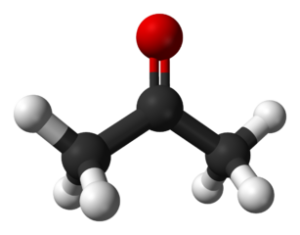
Aceton (Ch3(CO) CH3)
 Acetonforbindelse. Benjah-BMM27 / Public Domain
Acetonforbindelse. Benjah-BMM27 / Public Domain Også kjent som Propanona, det er en fargeløs forbindelse som brukes til fremstilling av forskjellige industriprodukter som plast, samt for hjemmehygieneprodukter og kosmetikk som fjerning.
Kortison (catjueenH28ENTEN5)
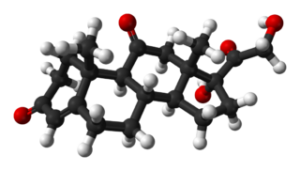 Kortison. Benjah-BMM27 / Public Domain
Kortison. Benjah-BMM27 / Public Domain Steroidhormon som brukes til å bekjempe visse plager og tilstander som betennelser, kviser, allergier og andre typer hudreaksjoner, astma eller kreft og leukemi.
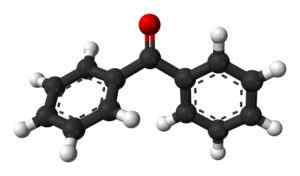
Benzofenona (ca1. 3H10ENTEN)
 Benzofenom. Benjah-BMM27 / Public Domain
Benzofenom. Benjah-BMM27 / Public Domain Sammensatt mye brukt i opprettelsen av parfymer og andre kosmetiske eller solbeskyttelsesprodukter på grunn av dens aromatiske sammensetning.
Referanser
- Wikipedia. (s.F.). Keton. Hentet fra IN.Wikipedia.org
- Britannica, e. (s.F.). Keton. Hentet fra Britannica.com
- University, m. S. (s.F.). Aldehyder og ketoner. Hentet fra kjemi.MSU.Edu
- Chemguide. (s.F.). Introduksjon aldehyder og ketoner. Hentet fra Chemguide.co.Storbritannia
- Calgary, u. ENTEN. (s.F.). Ketoner. Hentet fra Chem.Ucalgary.Ac

