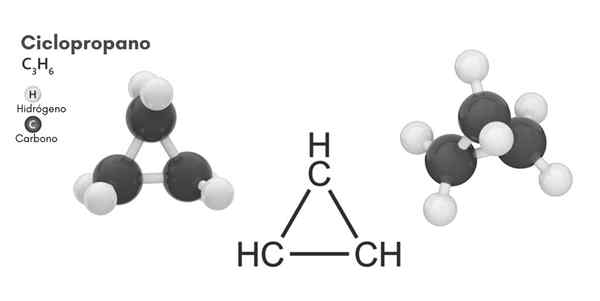
Cycopropan (C3H6)
- 4371
- 1341
- Prof. Oskar Aas
Hva er cyclopropane?
Han Sykling Det er et syklisk molekyl som har molekylformelen C3H6, og det består av tre karbonatomer forenet sammen i form av en ring. I kjemi er det en familie av mettede hydrokarboner som har et skjelett dannet av karbonatomer forent av enkle ring -formede bindinger.
Denne familien består av et variert antall molekyler (som avviker med lengden på dens viktigste kullsyreholdige kjede), og er kjent for å ha raskere smelting og kokepunkter enn for høye kjeder, i tillegg til større reaktivitet enn disse disse.
Cycropotus ble oppdaget i 1881 av en østerriksk kjemiker kalt August Freund, som var fast bestemt på å vite hva det giftige elementet var i etylen og hvem som tenkte at det var den samme syklopropanen.
Likevel var det først på 1930 -tallet at det begynte å bli produsert på industrielt nivå, da de oppdaget bruken av dem som anestesi, for før det øyeblikket var de ikke en kommersiell attraksjon.
Kjemisk struktur
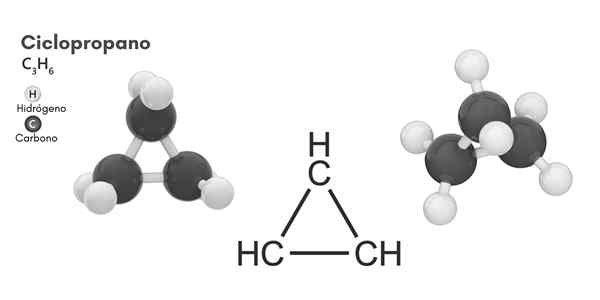
 Molekylær struktur av cyklopropan
Molekylær struktur av cyklopropan Sykling, molekylær formel C3H6, Den består av tre små karbonatomer som binder seg i en konfigurasjon slik at en ring dannes, og etterlater en molekylær symmetri av D3H I hvert karbon i kjeden.
Strukturen til dette molekylet krever at koblingsvinklene som er dannet fra omtrent 60º, mye mindre enn de på 109,5º som er observert mellom hybridene SP -atomer3, som er en mer stabil vinkel termodynamisk.
Dette fører til ringen som lider av en mer betydelig strukturell spenning enn andre strukturer av denne typen, i tillegg til en naturlig vridningsspenning som den har ved den formørkede konformasjonen av dens hydrogenatomer.
Kan tjene deg: enzymatisk kinetikkAv samme grunn er bindingene som dannes mellom karbonatomer i dette molekylet betydelig svakere enn i vanlige alkaner.
På en særegen måte og i motsetning til andre koblinger der nærheten mellom to molekyler symboliserer større koblingsenergi, har bindingene mellom karbonene i dette molekylet en særegenhet med å ha en lengde mindre enn de andre alkanene (på grunn av deres geometri), og på samme tid de er svakere enn fagforeningene mellom dem.
I tillegg er syklopropanen.
Cyclo -En -egenskaper
Kokepunkt
Sammenlignet med de andre vanligste sykloalcanos, syklopropanen.
På den annen side, sammenlignet med den lineære propanen, syklopropanen.
Smeltepunkt
Fusjonspunktet for cyklopropan. Likevel er det ikke den eneste cykloalcano som smelter ved en temperatur mindre enn null, og kan observere dette fenomenet også i syklobutan, cyclopentano og cycloheptan.
Så når det gjelder lineær propan, smelter den ved en temperatur på mindre enn 187 ºC under null.
Tetthet
Cycropopan har den høyeste tettheten blant cycloalcanos, og er mer enn to ganger til den tetteste vanlige syklusen (1 879 g/l for cyklopropan, og overgår syklodecano med 0,871).
Kan tjene deg: aluminiumoksyd: struktur, egenskaper, bruksområder, nomenklaturDet er også en høyere tetthet i syklopropanen enn i lineær propan. Forskjellen i koke- og fusjonspunkter mellom lineære og cycloalcanos alkaner skyldes større London -styrker, som øker på grunn av ringformen som tillater større kontaktområde mellom indre atomer å være.
Reaktivitet
Reaktiviteten til syklopropanen.
Takket være dette kan syklopropan lettere skilles, og kan oppføre seg som Alqueno i visse reaksjoner. Faktisk kan den ekstreme reaktiviteten til syklopropan-oksygenblandinger bli en fare for eksplosjon.
Bruk/applikasjoner
Den kommersielle bruken av cyclopropane par excellence er som et bedøvelsesmiddel, og studerer denne egenskapen for første gang i 1929.
Cyclo -Ew er et kraftig bedøvelsesmiddel for rask handling, som ikke irriterer luftveiene eller presenterer en dårlig lukt. Det ble brukt i flere tiår sammen med oksygenet for å sove pasienter under kirurgiske inngrep, men uønskede bivirkninger representert som "Cyclopropane Shock" begynte å bli observert.
Sammen med kostnadene for kostnader og høy brennbarhet gikk det gjennom en forkast og erstatningsprosess av andre tryggere bedøvelsesmidler.
Selv om det fortsatte å være en del av forbindelsene som ble brukt i induksjon av anestesi, er det i dag ikke en del av midlene som brukes i medisinske anvendelser.
Risiko
- Cyclopropane er en svært brennbar gass, som produserer giftige gasser når du kommer i kontakt med en flamme. I tillegg kan den reagere med oksidasjonsmidler som peroksider, peroksider, permanganater, nitrater og halogener, forårsaker branner og/eller eksplosjoner.
Kan tjene deg: klorogensyre- Sykling på høye nivåer kan forårsake hodepine, svimmelhet, kvalme, tap av koordinering, følelse av besvimelse og/eller falming.
- Det kan også generere uregelmessigheter i hjertefrekvens eller arytmi, pustevansker, koma og til og med død.
- Flytende cyclopropa kan forårsake hudfrysing på grunn av temperaturen betydelig lavere enn null.
- Å være en gass under miljøforhold, kan denne forbindelsen lett komme inn i kroppen gjennom luften, og reduserer også oksygennivået i luften.