Glykosidisk kobling Hva er, egenskaper, typer, nomenklatur
- 1309
- 381
- Magnus Sander Berntsen
De Glykosidiske koblinger De er de kovalente bindingene som oppstår mellom sukker (karbohydrater) og andre molekyler, som kan være andre monosakkarider eller andre molekyler av mangfoldig natur.
Disse koblingene muliggjør eksistensen av flere grunnleggende komponenter for livet, ikke bare i dannelsen av reservebrensel og strukturelle elementer, men også av essensielle informasjonstransportmolekyler for cellulær kommunikasjon.
Dannelsen av polysakkarider avhenger grunnleggende av etablering av glykosidbindinger mellom alkoholer eller frie hydroksylgrupper av individuelle monosakkaridenheter.
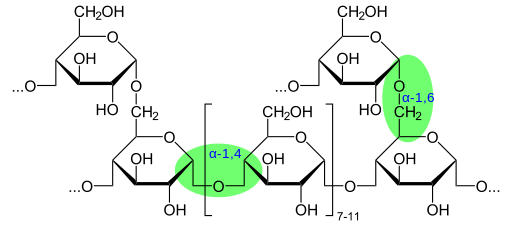 Glykosidbindingseksempel i glykogen (kilde: glykogen.SVG-Neurotkerivative-Work-Marek-M-Public-Domain via Wikimedia Commons)
Glykosidbindingseksempel i glykogen (kilde: glykogen.SVG-Neurotkerivative-Work-Marek-M-Public-Domain via Wikimedia Commons) Glykosidiske koblinger forekommer i flere cellesammenhenger, inkludert foreningen av den polare hodegruppen til noen sfingolipider, essensielle bestanddeler av cellemembranene til mange organismer, og dannelse av glykoproteiner og proteoglykaner.
Viktige polysakkarider som cellulose, kitin, agar, glykogen og stivelse ville ikke være mulig uten glukosidbindinger. På samme måte er proteinglykosylering, som forekommer i endoplasmatisk retikulum og i Golgi -komplekset, av største betydning for aktiviteten til mange proteiner.
Kjennetegn
Glykosidbindinger er mye mer varierte enn deres analoger i proteiner og nukleinsyrer, siden to sukkermolekyler i prinsippet kan bli med hverandre på mange måter, fordi de har flere grupper -OH som kan delta i dannelsen av lenken.
I tillegg gir isomerer av monosakkaridene, det vil si en av de to orienteringene som hydroksylgruppen kan ha i den sykliske strukturen med hensyn til anomere karbon, et ekstra nivå av mangfold.
Isomerer har forskjellige tre -dimensjonale strukturer, så vel som forskjellige biologiske aktiviteter. Cellulose og glykogen består av gjentatte enheter av D-glukose, men er forskjellige når det gjelder typen glukosidbinding (α1-4 for glykogen og β1-4 for cellulose), og derfor har de forskjellige egenskaper og funksjoner.
Akkurat som polypeptider har en polaritet med den ene enden og en annen C-, og polynukleotider har 5 'og 3' ender, har oligo-eller polysakkarider en polaritet definert ved å redusere ender og ikke redusere.
Den reduserende enden har et fritt anomerisk senter som ikke danner en glykosidisk kobling med et annet molekyl, så den beholder den kjemiske reaktiviteten til aldehyden.
Kan tjene deg: ekstern befruktningGlukosidbindingen er den mest fleksible regionen i en oligo-eller polysakkarid.
Glykosidbindingsdannelse
Glukosidbindingen kan bli med i to monosakkaridmolekyler gjennom den ene og hydroksylgruppen til den andre. Det vil si at hemiacetal -gruppen til ett sukker reagerer med alkoholgruppen til en annen for å danne en acetal.
Generelt skjer dannelsen av disse koblingene ved kondensasjonsreaksjoner, der et vannmolekyl frigjøres med hver kobling som dannes.
I noen reaksjoner forlater oksygen imidlertid ikke sukkermolekylet som vann, men som en del av difosfatgruppen til et difosfat uridindukleotid.
Reaksjonene som gir opphav til glukosidiske koblinger blir katalysert av en klasse enzymer kjent som glykosyltransferaser. De dannes mellom et kovalent modifisert sukker ved tilsetning av en fosfatgruppe eller et nukleotid (6-fosfatglukose, UDP-galaktose, for eksempel) som binder seg til vekstkjeden i voksende polymer.
Glykosidisk bindingshydrolyse
Glykosidbindinger kan lett hydrolysere i svakt sure miljøer, men de motstår ganske alkaliske miljøer.
Den enzymatiske hydrolysen av glukosidbindinger er mediert av enzymer kjent som glykosidaser. Mange pattedyr har ikke disse enzymene for nedbrytning.
Duminanter som kyr, for eksempel, har bakterier assosiert med tarmen som produserer enzymer som er i stand til å nedbryte cellulosen de spiser, noe som gjør at de er i stand til å dra nytte av energien som er bevart i plantevev.
Det glatte enzymet, produsert i øyets tårer og av noen bakterievirus, er i stand til å ødelegge bakterier takket være dens hydrolytiske aktivitet, som bryter den glukosidiske bindingen mellom n-acetylglukosamin og n-acetylmuraminsyren i celleveggen til den bakterie.
Mangfold
Oligosakkarider, polysakkarider eller glykaner er veldig forskjellige molekyler, og dette skyldes de flere måtene monosakkarider kan gå sammen ved å danne strukturer med høyere orden.
Dette mangfoldet starter fra det faktum, som nevnt ovenfor, at sukker har hydroksylgrupper som tillater forskjellige unionsregioner, og at bindingene kan oppstå mellom de to mulige stereoisomerer med hensyn til det anomere karbonet i sukker (α eller β).
Kan tjene deg: blastozoosGlykosidiske koblinger kan dannes mellom et sukker og eventuell hydroksylert forbindelse som alkoholer eller aminosyrer.
I tillegg kan et monosakkarid danne to glukosidbindinger, slik at det kan tjene som et grenpunkt, og introdusere en potensiell kompleksitet i strukturen til glykaner eller polysakkarider i celler.
Folkens
Når det.
O-glukosidiske koblinger
O-glykosidiske koblinger forekommer mellom monosakkarider, dannes ved reaksjonen mellom hydroksylgruppen til et sukkermolekyl og det anomere karbonet til en annen.
Disakkarider er fra de vanligste oligosakkarider. Polysakkarider har mer enn 20 enheter monosakkarider som er sammenliknet lineært og har noen ganger flere konsekvenser.
 O-Glucosidic Link Eksempel (Kilde: TPPIROJSI [Public Domain] via Wikimedia Commons)
O-Glucosidic Link Eksempel (Kilde: TPPIROJSI [Public Domain] via Wikimedia Commons) I disakkarider som maltose, laktose og sukrose, er den vanligste glukosidbindingen O-glykosidtypen. Disse koblingene kan oppstå mellom karbonatomer og -oh av isomere former α eller β.
Dannelsen av glukosidbindinger i oligo- og polysakkarider vil avhenge av den stereokjemiske naturen til sukkeret som er sammen med, så vel som antall karbonatomer. Generelt, for sukker med 6 karbonatomer, oppstår lineære bindinger mellom karbonatom 1 og 4 eller 1 og 6.
Det er to hovedtyper av o-Glykosider som, avhengig av nomenklaturen, er definert som α og β eller 1.2-Cis og 1.2-trans-glykosider.
Avfallet 1.2-Cis Glykosylerte, a-glykosider for D-glykose, D-galaktose, L-fucosa, D-Xilosa eller ß-glykosider for D-manosa, L-yarabinosa; så vel som 1.2-trans (ß-glykosider for D-glukose, D-galaktose og α-glykosider for D-MANY, etc.), er av stor betydning for mange naturlige komponenter.
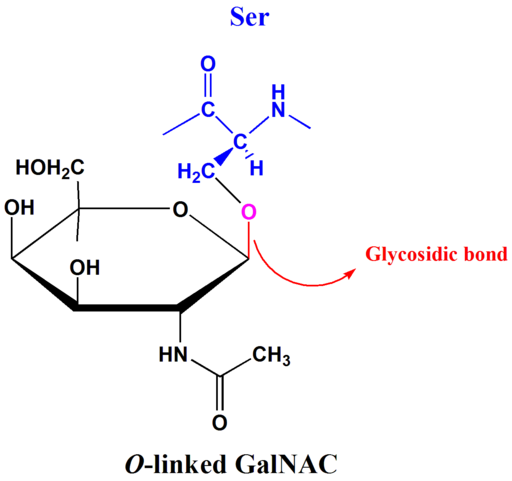
O-glykosylering
En av de vanligste post -translasjonelle modifikasjonene er glykosylering, som består i tilsetningen av en glukiddel til et voksende peptid eller protein. Muciner, sekresjonsproteiner, kan inneholde store mengder oligosakkaridkjeder koblet sammen med O-glukosidiske bindinger.
O -glykosyleringsprosessen skjer i golgi -komplekset til eukaryotene og består av foreningen av proteiner til glukidedelen gjennom en glukosidisk binding mellom den -OH -gruppen av en aminoacid rest av serin eller treonin og den anomere karbon av sukker.
Kan tjene deg: glukolipider: hva er, klassifisering, struktur, funksjonerDannelsen av disse bindingene mellom karbohydrater og hydroksylisin og hydroksilisin og den fenoliske gruppen av tyrosinavfall er også observert.
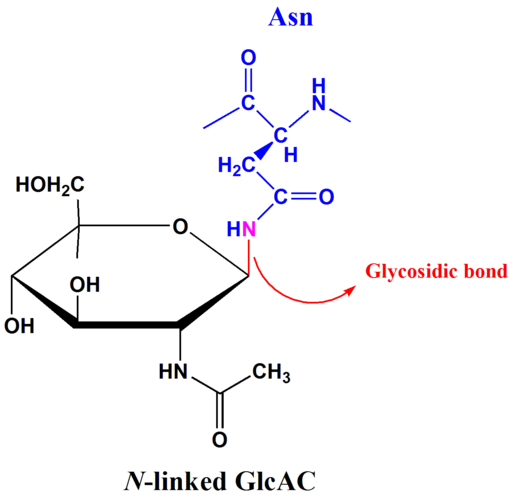
N-glukosidiske koblinger
N-glycycosidiske koblinger er de vanligste blant glykosylerte proteiner. N-glykosylering skjer hovedsakelig i endoplasmatisk retikulum av eukaryoter, med påfølgende modifikasjoner som kan oppstå i Golgi-komplekset.
 N-glukosidisk lenkeeksempel (Kilde: TPPIROJSI [Public Domain], via Wikimedia Commons)
N-glukosidisk lenkeeksempel (Kilde: TPPIROJSI [Public Domain], via Wikimedia Commons) N-glykosylering avhenger av tilstedeværelsen av ASN-XXX-serien/THR-konsensus-sekvensen. Glykosidbindingen oppstår mellom det midt i nitrogenet i sidekjeden til asparagin og anomere karbon av sukker som binder seg til peptidkjeden.
Dannelsen av disse bindingene under glykosylering avhenger av et enzym kjent som oligosacariltransferase, som overfører oligosakkaridene fra en fosfatdolicol til midt i nitrogen av asparaginavfall.
Andre typer glukosidiske lenker
S-glukosidiske koblinger
De forekommer også mellom proteiner og karbohydrater, er blitt observert mellom peptider med N-terminale cysteiner og oligosakkarider. Peptider med denne typen koblinger ble opprinnelig isolert fra protein i urinen og humane erytrocytter koblet til glukose oligosakkarider.
C-glukosidiske koblinger
De ble først observert som en post -translasjonell modifisering (glykosylering) i en tryptofanrester i RNASA 2 til stede i menneskelig urin og i erytrocyte 2. En hånd binder seg til karbon fra posisjon 2 av aminosyrekjernen ved hjelp av en c-glukosidbinding.
Nomenklatur
Begrepet glykosid brukes til å beskrive ethvert sukker hvis anomere gruppe erstattes av en gruppe -eller (o -glykosider), -sr (tioglycosides), -ser (selenoglucosides), -nr (n -glykosider eller glukosaminer) eller til og med -cr (n -glykosider eller glukosaminer) (C-glukosider).
De kan navngis på tre forskjellige måter:
(1) Bytte ut "-o" -terminalen med navnet på den tilsvarende sykliske formen for monosakkaridet med "-ido" og skrive før, som et annet ord, navnet på erstatningsgruppen R-gruppen.
(2) Bruke begrepet "glykosyloxi" som et prefiks av navnet på monosakkaridet.
(3) Bruke begrepet ENTEN-glykosil, N-glykosil, S-glykosil eller C-glykosil som et prefiks for navnet på den hydroksylerte forbindelsen.
Referanser
- Nelson, d. L., & Cox, m. M. (2009). Lehninger prinsipper for biokjemi. Omega -utgaver (5. utg.).
- Nomenklatur av karbohydrater (Anbefalinger 1996). (nitten nittiseks). Hentet fra www.QMUL.Ac.Storbritannia
- « Filialiopoda hva er, egenskaper, reproduksjon, mat
- Pacific Desert Hva er, egenskaper, klima, flora, fauna »

