Magnesiumfluoridstruktur, egenskaper, syntese, bruk
- 5108
- 978
- Dr. Andreas Hopland
Han Magnesiumfluorid Det er et fargeløs uorganisk salt hvis kjemiske formel er MGF₂. Det finnes i naturen som Sealíta -mineralet. Den har et veldig høyt fusjonspunkt og er veldig lite oppløselig i vann. Den er relativt inert, fordi for eksempel dens reaksjon på svovelsyre er langsom og ufullstendig og motstår hydrolyse med fluorhorinsyre (HF) til 750 ºC.
Det er en forbindelse som er lite påvirket av høy energidyring. I tillegg har den en lav brytningsindeks, høy korrosjonsmotstand, god termisk stabilitet, betydelig hardhet og utmerkede synlige lysoverføringsegenskaper, UV (Ultraviolet) og IR (infrarød).

Disse egenskapene har utmerket ytelse i det optiske feltet, og i tillegg gjør de det til et nyttig materiale som katalysatorstøtte, beleggelement, anti -reflekslinser og vinduer for infrarød overføring, blant andre applikasjoner.
[TOC]
Struktur
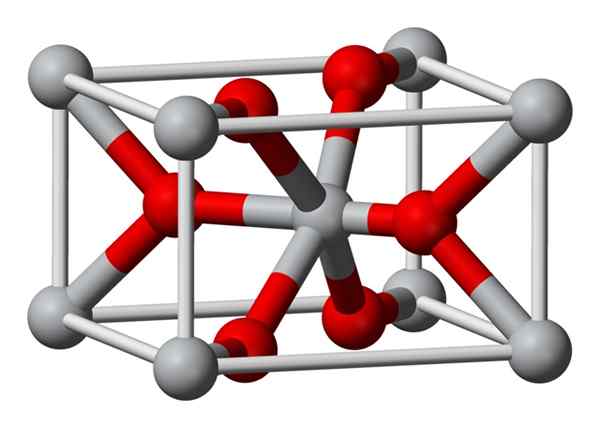
Den krystallinske strukturen av magnesiumfluorforberedt er kjemisk den samme typen som den av Sellaíta naturlige mineral. Krystalliserer i dipiramidalklassen i det tetragonale systemet.
Magnesiumioner (Mg2+) er lokalisert i en tetragonal-sentrert romsentrert, mens fluorioner (F-) finnes i samme plan for naboene Mg2+ og assosiert med disse, gruppert i par med hver. Avstanden mellom Mg2+ og F-ionene er 2,07 Å (angstroms) (2,07 × 10-10m).
Den krystallinske koordinasjonen er 6: 3. Dette betyr at hvert Mg2+ -ion er omgitt av 6 ioner f- og hvert ion f-, på sin side, er omgitt av 3 mg2+ 5-ioner.
Strukturen er veldig lik den for rutilo -mineralet, som er den naturlige formen for titandioksid (TiO2), som den har flere krystografiske egenskaper til felles.
Under dens oppnåelse utfeller ikke magnesiumfluorid i form av amorft faststoff, fordi Mg2+ og F-ioner ikke har en tendens til å danne polymerkomplekser i løsning.
Egenskaper
Det er interessant å understreke at magnesiumfluorid er et birrefringent materiale. Dette er en optisk egenskap som lar deg utfolde en stråle av hendelseslys i to separate stråler som sprer seg ved forskjellige bølger og bølgelengder.
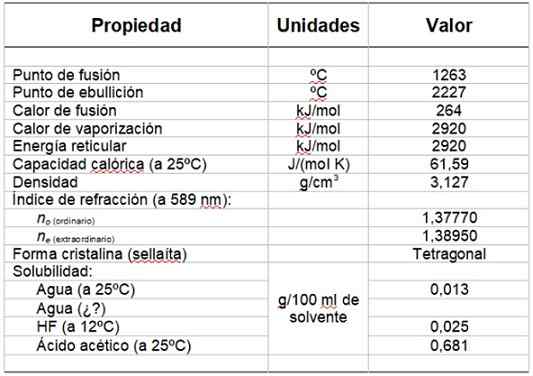
Kan tjene deg: hydroksylgruppeTabell 1 viser noen av dens egenskaper.
Tabell 1. Fysiske og kjemiske egenskaper ved magnesiumfluorid.
Syntese og preparat
Det kan utarbeides på flere måter, blant dem følgende kan nevnes:
1-fordi reaksjonen mellom magnesiumoksyd (MgO) eller magnesiumkarbonat (MgCO3) med fluorsyre (HF) 2:
MgO + 2 HF Mgf2 + H2O
Mgco3 + 2 hf mgf2 + co2 + h2o
2-for reaksjon mellom magnesiumkarbonat og ammoniumbifluoruro (NH4HF2), begge i fast tilstand, ved en temperatur mellom 150 og 400 ºC2:
150-400 ºC
MgCO3 + NH4HF2 Mgf2 + NH3 + CO2 + H2O
3-Calento En vandig løsning av magnesiumkarbonat og ammoniumfluorid (NH4F) i nærvær av ammoniumhydroksyd (NH4OH) ved 60 ºC 2:
60 ºC, NH4OH
MgCO3 + 3 NH4F NH4MGF3 + (NH4) 2CO3
Bunnfallet av ammonium og magnesiumfluorid (NH4MGF3) varmes deretter opp til 620 ºC i 4 timer for å oppnå magnesiumfluorid:
620 ºC
NH4MGF3 Mgf2 + NH3 + HF
4-som biprodukt av å skaffe beryllium (være) og uran (u). Fluor av det ønskede elementet med metallisk magnesium varmes opp i en Mgf2 2 -dekket smeltedigel:
Bef2 + mg være + mgf2
5-fold reagerer magnesiumklorid (Mgcl2) med ammoniumfluorid (NH4F) i vandig løsning ved romtemperatur 3:
25 ºC, H2O
Mgcl2 + 2 nh4f mgf2 + 2nh4cl
Siden MGF2 -forberedelsesmetoder er dyre, er det forsøk på å oppnå det mer økonomisk, blant dem metoden for å produsere den fra sjøvann.
Kan tjene deg: kalsiumhydrid (CAH2): egenskaper, reaktivitet og brukDette karakteriseres ved å tilsette nok fluorioner (f-) til sjøvann, som har rikelig konsentrasjon av magnesiumioner (Mg2+), og dermed favoriserer nedbøren av Mgf2.
Optiske magnesiumfluoridkrystaller oppnås ved varmt trykk fra høy kvalitet MGF2, oppnådd for eksempel ved NH4HF2 -metoden.
Det er mange teknikker for å fremstille magnesiumfluoridmaterialer, for eksempel en glassvekst, sintring (komprimering til mugg eller form) uten trykk, varmt og sintring presset med mikrobølgeovn.
applikasjoner
Optikk
MGF2 -krystaller er egnet for optiske anvendelser fordi de er gjennomsiktige fra UV -regionen til IR -gjennomsnittet 2,10 -regionen.
Som en inert film brukes til å endre lysoverføringsegenskapene til optiske og elektroniske materialer. En av de viktigste applikasjonene er i VUV -optikken for romutforskningsteknologi.
På grunn av dens birefringency -egenskap er dette materialet nyttig i polarisasjonsoptikken, i ECIMER -laservinduer og prismer (ultrafiolett lasertype brukt i okulær kirurgi).
Det skal bemerkes at magnesiumfluorene som brukes i fremstilling av optiske materialer av tynn film, må være fri for urenheter eller forbindelser som er oksydkilde, for eksempel vann (H2O), hydroksydioner (OH-), karbonationer (CO3 = ), Sulfationer (SO4 =), og lignende 12.
Katalyse eller akselerasjon av reaksjoner
MGF2 har blitt brukt med hell som en katalysatorstøtte for reaksjonen av kloreliminering og tilsetning av hydrogen i CFC (klorfluorokarboner), kjente kjølemidler og aerosoldrevne, og ansvarlig for skaden på atmosfæren ozonlaget.
De resulterende forbindelsene, HFC (hydrofluorokarboner) og HCFC (hydroklorofluorokarboner), presenterer ikke denne skadelige effekten for atmosfæren 5.
Det har også vært nyttig som støtte for katalysatorer for hydrodesulfrasjon (svovel eliminering) av organiske forbindelser.
Kan tjene deg: Kjemisk balanse: Forklaring, faktorer, typer, eksemplerAndre bruksområder
Materialene generert av grafitt, fluor og MGF2 fletter.
Eutctic dannet av NAF og MGF2 presenterer energilagringsegenskaper i latent varme, så det har blitt vurdert for bruk i solenergisystemer.
I området biokjemi brukes magnesiumfluorid sammen med andre metallfluorider for å hemme fosforyloverføringsreaksjoner i enzymer.
Nylig har MGF2 -nanopartikler blitt testet som medikamentell plasseringsvektorer i syke celler for kreftbehandling.
Referanser
- Buckley, h.OG. og Vernon, w.S. (1925) xciv. Krystallstrukturen til magnesiumfluorid. Philosophical Magazine Series 6, 49: 293, 945-951.
- Kirk-Ohmer (1994). Encyclopedia of Chemical Technology, bind 11, femte utgave, John Wiley & Sons. ISBN 0-471-52680-0 (V.elleve).
- Peng, Minhong; Cao, Weiping; og sang, Jinhong. (2015). Forberedelse av MGF2 gjennomsiktig keramikk ved varmpressende sintring. Journal of Wuhan University of Technology-Mater: Sci. Ed. Vol. 30 nei. 4.
- Непонов, и.С. (2011). Fluor magnesium. Kilde: eget arbeid.
- Wojciechowska, Maria; Zielinski, Michal; og Piettowski, Mariusz. (2003). MGF2 som en ikke-konfensjonell katalysatorstøtte. Journal of Fluorine Chemistry, 120 (2003) 1-11.
- Korth Kristalle GmbH. (2019). Fluor magnesium (Mgf2). Konsultert den 07/12/2019 i: Korth.av
- Sevonkaev, Igor og Matijevic, Egon. (2009). Dannelse av magnesiumfluoridpartikler av forskjellige morfologier. Langmuu 2009, 25 (18), 10534-10539.
- Непонов, и.С. (2013). Fluor magnesium. Kilde: eget arbeid.
- Tao Qin, Peng Zhang og Weiwei Qin. (2017). En ny metode for å syntetisere lavpris magnesiumfluorid kuler fra sjøvann. Ceramics International 43 (2017) 14481-14483.
- Ullmanns Encyclopedia of Industrial Chemistry (1996) Femte utgave. Volum A11. VCH Verlagsgellschaft MBH. New York. ISBN 0-89573-161-4.
- NASA (2013). Ingeniører som inspiserer Hubble -romteleskopets primære speil 8109563. Kilde: Mix.MSFC.gryte.Gov
- « Piktografisk skriving opprinnelse, egenskaper og eksempler
- Kommer og eksempler på kommersielle transaksjoner »

