Sinkfosfat (Zn3 (PO4) 2) Struktur, egenskaper, bruk

- 1133
- 207
- Markus Fredriksen
Han Sinkfosfat Det er en uorganisk forbindelse med kjemisk formel er Zn3(Po4)2, Men det er presentert i naturen i sin tetrahydratform, Zn3(Po4)2· 4H2Eller, i Hopeíta og Parahopeíta mineraler. Også et grunnleggende utvalg av det ligger i Tarbutita -mineralet, Zn2(Po4) (ÅH). Disse mineralene dannes ved oksidasjon av sfaleritten i rike fosfatvann.
All bruk som er kjent for denne forbindelsen er basert på Zn3(Po4)2· 4H2Eller fordi vannmolekylene gir den egenskapen til å være et godt fikseringsmiddel. Derfor mangler dens vannfrie form som sådan bruk av stor økonomisk etterspørsel.
 Sinkfosfatfragmenter. Kilde: ChemicalInterest [Public Domain]
Sinkfosfatfragmenter. Kilde: ChemicalInterest [Public Domain] Som det fremgår av det overlegne bildet, er sinkfosfat et hvitt fast stoff, til stede i støv eller kaket i små fragmenter. Den hvite fargen har benyttet seg av i formuleringen av kosmetiske produkter, så vel som ved fremstilling av tannsement og fosferte puzzoliske sement.
Sinkfosfat er et antikorrosivt middel som har blitt brukt i sinkmineralelektrodeponeringsprosesser (Hopeíta og fosfofilitt) på overflaten av stål.
[TOC]
Struktur
Zn -formelen3(Po4)2 Indikerer at Zn -ioner2+ og po43- komponere salt i et 3: 2 -forhold, som betyr at for hver tredje kationer Zn2+ Det er to anioner PO43-. Disse ionene samhandler med hverandre elektrostatisk, så de etablerer en sterk ionisk binding på grunn av størrelsen på belastningen. Begge ionene er allsidige.
Dermed Zn2+ og po43- De ender i verdensrommet til de definerer en ordnet og repeterende struktur: en sinkfosfatkrystall. Denne krystallen vedtar en monoklinisk struktur, α-Zn3(Po4)2. Dette er tilsynelatende i stand til å lide faseoverganger til andre polymorfe former: β-Zn3(Po4)2 og y-zn3(Po4)2, All temperaturavhengig.
Kan tjene deg: Termodynamiske prosesserDe tre polymorfene er isoestrukturelle, og skiller bare i den romlige orienteringen av deres ioner; det vil si at de har forskjellige romgrupper.
På den annen side har sinkfosfat en tendens til å bli presentert mest som et hydrat: Zn3(Po4)2· 4H2Eller, hvis krystallinske struktur også er monoklinisk. Denne gangen er ionene ledsaget av fire vannmolekyler, som samhandler med dem gjennom dipol-ion-krefter og hydrogenbroer.
Sinkfosfategenskaper
 Sinkfosfat. Ondřej Mangl [Public Domain]
Sinkfosfat. Ondřej Mangl [Public Domain] Fysisk utseende
Støvete hvitt faststoff.
Molmasse
454.11 g/mol
Smeltepunkt
900 ºC
Kokepunkt
Ingen informasjon. Dette kan skyldes en mulig termisk nedbrytning, eller utilgjengeligheten av trykkforholdene for å koke saltvæsken.
Tetthet
3.998 g/cm3
Brytningsindeks
1.595.
Vannløselighet
Uoppløselig. Dette skyldes delvis den ioniske koblingen mellom Zn -ionene2+ og po43-, som øker krystallinsk retikulær energi mot saltoppløsning.
Flash Point
Sinkfosfat er et ikke -brennbart stoff.
applikasjoner
Sinkfosfatbruk tilsvarer de av dets tetrahydrat, Zn3(Po4)2· 4H2Eller siden det er dens dominerende form og til og med oppnås i Hopeíta og Parahopeíta mineraler. Derfor er det ukjent om dens vannfrie form, Zn3(Po4)2, Har en spesifikk bruk.
Kosmetikk
Sinkfosfat har blitt brukt som hvitt pigment, og erstattet sinkoksider og titan i kosmetiske og skjønnhetsprodukter. Materialet, mykt å berøre, av små og runde partikler for å dekke overflaten av huden uten å snike seg gjennom porene, syntetiseres fra en blanding av fosforsyre, H3Po4, og sinknitrat, Zn (nei3)2.
Kan tjene deg: karbokasjon: dannelse, egenskaper, typer, stabilitetDermed forbereder hvite sinkfosfatpigmenter varierende Zn/P -proporsjonene. For dette, ved å blande reagensene, tilsettes variable mengder h3Po4 og Zn (nei3)2, Inntil produktet med de beste kosmetiske egenskapene.
I en studie utført av University of the Kyoto Prefecture, fant de ut at pigmentene tilberedt med et Zn/P -forhold lik 2/1, 1/1 og 3/2 viste de beste refleksjonene; Derfor var ansiktene til de som brukte kosmetisk sammenlignet med lysstyrken til andre formuleringer mer opplyst.
Antibakterielt middel
Sinkfosfat -nanopartikler er innenfor arsenal som er ment å bekjempe mikrober og dermed være et alternativ til bruk av antibiotika. På denne måten reduseres den konstante og progressive resistens som er utviklet av bakterier mot antibiotika, mens den søker å redusere utgiftene i behandlingen av smittsomme sykdommer.
Disse nanopartiklene har vist stor antibakteriell aktivitet mot koliforme bakterier, en studie som ble sjekket hos rotter uten å forårsake oksidativt stress.
Tannsement
Sinkfosfat brukes til å fremstille fosfatsement, som brukes i restaureringene av mange materialer; Blant dem, våre egne tenner, oppfører seg som en ganske populær tannsement innen tannbehandling i lang tid. Denne fosfatsementet tjener til å fikse og slå sammen flere faste stoffer samtidig.
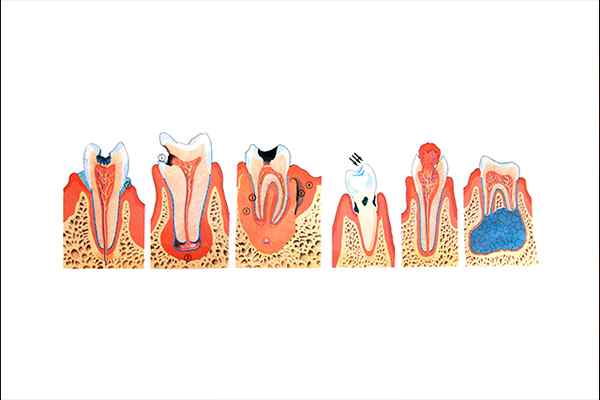 Sinkfosfat brukes til fremstilling av tannsement.
Sinkfosfat brukes til fremstilling av tannsement. Det er fremstilt ved å løse sinkoksider og magnesium i fosforsyre, så Zn -ioner er til stede2+ og mg2+, danner komplekse strukturer. Denne tannsement er avgjørende for den endelige sementeringen av tennene. På grunn av surheten, for pasienter som er for følsomme for den, brukes imidlertid i stedet for polykarboksylatsement.
Kan tjene deg: umettede hydrokarbonerAntikorrosivt belegg
I likhet med hvordan med sementen kan stålens overflate også være fosfatisk.
For å gjøre dette blir stålbitene introdusert i et alkalisert fosforsyrebad, og etter å ha levert en elektrisk strøm, dannes en beskyttende film sammensatt av Hopeíta på overflaten (Zn3(Po4)2· 4H2O) og fosfofilita (Zn2Tro (Po4)2· 4H2O), å være den sistnevnte forbindelsen de mest motstandsdyktige mot sterkt alkaliske medier.
De kjemiske reaksjonene som er involvert er følgende:
3zn2+ + 2H2Po4- + 4H2O → Zn3(Po4)2· 4H2O + 4H+
2zn2+ + Tro2+ + 2H2Po4- + 4H2O → Zn2Tro (Po4)2· 4H2O + 4H+
Problemet med disse beleggene ligger i graden av porøsitet, fordi det etterlater flanker utsatt der stål kan lide korrosjoner.
På den annen side har puzzolanisk sement blitt brukt som inneholder sinkfosfat for utvikling av betong som er mer motstandsdyktig mot korrosjon.
Generelt har den antikorrosive egenskapen til sinkfosfat blitt tildelt til å tjene som belegg for veggene før malingslagene påføres, slik at de er lengste og flere farger viser bedre farger.
Referanser
- Shiver & Atkins. (2008). Uorganisk kjemi. (Fjerde utgave). Mc Graw Hill.
- Wikipedia. (2020). Sinkfosfat. Hentet fra: i.Wikipedia.org
- Elsevier f.V. (2020). Sinkfosfat. Scientedirect. Hentet fra: Scientedirect.com
- Nasjonalt senter for bioteknologiinformasjon. (2020). Sinkfosfat. PubChem -database., CID = 24519. Gjenopprettet fra: Pubchem.NCBI.NLM.NIH.Gov
- Aref m. al-Swaidani. (2018). Inhiberingseffekt av naturlige pozzolan- og sinkfosfatbad på forsterkende stålkorrosjon. gjør jeg.org/10.1155/2018/9078253
- Onoda, h., & Haruki, m. (2014). Blandingsforholdet mellom sinknitrat og fosforsyre for fremstilling av sinkfasfathvite pigmenter. Cerâmica, 60 (355), 392-396. Dx.gjør jeg.org/10.1590/S0366-69132014000300010
- Horky, p., Skalickova, s., Urbankova, l. et al. (2019). Sinkfosfatbaserte nanapartikler som et nytt antibakterielt agenc: In vivue studie på rotter etter kostholdseksponering. J Animal Sci Biotechnol 10, 17. gjør jeg.org/10.1186/S40104-019-0319-8

