Fucosa -egenskaper, struktur, funksjoner
- 3943
- 50
- Prof. Joakim Johansen
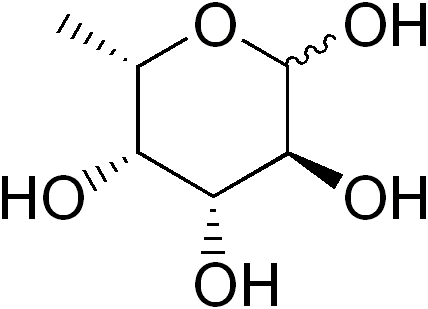
De Fucosa (Forkortet FUC), eller 6-L-DEXI-galaktose, det er en delvis deoxigenado (deoxiazúcar) monosakkarid av seks karbonatomer hvis empiriske formel er c er c er6H12ENTEN5. Som andre monosakkarider er det et polyhydroksylert sukker.
Når en hydroksylgruppe erstattes av et atom av hydrogen, blir en deoxiazúcar avledet. Selv om teoretisk sett kan denne erstatningen påvirke enhver hydroksylgruppe av et hvilket som helst monosakkarid, i naturen er det lite utvalg av dexiazúcús.
 Kilde: Edgar181 [Public Domain]
Kilde: Edgar181 [Public Domain] Noen deoxiazúces er: 1) Deoxyribosa (2-disoxxi-d-libose), avledet fra D-libosen, som er en del av DNA; 2) Ramnosa (6-D-Dexxi-Marso), avledet fra D-Manosa; 3) Fucosa, avledet fra L-galaktose. Sistnevnte er hyppigere enn D-Fucosa, avledet fra D-galaktose.
[TOC]
Egenskaper og struktur
Fucosa er også kjent med 6-Disoxxi-scalact-hexose, fucopiranous, galactomethyl og rodeous navn.
Selv om det normalt danner polysakkarider og glykoproteiner, er isolert som monosakkarid søtere enn galaktose. Dette er fordi erstatningen av en hydroksylgruppe med et hydrogenatom øker den hydrofobe karakteren og derfor molekylets søthet.
Fucosa hydroksylgrupper kan oppleve de samme reaksjonene som andre sukkerarter, og produserer et bredt utvalg av acetaler, glykosider, etere og estere.
Et fucosilert biomolekyl er en som de ved virkningen av en fucosyltransferase har sluttet seg til, av glykosidbindinger, fucosa -molekyler. Når hydrolysen av glykosidbindinger oppstår ved virkningen av en fucosidase, og dermed skiller fucosa, sies det at biomolekylet har blitt defukosylert.
Når glukanosfukosyl, genereres mer komplekse glukaner som kalles fucanos, som kanskje ikke er en del av glykoproteiner. Sulfatfucaner er definert som de polysakkarider som inneholder sulfatrester av L-fucosa. De er typiske for brune alger. Som eksempler kan de utnevnes Ascophilano, Sargasano og Pelvetano.
En av de beste studerte fucanos er fucoidano, oppnådd fra de brune algene Fucus vesiculosus, som har blitt markedsført (Sigma-Aldrich Chemical Company) i flere tiår.
Kan tjene deg: hva er erristeneo?Distribusjon i naturen
D-fucose er til stede i antibiotikastoffer produsert av mikrober, og i vegetabilske glykosider, for eksempel konvolering, charrtreusine, ledenosida og queirotoxin.
L-fucosen er en bestanddel av polysakkaridene til algene, laken på plommen, linene i lin, soya og raps, Tragacanto-gummien, celleveggene i poteten, knollene til kassavaen, kiwi-frukten, Cortex av CEIBA og Mucigel of the Corn Caliptra, så vel som andre planter.
L-Fucosa er også til stede i kråkevinker og i geléen som beskytter froskegg.
Hos pattedyr danner fucaner med L-fucosa ligandene som virker i den utvalgte medierte leukocytt-endotelial vedheft, og deltar i mange ontogenetiske hendelser.
L-Fucosa bugner av fucoSphingolipider i mage-tarmpitel og benmarg, og vises i små proporsjoner i brusk og keratinøse strukturer.
Hos mennesker er fucanos med L-fucosa en del av spyttglykoproteiner og magesaft. De er også en del av antigenene som definerer ABO -blodgruppene. De er til stede i flere oligosakkarider av morsmelk.
Fucosa metabolisme
Fucosyltransferaser bruker BNP-fucose, en fucosa-form aktivert av nukleotider, som en fucosa-donor i konstruksjonen av fucosylerte oligosakkarider.
BNP-fucosa er avledet fra BNP-manosa for suksessiv virkning av to enzymer: BNP-Manasea 4.6-dehydratasa og BNP-4-ZO-6-Desoximanosa 3.5-Epimerasa-4-reduktase.
UITLISERING EN NADP+COFACTOR, det første enzymet katalyserer dehydrering av BNP-Many. Reduksjonen av posisjon 6 og oksidasjon av posisjon 4 produserer BNP-6-desoxi-4-keto-koaming (under reaksjonen overføres hybriden fra posisjon 4 til 6 i sukkeret).
Det andre enzymet, som er NADPH-avhengig, katalyserer epimeriseringen av posisjoner 3 og 5, og nettverket av gruppe 4-ZO, av BNP-6-Desoxi-4-Ecto-Mamosa.
Bakterier kan vokse ved bruk av fucosa som en enkelt kilde til karbon og energi gjennom en fucosa -inducerbar opeone som koder for kataboliske enzymer for dette sukkeret.
Kan tjene deg: karboksylsyreDen forrige prosessen innebærer: 1) gratis fucosa -inngang gjennom celleveggen med formidling av en permease; 2) fucosa -isomerisering (en aldosa) for å danne en fucoulous (en Zea); 3) fosforylering av det fucoulous for å danne fucoulous-1-fosfat; 4) En aldolase-reaksjon for å danne laktaldehyd og dihydroksyacetonfosfat fra Fuculous-1-fosfat.
Funksjoner
Kreftpapir
Blant symptomene på mange typer kreftfremkallende tumor er tilstedeværelsen av glukan -koblede proteiner som skilles ut ved å ha en endret oligosakkaridsammensetning. Tilstedeværelsen av disse unormale glukanene, blant dem Fucanos skiller seg ut, er knyttet til det malignitet og metastatiske potensialet til disse svulstene.
I brystkreft inkluderer tumorceller fucosa i glykoproteiner og glykolipider. Fucosa bidrar til progresjon av denne kreften, og favoriserer aktivering av kreftstamceller, hematogen metastase og invasjonen av svulster gjennom ekstracellulære matriser.
I lungekarsinom og hepatokarsinogenese er det forsterkede uttrykket av fucosa knyttet til høyt metastatisk potensial og med lav sannsynlighet for overlevelse.
Som motpart er noen sulfaterte fucanos lovende stoffer i behandlingen av kreft, som bestemt.
Papir ved andre sykdommer
Det forsterkede uttrykket av fucanos i serumimmunoglobuliner har vært relatert til ungdom og voksen revmatoid artritt.
Mangelen i leukocyttadhesjon II er en sjelden medfødt sykdom på grunn av mutasjoner som endrer aktiviteten til en FDP-fucosetransportør lokalisert i Golgi-apparatet.
Pasienter lider av mental og psykomotorisk forsinkelse, og lider tilbakevendende bakterieinfeksjoner. Denne sykdommen reagerer gunstig på orale fucosa -doser.
Biomedisinsk potensial
Sulfatfucanoer oppnådd fra brune alger er viktige reservoarer av forbindelser med terapeutisk potensial.
Det kan tjene deg: ititrium: struktur, egenskaper, bruk, innhentingDe har anti -inflammatoriske og antioksidantegenskaper, som hemmer lymfocyttmigrasjon på infeksjonssteder og favoriserer frigjøring av cytokiner. Øk immunresponsen ved å aktivere lymfocytter og makrofager.
De har antikoagulantegenskaper. Det er bevist hos menneskelige pasienter som oralt hemmer blodplateaggregering.
De har antibiotika og antiparasittisk potensial og hemmer veksten av magen av magen Helicobacter pylori. Drep parasitter Plasmodium spp. (Malaria årsaksmiddel) og Leishmania Donovani (Årsaksmiddel for amerikansk visceotropisk leishmaniasis).
Til slutt har de kraftige antivirale egenskaper, og hemmer inntreden i cellen til flere virus av stor betydning for menneskers helse, inkludert Arenavirus, Cytomegalovirus, Hantavirus, Hepadnavirus, HIV, herpes simplex virus og influensavirus.
Referanser
- Becker, d. J., Lowe, J. B. 2003. Fucose: Biosyntese og biologisk funksjon hos pattedyr. Glycobiology, 13, 41r-53r.
- Deniaud-Bouët, e., Hardouin, k., Potin, s., Kloareg, f., Hervé, c. 2017. En gjennomgang om brune algecellevegger og fukoseholdige sulfaterte polysakkarider: celleveggskontekst, biomedisinske egenskaper og viktige forskningsutfordringer.Karbohydratpolymerer, http: // dx.gjør jeg.org/10.1016/j.Karbol.2017.07.082.
- Blomster h. M. 1981. Kjemi og biokjemi av D-og L-fucose. Fremskritt innen karbohydratkjemi og biokjemi, 39, 279-345.
- Listinsky, J. J., Siegal, g. P., Listinsky, ca. M. 2011. Den nye viktigheten av α-L-fucose i menneskelig brystkreft: En gjennomgang. ER. J. OVERSIKT. Storfekjøtt., 3, 292-322.
- Murray, r. K., et al. 2003. Harpers illustrerte biokjemi. McGraw-Hill, New York.
- Pereira, l. 2018. Terapeutisk og ernæringsmessig bruk av alger. CRC Press, Boca Raton.
- Staudacher, e., Altmann, f., Wilson, i. B. H., März, l. 1999. Fucose i N-glykaner: Fra plante til mann. Biochimica et Biophysica Acta, 1473, 216-236.
- Tanner, w., Loewus, f. TIL. 1981. Plante karbohydrater ii. Ekstracellulære karbohydrater. Springer, New York.
- Vanhooren, p. T., Vandamme, e. J. 1999. L-fucose: Forekomst, fysiologisk rolle, kjemisk, enzymatisk og mikrobiell syntese. Journal of Chemical Technology and Biotechnology, 74, 479-497.
- « Antarktisk polar sirkelplassering, egenskaper, flora og fauna
- Kjemosyntesefaser, organismer, forskjeller med fotosyntese »

