Glyseraldehydstruktur, egenskaper, funksjoner
- 1555
- 335
- Marius Aasen
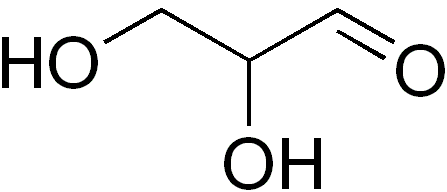
Han glyseraldehyd Det er det eneste tre -karbon -monosakkaridet, som på sin side er den eneste triosaen. Det er også en aldotriosa fordi den har en aldehydgruppe. Ordet glyseraldehyd kommer fra glyserin og aldehyd -kombinasjon. Dette er fordi glyseraldehyd ligner glyserin, men Carbon One (C-1) er en aldehyd.
Den kjemiske syntesen av glyseraldehyd utføres ved forskjellige metoder, for eksempel ved bruk av enzymer. Glyceraldehyd er et ganske reaktivt molekyl, og kan danne skandaløst mellom proteiner.
 Kilde: DRTW på Dutch Wikedia [CC BY-SA 3.0 (http: // creativecommons.Org/lisenser/by-SA/3.0/]]
Kilde: DRTW på Dutch Wikedia [CC BY-SA 3.0 (http: // creativecommons.Org/lisenser/by-SA/3.0/]] [TOC]
Struktur
Glyseraldehyden har et asymmetrisk eller chiral sentrum (karbonatom 2, C-2). Det danner to enantiomerer d (dextrogyr) og L (Levógiro), som roterer planet med polarisert lys i motsatte retninger: D-glyseraldehydet vender det til høyre og L-glyseraldehyd til venstre.
Den spesifikke optiske rotasjonen av D-glyceraldehyd, ved 25 ºC, er +8,7º, og den spesifikke optiske rotasjonen av D-glyceraldehyd, ved 25 ° C, er -8,7º. D-glyseraldehyd finnes ofte i naturen, hovedsakelig som glyseraldehyd 3-fosfat.
L-glyseraldehydkonfigurasjon brukes hvordan standardreferanse for karbohydrater. I biologiske molekyler florerer D-sukker. Karbonatom 3 (C-3) av glyseraldehyd er en hydroksymetylengruppe (-CH2ÅH).
Kjennetegn
Glyseraldehydkrystaller er fargeløse og har en søt smak. Den empiriske formelen til dette sukkeret er C3H6ENTEN3 og molekylvekten er 90 g/mol.
I vandig løsning er DL-glyseraldehyd hovedsakelig til stede som aldehydrol, som er en hydrert form for aldehyd. Krystallinsk DL-glikaldehido er svak.
Analysen av glyseraldehydkrystaller med røntgenstråler har vist at den har 1,4-dioksanringer med alle substituenter i ekvatorialorientering.
I vandig oppløsning opplever glyseraldehyd selvoksidasjon genererende frie radikaler. Dette er assosiert med raskt oksygenforbruk.
Det kan tjene deg: protokooperasjonOksygenforbrukshastigheten avtar sakte i nærvær av superoksyddysmutase. Dette antyder at det er superoksyddannelse under glyseraldehyd autooxidation. Den begrensende passasjen av glyseraldehyd autoxid
Syntesen av D-glyseraldehyd blir katalysert av primære og sekundære aminosyrer, og blir foretrukket til lave pH-verdier (fra 3 til 4).
Funksjoner
I kryssbinding mellom proteiner
Protein-protein-interaksjon er en molekylær mekanisme for flere komplekse biologiske prosesser. Disse interaksjonene kan være forbigående, og er interaksjonen mellom protein fra en metabolsk vei eller signaloversettelse.
Kjemisk tverrbinding utgjør en direkte metode for å identifisere forbigående og stabile protein-protein-interaksjoner.
Teknikken for kryssbinding mellom protein består av dannelsen av kovalente bindinger, for hvilke midler som har bifuncionale reaktive grupper som reagerer med aminogrupper og aminosyreavfallsgrupper av proteiner brukes.
Spesielt reagerer midler med primære aminggrupper (som epsilon-amino av avfallet av lisinene) og danner krysser både inne i en underenhet av proteiner og mellom proteinunderenheter.
Det er et bredt utvalg av kommersielt tilgjengelige agenter. Selv om glyseraldehyd er et kryss -koblingsmiddel, er det andre mer populære agenter, for eksempel glutaraldehyd. Dette er fordi gluteraldehyd opprettholder den strukturelle stivheten til proteinet, som er et viktig krav i mange studier.
Andre populære agenter er homobifunksjonelle imiderere, som varierer i lengden på avstandsarmen blant sine reaktive grupper. Noen eksempler på imidoestere er Dimethyl Apimidato (DMA), Dimethyl Suberimidate (DMS) og Dimethyl Pimilimidato (DMP).
Kan tjene deg: homopolysakkarider: egenskaper, struktur, funksjoner, eksemplerI kryssbinding mellom gelatinmikrosfærer
Gelatin -mikrosfærer har potensial til å tjene til kontrollert medikamentfrigjøring. Dette er fordi disse mikrosfærene ikke er giftige og at produktene deres lett skilles ut. Imidlertid er gelatin en løselig polymer, så den må modifiseres kjemisk for å tjene som et medikamentfraktsystem.
D, L-glyceraldehyd kan betraktes som et ikke-giftig tverrbindingsmiddel (den dødelige dosen, DL50 I.p. Hos rotter er det 2000 mg/kg). I tillegg, i menneskekroppen, fosforyleres D-glyseraldehydet av triosa-kinasen. På denne måten dannes 3-fosfatglyseraldehyd som kommer inn i glykolyse.
Behandlingen av gelatinmikrosfærer med D, L-glyceraldehyd i 24 timer produserer mikrosfærer med et antall reduserte frie lysinaminosyrer. Derfor er mikrosfærens kapasitet til å forlenge for eksempel effekten av klodinin hydroklurid, som er antihypertensiv.
Mikrosfærene ble administrert ved subkutan injeksjon til hånlige albinas og rotter. Etter injeksjonen avtok systolisk blodtrykk i to timer, og gjenopprettet deretter basalverdien. Injeksjonsstedets stoffer ble analysert og mikrofeads ble ikke funnet, selv om betennelse ble observert.
I prebiotiske reaksjoner
Under prebiotiske forhold - slik som de som skal ha det primitive landet - kunne formaldehydet ha tjent for syntese av glyseraldehyd, en kjemisk mellomledd involvert i de kjemiske prosessene som kunne ha sin opprinnelse liv.
Den forrige hypotesen er basert på det faktum at både glykolyse og fotosyntese har glyseraldehyd 3-fosfat som metabolsk mellomledd.
Det er foreslått en kjemisk modell som forklarer biosyntesen av glyseraldehyd fra formaldehyd gjennom en syklisk bane. Syntesen av glyseraldehyd finner sted ved tilsetning av formaldehyd til en triosa (glyceraldehyd ↔ dihydroxyaceton) for å produsere en tetrosa (↔ aldotrosa ↔ ↔ ↔ ↔ ↔ ↔ ↔ ↔ ↔ ↔ ↔ ↔ ↔ ↔ ↔ ↔ ↔ ↔ ↔ ↔ ↔ ↔ ↔ ↔ ↔ ↔ ↔ ↔ ↔ ↔ ↔ ↔ ↔ ↔ ↔ ↔ ↔ ↔ ↔ ↔ ↔ ↔ ↔ ↔ ↔ ↔.
Kan tjene deg: erytrous: egenskaper, struktur, funksjonerTilsetningen av formaldehyd til glykaldehyden fullfører syklusen. Syntesen av to triosa -molekyler fra seks formaldehydmolekyler oppstår.
Generelt antas den prebiotiske syntese av sukkerarter at reaksjonen av formosa er involvert, der formaldehydet i nærvær av en liten mengde glykaldehyd omdannes til sukker ved aldoliske kondenseringsreaksjoner.
Det er blitt foreslått at prebiotisk sukkeroksidasjon (glykaldehyd, triosas, tetrosas) produserte polyhydroxyacids som fungerer som selv -tilalitiske stoffer.
Konvertering av glyseraldehyd til melkesyre og glycerinsyre, oksyd avhengig av jernhydroksyd, peker på oligoésterene til disse hydroksyacidene fant sted på overflaten av dette materialet.
Referanser
- Breslow, r., Ramalingam, v., Appaeee, ca. 2013. Katalyse av glyseraldehydsyntese av primære eller sekundære aminosyrer under prebiotiske forhold en funksjon av pH. Life Evolution Biosphera Origin. Doi 10.1007/S11084-013-9347-0.
- Carey, f. TIL., Giuliano, r. M. 2016. Organisk kjemi. McGraw-Hill, New York.
- Robyt, J.F. 1998. Essentials of Carbohydrate Chemistry. Springer, New York.
- Thornalley, p., Wolff, s., Crabbe, J., Stern, a. 1984. Autoksidasjonen av glyseraldehyd og andre enkle monosakkarider under fysiologisk katalysert av bufferinnlegg. Biochimica et Biophysica Acta, 797, 276-287.
- Vandelli, m.TIL., Rivas, f., Krig, s., Forni, f., Arletti, r. 2001. Mikrosfærer gelatin tverrbundet med D, L-glyceraldehyd som et potensielt Drarug-leveringssystem: Forberedelse, karakterisering, in vitro og in vivo-studier. International Journal of Pharmaceutics, 215, 175-184.
- Weber, a.L. 1987. Trose -modellen: Glyceraldehyd som en kilde til energi og monomerer for prebiotiske kondensasjonsreaksjoner. Livets opprinnelse, 17, 107-19.

