PH -indikatorer

- 2924
- 575
- Daniel Skuterud
Hva er pH -indikatorene?
De pH -indikatorer De er stoffer som tjener til å bestemme mengden pH som finnes i et spesifikt medium. Når du snakker om pH -konseptet, representerer dette konsentrasjonen av hydroniumioner (h3ENTEN+) som er til stede i en vandig løsning.
På samme måte måles det i negativ logaritmisk skala mellom 0 og 14, hvor løsninger med pH lavere enn 7 anses som sure, de av pH større enn 7 er basiske og de av pH -pH -er som er ansett som nøytrale løsninger. Denne parameteren er uttrykt som følger med Henderson-Hasselbalch-ligningen: pH = PKA + log10 ([TIL-]/[Ha]).
I det forrige uttrykket representerer PKA den negative logaritmen til syredissosiasjonskonstanten og molare konsentrasjoner [A-] og [ha] er henholdsvis de av svak syre og dens konjugatbase. Å kjenne pH lar deg studere kvaliteten på vann og mat, og å kunne opprettholde repeterbarheten til et forseggjort kjemikalie.
Typer indikatorer
Det er tre hovedtyper av pH -indikatorer:
- Syre-base væskeindikatorer, som fungerer i henhold til et visst pH-område.
- Papirene, stripene og andre indikatormaterialer som endrer farge når det legges til prøve eller brus på overflaten.
- Digitale pH-metters, som måler den potensielle elektriske forskjellen mellom to elektroder.
Flytende indikatorer
 Flytende indikatorer
Flytende indikatorer Væskeindikatorer er svake syrer eller organiske baser som har variantfarger i henhold til deres syre eller grunnleggende form. Disse fungerer innenfor begrensede områder, varierende farge når dette er nådd, og slutter å variere fargen når det maksimale nivået på området er nådd.
Kan tjene deg: diklormetan: struktur, egenskaper, bruksområder, toksisitetFor å fungere, må de bare brukes i løsninger der en fargeendring kan observeres (helst fargeløs).
Det er et stort antall flytende indikatorer i forskjellige farger og pH -områder, inkludert Cresol Red (rød gul i et område fra 0,2 til 1,8), det røde metyl (rød til gul i et område fra 4, 2 til 6,2), bromocresol grønn (rosa til blå/grønn fra 4.2 til 5.2), og fenolftalein (fargeløs til rosa i et område fra 8.0 til 10.0).
Disse indikatorene er populære for grader i analytisk kjemi, selv om et visst treningsnivå må være måttet utføre denne praksisen på en presis måte.
Indikatorer eller strips papirer
 Forsker som bruker en pH -indikatorstripe
Forsker som bruker en pH -indikatorstripe Det er flere typer papirer som brukes til å måle pH, men det mest kjente er det så -kallede lakmuspapiret, som er laget med et pulver som kommer fra lav.
Shortasol -papir tjener til å vite om en flytende eller gassoppløsning er sur eller grunnleggende (uten å vite hva dens eksakte pH eller et estimat vil være), og kommer i to presentasjoner: blå og rød.
Blå skinnende papirforandringer til rødt under sure forhold, og rød spirende papirforandringer til blått under grunnleggende eller alkaliske forhold, og kunne resirkulere for å utføre testen på en omvendt måte når papiret allerede har endret fargen.
De kjente begrensningene av papirlignende den indikatorer.
Ph -Metros
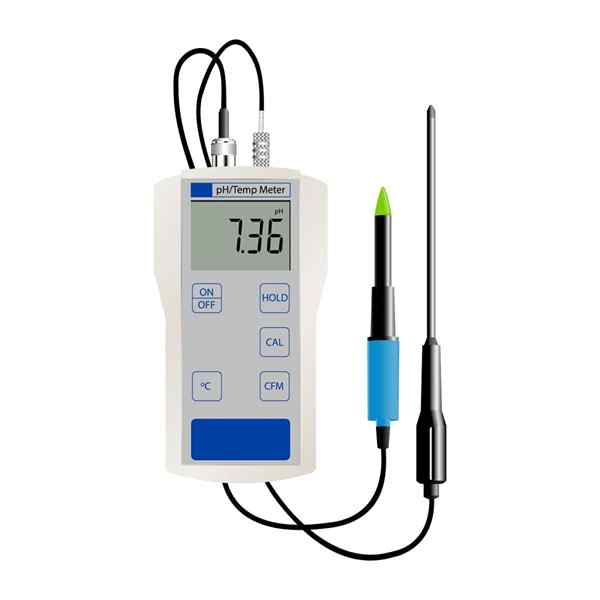 Digital pH -måler
Digital pH -måler PH-metoder er født fra behovet til laboratorieanalytikere for å oppnå eksakte verdier av denne parameteren, noe som ikke var mulig med papirindikatorer eller flytende indikatorer.
Kan tjene deg: kation: trening, forskjeller med anion og eksemplerDe er basert på måling av den elektriske potensielle differensialen mellom elektrode -pH og referanseelektroden.
Betjeningen av disse pH -metrene blir forklart mer dybde i den følgende seksjonen, men generelt anses disse indikatorene som den mest presise par excellence, og gir et presist antall (til nøyaktigheten på 0,01 enheter av pH) i parameteren og teller med en følsomhet og hastighet større enn de to andre metodene.
I tillegg kan andre egenskaper, for eksempel oppløste faste stoffer, elektrisk ledningsevne og oppløsningstemperatur også måle.
Den eneste ulempen med denne typen pH -målere er at de er delikat utstyr, og i tillegg til en innledende kalibrering som må utføre en instrumentalist eller en kjenner av utstyret, vil de også måtte rengjøres regelmessig for å forhindre at elektrodene lider akkumulering av materiale i disse.
Hvordan fungerer pH -indikatorer?
Flytende indikatorer
Væskeindikatorer endrer farge ved protonasjon eller tull i sin struktur (avhengig av den grunnleggende eller sure naturen til indikatoren), som er basert på reaksjonens balanse, som følger: Hin + H2Eller ↔ h3ENTEN+ + I-
Det vil si at når indikatoren er lagt til løsningen, hvis balansen i dette mediet begynner å ha en tendens til motsatt retning ved å øke eller redusere i hydroniumionet (igjen, avhengig av indikatorens natur), vil dette endre farge til Endelig hold deg i en ny ufravikelig farge.
Indikatorer
Indikatorene, nærmere bestemt lakmuspapiret, må komme i kontakt med løsningen for å bli diskret analysert for å kunne måle nøyaktig.
Kan tjene deg: flytende tilstandDet vil si at i en flytende løsning bør dette ikke introduseres fullstendig i den, men må dryppes med den eller kort berøre en prøve av stoffet.
Når det gjelder en gassoppløsning, må gassen passere på overflaten av papiret for å tillate kontakt og denne endringsfargen.
Ph -Metros
PH-meters fungerer etter den potensielle elektriske forskjellen mellom en pH og en referanseelektrode.
PH-meteren måler spenningen som eksisterer mellom to elektroder i en løsning og viser resultatet konvertert til en tilsvarende pH-verdi.
Selve utstyret består av et par elektroder - hvorav den ene er metallisk og ufølsom for pH i løsningen - og en enkel elektronisk forsterker. For sin kalibrering er utstyret kalibrert med kjente pH -løsninger.

