Immunofluorescence Foundation, protokoll og applikasjoner
- 4512
- 973
- Oliver Christiansen
De Immunofluorescens Det er en kraftig immunomarcy -teknikk som bruker antistoffer forenet kovalent til fluorescerende molekyler for å identifisere spesifikke mål i celleprøver festet på en solid støtte.
Denne teknikkens mikroskopiske observasjon av immunspesifisitet, og muliggjør observasjon av levende eller døde celler som kan ha små mengder antigener. Det er mye brukt både innen forskning og innen klinisk diagnose av forskjellige patologier.
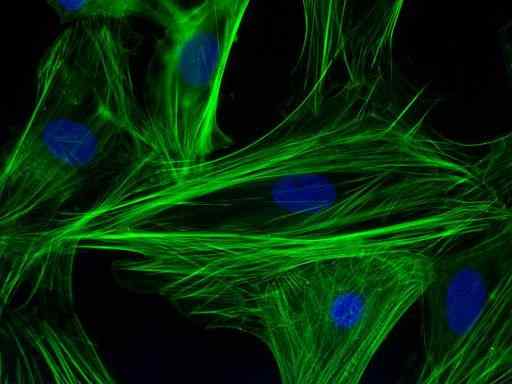
 Immunomariness av aktinfilamenter i kardiomyocyttceller (kilde: PS1415 [CC BY-SA 4.0 (https: // creativecommons.Org/lisenser/by-SA/4.0)] via Wikimedia Commons)
Immunomariness av aktinfilamenter i kardiomyocyttceller (kilde: PS1415 [CC BY-SA 4.0 (https: // creativecommons.Org/lisenser/by-SA/4.0)] via Wikimedia Commons) Denne hovedsakelig kvalitative teknikken (med noen kvantitative varianter), må gjøre spesielt med visualiseringen av en prøve av produktet av en fluorofor, som er et lysstoffmolekyl festet til et antistoff og som er i stand til å spennende seg selv i en viss bølgelengde.
I cellesammenheng er det veldig nyttig å studere nærvær/fravær og subcellulær plassering av proteiner. Teknikken ble brukt i begynnelsen på det kliniske feltet for diagnose av virus som influensa og deretter for mange andre smittsomme sykdommer.
Det er en teknikk for stor følsomhet, og med riktig mikroskopi -team kan det ha en veldig god oppløsning. Det krever, for observasjon, bruk av konfokale eller epifluorescensmikroskop.
Til tross for at du er veldig populær, kan du imidlertid presentere noen viktige problemer med å oppnå uspesifikk fluorescens som genererer en viss "støy" i bakgrunnen, noe som ofte begrenser riktig lesing av resultatene.
[TOC]
Basis
Immunofluorescens er basert på utnyttelse av det biologiske fenomenet med interaksjonsreaksjonen mellom et antistoff og et antigen. Det må gjøre spesielt med visualisering eller påvisning av denne reaksjonen når spennende lysstoffmolekyler ved en spesifikk bølgelengde.
Et antistoff er et immunoglobulinprotein som skilles ut fra aktive B -celler, og genereres spesielt mot et antigen, som kan forbundet med stor affinitet og spesifisitet. Immunofluorescence benytter seg av IgG -immunoglobuliner, som finnes løselig i blodserum.
Antistoffene er molekyler opp til 950 kDa sammensatt av to korte peptid (lys) og to lengder i form av "y" (tung). Både lys- og tunge kjeder er delt inn i to domener: en variabel, i stand til å gjenkjenne antigenet, og en annen konstant eller bevart, karakteristisk for hver art.
Antigener er funksjonelt definert som molekyler som kan gjenkjennes av et antistoff og er for det meste proteiner. Når et dyr blir utsatt for et antigen, aktiveres immunsystemets lymfocytter, og produserer spesifikke antistoffer mot det og fungerer som et forsvarssystem.
Et antigen, for eksempel et protein, for eksempel, kan ha mer enn en epitop eller gjenkjenningssted for et antistoff, så serumet til dyret utsatt for et antigen kan ha polyklonale antistoffer mot forskjellige regioner av samme protein.
Det kan tjene deg: epidermis of the OnionImmunofluorescens utnytter da et dyrs evne til å produsere polyklonale antistoffer mot et spesifikt antigen for å rense det og senere bruke det for påvisning av det samme antigenet i andre sammenhenger.
Among the most used fluorescent dyes or molecules for some immunofluorescence techniques are fluorescein isootiocyanate (FITC), tetramethylrodamine-5 and 6 (tritc) isochianate, many cyanines such as Cy2, Cy3, Cy5 and Cy7 and dyes called Alexa Fluor® , like the Alexa Fluor®448.
Protokoll
Immunofluorescensprotokollen varierer imidlertid avhengig av mange faktorer, og generelt omfatter en lineær sekvens av trinn som består av:
- Forberedelse av ark og celler
- Prøve fiksering
- Permeabilisering
- Blokkering
- Immunotiv eller immunomarcaje
- Montering og observasjon
-Forberedelse
Av prøvene
Forberedelsen av prøvene vil avhenge av deres natur og hvilken type erfaring som skal utføres. Deretter vil den enkleste saken bli forklart, noe som innebærer bruk av suspenderte celler.
Suspensjonsceller, det vil si i et flytende kulturmedium, må først skilles fra dette ved sentrifugering og bør deretter vaskes med en bufferløsning eller "buffer" isosmotisk, som bevarer dens integritet.
Normalt brukes en fosfat-saltbuffer kjent som PBS, der cellene blir resuspendert.
Av arkene
Arkene som brukes til mikroskopisk observasjon, der cellene vil være satt for de tilsvarende nedstrømsbehandlingene, må også utarbeides nøye.
Disse er dekket eller "sensibilisert" med en polysinoppløsning, en syntetisk polymer som vil tjene som "molekylær lim" mellom celler og fast støtte, takket være den elektrostatiske interaksjonen mellom de positive ladningene til deres aminogrupper og de negative belastningene med proteiner som dekker celler.
Prøve fiksering
Denne prosessen består i å immobilisere proteinene som er i det cellulære interiøret for å holde deres romlige beliggenhet intakt. Molekylene som brukes skal kunne krysse alle typer cellemembraner og danne rammer med kovalente proteiner.
Formaldehyd og paraformaldehyd, glutaraldehyd og til og med metanol er mye brukt, med hvilke celleprøver inkubert for en viss tid og deretter vaske dem med en isosmotisk bufferløsning.
Etter fiksering av cellene fortsetter den å bli med dem til de tidligere sensibiliserte arkene med polysin.
Permeabilisering
Avhengig av typen test som utføres, vil det være nødvendig å permeabilisere eller ikke cellene som studeres. Hvis det som er søkt er å vite plasseringen, tilstedeværelsen eller fraværet, av et visst protein på celleoverflaten, vil permeabilisering ikke være nødvendig.
Kan tjene deg: fosfatidylinositol: struktur, trening, funksjonerPå den annen side, hvis du vil vite plasseringen av et protein inne i det cellulære interiøret, er permeabilisering uunnværlig og vil bestå av inkuberende prøver med Triton X-100, et vaskent som er i stand til å permeabilisere cellemembraner.
Blokkering
Et grunnleggende trinn i alle immunologiske teknikker blokkerer. På dette stadiet av prosedyren består blokaden av å dekke, i de sensibiliserte arkene, alle steder med polyesinmolekyler som celler ikke ble festet. Det vil si at det forhindrer noen ikke -spesifikk union.
Normalt for blokkering av løsninger med albumin av myse bovine (BSA) brukes i PBS -buffer, og de beste resultatene oppnås jo lenger det er inkubasjonstiden med denne løsningen. Etter hvert trinn, inkludert blokaden, er det nødvendig å fjerne den gjenværende løsningen ved å vaske.
Immunotiv eller immunomarcaje
Immunomariteten eller immunomaritetsprosedyren vil hovedsakelig avhenge hvis det er en direkte eller indirekte immunofluorescens (se senere).
Hvis det er en primær eller direkte immunofluorescens, vil prøvene bli inkubert med de ønskede antistoffene, som må kobles til lysstoffer. Inkubasjonsprosedyren består i å lage en fortynning av antistoffet i en løsning som BSA også vil inneholde, men i en lavere andel.
Når saken er av en sekundær eller indirekte immunofluorescens, må to påfølgende inkubasjoner gjøres. Først med de ønskede antistoffene og deretter med antistoffene som er i stand til å oppdage de konstante regionene av primære immunoglobuliner. Det er disse sekundære antistoffene som er samlet kovalent til fluoroforer.
Teknikken er veldig allsidig, noe som tillater samtidig merker av mer enn ett antigen per prøve, så lenge de har primære antistoffer koblet til forskjellige fluoroforer, i tilfelle av direkte immunofluorescens.
For samtidige merker i indirekte immunofluorescens er det nødvendig.
Som blokaden gir inkubasjon med antistoffer bedre resultater jo større tid for dette. Etter hvert trinn er det nødvendig å vaske overflødig antistoffer som ikke ble sammen med prøvene og i den sekundære immunfluorescensen er det nødvendig å blokkere før du tilsetter det sekundære antistoffet.
Visse teknikker bruker andre fargestoffer som ikke har noe med immunomaritet å gjøre, for eksempel kjernefysisk DNA -farging med DAPI fluorofor.
Montering og observasjon
I løpet av den endelige inkubasjonstiden med fluoroforer er det nødvendig at prøvene forblir i mørket. For mikroskopobservasjon er det vanlig.
Folkens
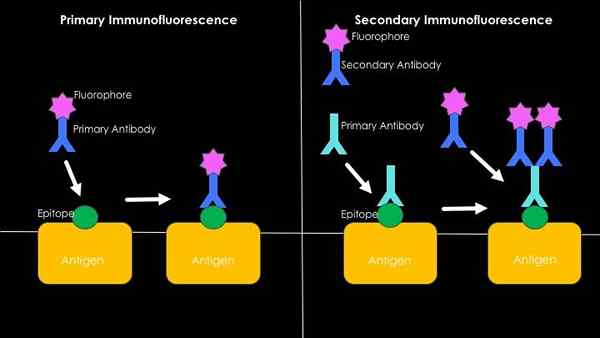 Grafisk sammendrag av direkte og indirekte immunofluorescence (kilde: Westhayl618 [CC BY-SA 4.0 (https: // creativecommons.Org/lisenser/by-SA/4.0)] via Wikimedia Commons)
Grafisk sammendrag av direkte og indirekte immunofluorescence (kilde: Westhayl618 [CC BY-SA 4.0 (https: // creativecommons.Org/lisenser/by-SA/4.0)] via Wikimedia Commons) Direkte eller primær immunofluorescens
Det har å gjøre med påvisning av antigener ved bruk av fluorescerende antistoffer. Den største fordelen med bruken av denne teknikken er dens hastighet, men mange tilfeller av ikke -spesifikk union kan oppstå i prosessen, spesielt når du studerer menneskelig sera, fordi de er rike på veldig heterogene antistoffer.
Kan tjene deg: De 5 grenene til hovedbiotechnologienIndirekte eller sekundær immunofluorescens
Det er også kjent som "sandwich" -teknikken, og dette innebærer utvikling av teknikken i to trinn. Den første har å gjøre med bruk av et ikke -fluorescerende antistoff og dets forening til det antigen av interesse.
Mot den konstante regionen av dette første antistoffet (som nå vil tjene som et antigen), brukes et andre antistoff som er i stand til å gjenkjenne det, som er assosiert med et lysstoffmolekyl.
Utseendet til et fluorescerende signal vil være et resultat av den spesifikke anerkjennelsen mellom det første ikke -fluorescerende antistoffet og antigenet av interesse; Tilstedeværelsen av de første antistoffforholdene som for det andre, som er merket og takket være at tilstedeværelsen eller fraværet av antigenet kan bestemmes.
Til tross for å være en teknikk som bruker mye lenger enn direkte immunofluorescens (siden det inkluderer et mer inkubasjonstrinn), innebærer denne teknikken ikke utformingen av et lysstoffrør for hvert antigen som er studert, noe som resulterer i økonomiske termer mer levedyktig.
I tillegg er det en mer følsom teknikk når det.
applikasjoner
Som tidligere lagt merke til, er immunofluorescens en ekstremt allsidig teknikk, som mangfoldet av bruksområder på de vitenskapelige og kliniske felt er gitt. Det kan brukes til å svare på økologiske, genetiske og fysiologiske spørsmål angående mange organismer.
Blant kliniske anvendelser brukes det for direkte diagnose av noen dermatologiske sykdommer, enten det er å bruke direkte eller indirekte immunofluorescens på epitelvevet hos pasientene som er studert.
Immunofluorescensteknikker er blitt arrangert i encellede organismer som gjær for å visualisere intranukleær og cytoplasmatiske mikrotubuli, aktin og tilhørende proteiner, 10nm filamenter og andre bestanddeler av cytoplasma, membran og cellevegger.
Referanser
- Abcam, immunocytokjemi og immunofluorescensprotokoll. Hentet fra Abcam.com
- Greph, c. (2012). Fluorescerende fargestoffer. Hentet fra Leica-mikrosystemer.com
- Miller, d. M., & Shakest, d. C. (nitten nitti fem). Immunofluorescensmikroskopi. I Metoder i cellebiologi (Vol. 48, s. 365-394). Academic Press, Inc.
- Odell, i. D., & Kok, d. (2013). Immunofluorescenseteknikker. Journal of Investigative Dermatology, 133, 1-4.
- Prince, f. J. R., Adams, a. OG. M., Druain, d. G., & Brian, K. (1991). Immunofluorescensmetoder for yeas. I Metoder for enzymologi (Vol. 194, s. 565-602). Academic Press, Inc.
- Schaeffer, m., Orsi, e. V, & Widelock, D. (1964). Anvendelser av immunofloret i folkehelsevirologi. Bakteriologiske gjennomganger, 28(4), 402-408.
- Vrieling, e. G., & Anderson, D. M. (nitten nittiseks). Immunofluorescens i planteplanktonforskning: applikasjoner og potensial. J: Phycol., 32, 1-16.
- « Areolar hastighet hvordan det beregnes og løses øvelser
- Alberto Fujimori -regjeringen første og andre regjering »

