Molmasse hvordan den beregnes, eksempler og øvelser løst
- 2385
- 553
- Prof. Theodor Gran
De Molmasse Det er en intensiv egenskap av materie som relaterer begrepet mol til massemålinger. Å være mer kortfattet, er det massemengden som tilsvarer en mol stoff; det vil si hva "veier" et avogadro -nummer, (6.022 · 1023) av visse partikler.
En mol av et hvilket som helst stoff vil inneholde samme antall partikler (ioner, molekyler, atomer osv.); Imidlertid vil massen variere fordi dens molekylære dimensjoner er definert av antall atomer og isotoper som utgjør strukturen. Jo mer masse atomet eller molekylet, desto største molmasse.
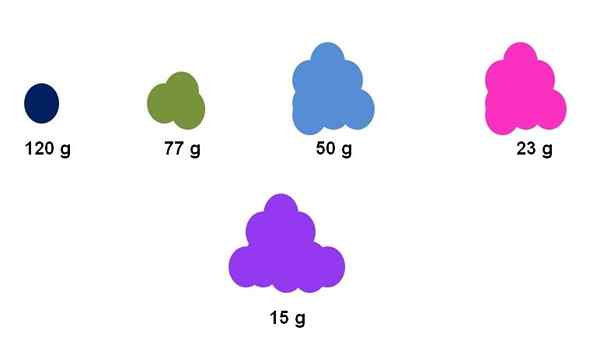
 Forskjellen mellom molmassene til forskjellige stoffer kan bli overfladisk lagt merke til av den tilsynelatende mengden av prøven. Kilde: Gabriel Bolívar.
Forskjellen mellom molmassene til forskjellige stoffer kan bli overfladisk lagt merke til av den tilsynelatende mengden av prøven. Kilde: Gabriel Bolívar. Anta for eksempel at nøyaktig en mol møtes for fem forskjellige forbindelser (overlegen bilde). Ved hjelp av en balanse er deigen blitt målt for hver klynge, uttrykt nedenfor. Denne massen tilsvarer molar deig. Av dem alle er den lilla forbindelsen den med de lettere partiklene, mens den mørkeblå forbindelsen, de tyngste partiklene.
Merk at en generalisert og overdrevet tendens er vist: jo større molmasse, desto lavere er mengden prøve som må plasseres i balansen. Imidlertid avhenger dette volumet av materie også sterkt av tilstanden til aggregering av hver forbindelse og dens tetthet.
[TOC]
Hvordan beregnes den molære deigen?

Definisjon
Molmassen kan beregnes ut fra definisjonen: mengde masse per mol stoff:
M = gram stoff /mol stoff
Faktisk er g/mol enheten som molmassen vanligvis uttrykkes, ved siden av kg/mol. Så hvis vi vet hvor mange føflekker vi har av en forbindelse eller element, og vi veier den, vil vi nå den molære massen på å bruke en enkel inndeling.
Kan tjene deg: Justus von LiebigGjenstander
Molmassen gjelder ikke bare forbindelsene, men også for elementene. Konseptet med føflekker diskriminerer ikke i det hele tatt. Derfor, ved hjelp av en periodisk tabell, plasserer vi de relative atommassene for et element av interesse, og multipliserer verdien med 1 g/mol; Dette er, Avogadros konstant, MELLER.
For eksempel er den relative atommassen til strontium 87,62. Hvis vi ønsker å ha sin atommasse, ville det være 87,62 UMA; Men hvis det vi leter etter er molmassen, vil det være 87,62 g/mol (87,62 · 1g/mol). Og slik oppnås molmassene av alle andre elementer på samme måte, uten engang å gjøre slik multiplikasjon.
Forbindelser
Molmassen til en forbindelse er ikke noe mer enn summen av de relative atommassene i atomene multiplisert med MELLER.
For eksempel vannmolekylet, h2Eller, den har tre atomer: to av hydrogen og et av oksygen. De relative atommassene av H og O er henholdsvis 1 008 og 15.999. Dermed legger vi til massene multipliserer med atomnummeret som er til stede i det sammensatte molekylet:
2 H · (1,008) = 2,016
1 o · (15.999) = 15.999
M(H2O) = (2.016 + 15.999) · 1g/mol = 18.015 g/mol
Det er en ganske vanlig praksis å utelate MELLER til slutt:
M(H2O) = (2.016 + 15.999) = 18.015 g/mol
Det er underforstått at den molære deigen har enheter g/mol.
Eksempler
En av de mest kjente molmassene har nettopp blitt nevnt: vannet, 18 g/mol. De som blir kjent med disse beregningene, når et punkt der de er i stand til å huske noen molmasser uten å lete etter dem eller beregne dem som ble gjort opp. Noen av disse molmassene, som fungerer som eksempler, er følgende:
Det kan tjene deg: Fordeler og ulemper ved helsekjemi-ENTEN2: 32 g/mol
-N2: 28 g/mol
-NH3: 17 g/mol
-Ch4: 16 g/mol
-Co2: 44 g/mol
-HCl: 36,5 g/mol
-H2SW4: 98 g/mol
-Ch3COOH: 60 g/mol
-Tro: 56 g/mol
Merk at de gitte verdiene er avrundet. For mer presise formål må molmasser med mer desimal uttrykkes og beregnes med forfalte og eksakte relative atommasser.
Løste øvelser
Oppgave 1
Gjennom analysemetoder ble det estimert at en prøveløsning inneholder 0,0267 mol av en analyt d. Det er også kjent at massen tilsvarer 14% av en prøve hvis totale masse er 76 gram. Beregne molmassen til den påståtte analytten d.
Vi må bestemme massen av D som er oppløst i løsningen. Vi fortsetter:
Masse (d) = 76 g · 0,14 = 10,64 g d
Det vil si at vi beregner 14% av de 76 gramene i prøven, som tilsvarer gramene til analytten d. Deretter, og til slutt, bruker vi definisjonen av molmassen, siden vi har tilstrekkelige data til å beregne den:
M(D) = 10,64 g d/ 0,0267 Mol D
= 398,50 g/mol
Hva oversettes som: en mol (6.022 · 1023) Fra og har en masse lik 398,50 gram. Takket være denne verdien kan vi vite hvor mye av, og vi vil veie på balansen i tilfelle vi for eksempel ønsker en løsning av en molsk konsentrasjon på 5 · 10-3 M; det vil si oppløs 0,1993 gram og i en liter løsningsmiddel:
5 · 10-3 (mol/l) · (398,50 g/mol) = 0,1993 g og
Oppgave 2
Beregn molmassen av sitronsyre, vel vitende om at dens molekylformel er C6H8ENTEN7.
Den samme formelen C6H8ENTEN7 Det letter forståelsen av beregningen, siden den forteller oss en gang antallet atomer av C, H og eller at det er i sitrusskyresyre. Derfor gjentar vi det samme trinnet som er laget for vann:
Kan tjene deg: Dodecil natriumsulfat (SDS): struktur, egenskaper, bruk6 C · (12.0107) = 72.0642
8 H · (1 008) = 8.064
7 o · (15.999) = 111.993
M(sitronsyre) = 72.0642 + 8.064 + 111.993
= 192,1212 g/mol
Øvelse 3
Beregn den molære deigen til pentahydratkobber sulfat, CUO4· 5H2ENTEN.
Vi vet før molmassen med vann er 18.015 g/mol. Dette tjener til å forenkle beregningene, fordi vi utelater det for øyeblikket og fokuserer på Cuo vannfrie salt4.
Vi har at de relative atommassene av kobber og svovel er henholdsvis 63.546 og 32.065. Med disse dataene fortsetter vi på samme måte som med oppgave 2:
1 cu · (63.546) = 63.546
1 s · (32.065) = 32.065
4 o · (15.999) = 63.996
M(Cuso4) = 63.546 + 32.065 + 63.996
= 159.607 g/mol
Men vi er interessert i den molære deigen til pentahydratsalt, ikke vannfri. For å gjøre dette, må vi legge til resultatet den tilsvarende massen av vannet:
5 H2O = 5 · (18.015) = 90.075
M(Cuso4· 5H2O) = 159,607 + 90,075
= 249.682 g/mol
Referanser
- Whitten, Davis, Peck & Stanley. (2008). Kjemi. (8. utg.). Cengage Learning.
- Wikipedia. (2020). Molmasse. Hentet fra: i.Wikipedia.org
- Nissa Garcia. (2020). Hva er molmasse? Definisjon, formel og eksamener. Studere. Gjenopprettet fra: Studie.com
- Dr. Kristy m. Bailey. (s.F.). Støkiometri -opplæring
Finne molmasse. Hentet fra: OCC.Edu - Helmestine, Anne Marie, PH.D. (2. desember 2019). Molmasseeksempel problem. Gjenopprettet fra: Thoughtco.com
- « Darmstadtio oppdagelse, struktur, egenskaper, bruk
- Vann eller hydrologiske syklusstadier og betydning »

