Ovoalbúmin struktur, funksjoner, denaturering
- 3144
- 348
- Mathias Aas
De ovoalbúmina Det er det mest tallrike proteinet av "klare" av fugler av fugler. Det tilhører proteinfamilien kjent som "serpins" eller "hemmere av serin proteas", som er en ekstremt mangfoldig gruppe eukaryoter (inkluderer mer enn 300 homologe proteiner).
Det var et av de første isolerte proteinene med stor renhet, og takket være den overraskende overflod i fuglenees reproduktive strukturer, brukes dette mye som "modell" i utarbeidelsen av "standarder" for studiet av strukturen, egenskapene , egenskapene, egenskapene, syntesen og sekresjonen av mange proteiner.
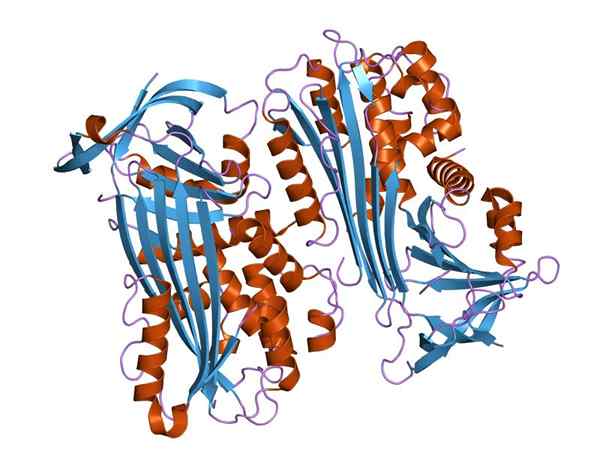
 Ovalbúmina Molecular Structure (Kilde: Jawahar Swaminathan og MSD -ansatte ved European Bioinformatics Institute [Public Domain] via Wikimedia Commons)
Ovalbúmina Molecular Structure (Kilde: Jawahar Swaminathan og MSD -ansatte ved European Bioinformatics Institute [Public Domain] via Wikimedia Commons) Prosentvis inkluderer ovoalbumin mellom 60 og 65% av det totale proteininnholdet i eggehvite, men i motsetning til de andre medlemmene av serpinsproteinfamilien, har det ingen aktivitet som en proteaseinhibitor.
Kyllingeggene har også andre proteiner:
- Ovotransferrin, også kalt conalbúmina, som representerer 13% av det totale proteininnholdet
- Ovomucoid, et glykoprotein som inkluderer 11% av totalen
- Ovomucin, et annet sulfert glykoprotein som representerer 3.5%
- Den glatte eller muramidase, som også inkluderer 3.5% av klart protein
- Globuliner, som representerer 4%
Syntesen av ovoalbumin oppstår fra en blanding av mellomledd peptider under transporten av egget gjennom fuglene og det er rapporter om at transkripsjonen av genene bare oppstår som respons på tilstedeværelsen av østrogen, et seksuelt hormon.
[TOC]
Struktur
Ovoalbúmin er en monomer fosfografisk på rundt 45 kDa molekylvekt og et isoelektrisk punkt nær 4.5. I sin struktur er det derfor mange steder for fosforylering og glykosylering, som er veldig vanlige post -translasjonelle modifikasjoner i proteiner.
Det kan tjene deg: Utviklingsbiologi: Historie, hvilke studier, applikasjonerDette proteinet er kodet av et 7 -gen.700 basepar, preget av tilstedeværelsen av 8 eksoner ispedd 7 intron.
Ovalbuminet av kyllingegg har 386 aminosyreavfall, og det er vist at den rene formen for dette proteinet består av tre underklasser kjent som henholdsvis A1, A2 og A3, karakterisert ved å inneholde to, en og ingen fosfatgruppe, henholdsvis.
Når det gjelder tertiærstrukturen, avslører aminosyresekvensen til ovoalbumin tilstedeværelsen av 6 cysteinrester, hvorav fire disulfidbroer dannes. I tillegg har noen strukturelle studier bevist at den N-terminale enden av dette proteinet er acetyled.
S-ovoalbúmina
Når eggene lagres, blir strukturen til ovalbumin modifisert, og danner det som er kjent i litteraturen som S-Ovalbumin, som er en mer stabil form mot varme og dannes på grunn av mekanismer for utveksling mellom disulfider og sulfloriler.
I tillegg til lagringstemperaturen, dannes også denne "formen" av ovoalbumin avhengig av den indre pH i egg, noe som kan forventes i enhver type protein i naturen.
De S-Ovalbumin er da noen menneskers overfølsomhetsreaksjoner som noen mennesker har lidd etter inntak av egg tilskrevet.
Funksjoner
Selv om ovoalbumin tilhører en familie av protein som er preget av dens aktivitet som proteasehemmere, har den ikke hemmende aktivitet og dens funksjon er ikke blitt fullstendig belyst.
Imidlertid har det blitt antatt at en potensiell funksjon av dette enzymet er transport og lagring av metallioner fra og fra embryoet. Andre forfattere har foreslått at dette også fungerer som en ernæringskilde til embryoet under veksten.
Kan tjene deg: noxaFra det eksperimentelle synspunktet representerer Ovoalbúmina en av de viktigste "modell" -proteiner for forskjellige strukturelle, funksjonelle, syntese og proteinsekresjonsstudiesystemer, så det har vært veldig viktig for fremgang i vitenskapelige saker.
Funksjoner for matindustri
I tillegg, med tanke på det faktum at det er et av de mest tallrike proteinene i kyllingegg, er dette et ekstremt viktig protein for ernæring av mennesker og andre dyr som lever av egg fra forskjellige fugler.
I det kulinariske aspektet brukes ovoalbumin, så vel som resten av eggehvite proteiner, for deres funksjonelle egenskaper, spesielt ved skumdannelseskapasitet, prosess der polypeptider er denaturert, og danner luftgrensesnittet /stabil væske typisk for nevnte tilstand av spredning.
Denaturering
Siden ovoalbumin har mange sulfhydrilgrupper, er dette et ganske reaktivt og lett denatulerbart protein.
Denatureringstemperaturen til ovoalbumin er mellom 84 og 93 ° C, og er 93 som kjennetegner formen S-ovoalbúmin, som er mer stabil ved høyere temperaturer. Denaturering av varme ovoalbumin resulterer i dannelsen av den karakteristiske hvitaktige "geler" som blir observert under matlagingen av eggene.
 Stekte egg (kilde: hva midtoing [CC BY-SA 4.0 (https: // creativecommons.Org/lisenser/by-SA/4.0)] via Wikimedia Commons)
Stekte egg (kilde: hva midtoing [CC BY-SA 4.0 (https: // creativecommons.Org/lisenser/by-SA/4.0)] via Wikimedia Commons) PH er også en viktig faktor når denaturering av dette proteinet blir vurdert, samt type og konsentrasjon av salter. For ovoalbúmina er en denaturering pH rundt 6.6.
Kan tjene deg: Tropical Jungle: Flora, Fauna, Egenskaper, klima, lettelseUnder forskjellige denatureringsbetingelser har ovoalbuminmolekyler en høy tendens til å legge til, en prosess som vanligvis kan akselereres med tilsetning av salter og økning i temperaturen.
Evnen til ovoalbumin og annet protein av eggehvite til å danne gel -type strukturer når de blir oppvarmet, så vel som deres evne til å slå sammen vannmolekyler og fungere som emulgatorer, er de som gir dem sine viktigste funksjonelle egenskaper og grunnen til at de er Så utnyttet spesielt i matindustrien.
Prosessen med denaturalisering av dette proteinet har vært veldig nyttig for undersøkelsen av overgangsmekanismene mellom faststoff- og gel -tilstandene, så vel som for studiet av effekten som forskjellige typer salter har til forskjellige konsentrasjoner (ionisk kraft) på integritet av proteiner.
Referanser
- Huntington, J. TIL., & Stein, P. OG. (2001). Struktur og egenskaper til ovalbumin. Journal of Chromatography B: Biomedical Sciences and Applications, 756 (1-2), 189-198.
- Koseki, t., Kitabatake, n., & Doi, og. (1989). Irmal denaturering og dannelse av lineære aggregater av ovalbumin. Mathydrocolider, 3 (2), 123-134.
- Nisbet, a. D., Soundry, r. H., Moir, a. J., Fothergill, l. TIL., & Fothergill, J. OG. (1981). Den komplette aminoen - syresekvens av høne ovalbumin. European Journal of Biochemistry, 115 (2), 335-345.
- Phillips, g. ENTEN., & Williams, P. TIL. (Eds.). (2011). Håndbok for matproteiner. Elsevier.
- Fet-o'donnell, e. (1993). Ovalbumin -familien av serpinproteiner. FEBS Letters, 315 (2), 105-108.
- Sankar, d. S., & Theis, h. W. (1959). Biosyntese av ovalbumin. Nature, 183 (4667), 1057.
- Sharif, m. K., Salem, m., & Javed, K. (2018). Matmaterialvitenskap i eggpulverindustri. I Roll of Materials Science in Food Bioengineering (PP. 505-537). Akademisk presse.
- Weijers, m., Barneveld, p. TIL., Cohen Stuart, m. TIL., & Visschers, r. W. (2003). Varmeindusert denaturering og aggregering av ovalbumin ved nøytral pH beskrevet av irreversibel skog -ordre kinetikk. Protein Science: A Publication of the Protein Society, 12 (12), 2693-2703.

