Fysiske og kjemiske egenskaper ved vann

- 1688
- 116
- Magnus Sander Berntsen
De Fysiske og kjemiske egenskaper ved vann De er alle disse manifestasjonene av vannet som vi kan måle takket være interaksjonene mellom molekylene deres med seg selv eller omgivelsene. Men hva er vann? Vann er et kjemisk stoff eller molekyl som dannes ved forening av et oksygenatom (O) med to hydrogenatomer (H).
Disse tre atomene forblir forent ved dannelse av kovalente bindinger, veldig sterke og stabile koblinger. Vannmolekylet er for formel H2Eller, å kunne skrive som H-O-H. Det er dette molekylet, dets koblinger og dets interaksjoner er ansvarlige for å være et fargeløst og smakløst flytende stoff.

Vann er i en stor distribuert andel over hele jorden, mellom ferskt og saltet vann. Vann er uunnværlig for at livet skal eksistere på planeten vår, siden det er en veldig verdifull naturressurs. Det er mellom 60 og 70% i levende organismer, som er en høy andel som lar dem oppfylle utallige funksjoner.
Blant noen av disse viktige funksjonene er strukturelle, regulatorer som vedlikehold av kroppstemperatur og pH -regulering (surhet eller alkalinitet) innenfor normale grenser. På samme måte utfører vann transport av næringsstoffer og avfall hos levende vesener.
Det brukes også på mange områder av det produktive, teknologiske, vitenskapelige og daglige rutinemessige arbeidet til mennesket; Fra toalett, matlaging, blant andre bruksområder.
[TOC]
Fysiske vannegenskaper
De fysiske egenskapene til vann er relatert til egenskapene eller størrelsene som kan måles eller bestemmes når man vurderer materie, for eksempel dens masse, energi, blant andre.
Blant de fysiske størrelsene på vann er dens farge, lukt, måtene den kan bli funnet på, og alle de som vi kan bestemme uten reaksjoner eller endre dens kjemiske sammensetning.
Smak
Ved å smake litt rent vann til ganen vår viser det seg at det er insabor eller smakløs. Det er like luktfritt eller lukt. For rensingsprosessen kan en svak lukt oppfattes som skyldes klorrester. Det er mineralene som gir vann forskjellige smakerbrev.
Aspekt

Vann generelt er fargeløst og gjennomsiktig når det blir observert i et glassglass. Imidlertid ser det ut til at den hadde en lys lys blå farge når den ble akkumulert i store mengder i store containere, eller når det ble observert i isbreer, elver eller hav.
Kan tjene deg: Hva er forskningskilder?Og faktisk viser vannet en viss blek blåaktig farge, hvis oppfatning er konsentrert jo høyere mengde vann.
Vannstater
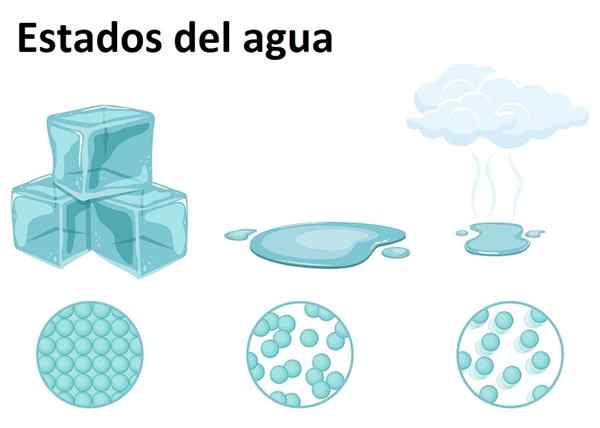 Fast, flytende og gassformig tilstand
Fast, flytende og gassformig tilstand Vann er veldig rikelig på jorden og kan finnes i noen av de tre tilstandene av materie: fast, flytende eller gassformig. Vann ved romtemperatur er et flytende stoff, som tilsvarer den vanligste formen.
Som fast stoff kalles vann is eller snø, avhengig av størrelsen på krystaller og prosessen med dannelsen. I mellomtiden dannes den gassformige tilstanden når vannet passerer fra flytende tilstand til gassen, og danner den berømte vanndampen, lett gjenkjennelig på kjøkkenet og over maten.
Tetthet
Ren vanntetthet varierer rundt 1 g/cm3. I mellomtiden er tettheten av sjøvann litt høyere på grunn av saltet det inneholder.
Frysepunktet
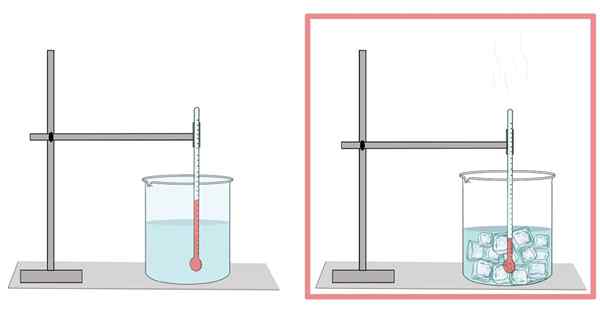
Vann fryser ved 0 ° C. Ved denne temperaturen går fra sin flytende fase til det faste stoffet. Når vannet er frossent, utvides det. Det er grunnen til at den i sin faste form har mindre tetthet enn i sin flytende tilstand, noe som gjør det lettere for is å flyte på flytende vann.
På samme måte er dette grunnen til at vannkjøling i en flaske ikke skal fylles mye, siden isen utvides og slutter å bryte flasken.
Kokepunkt
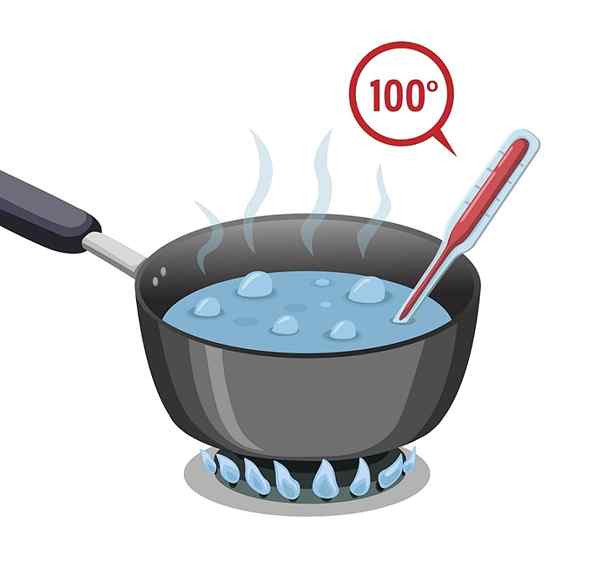
Vannet har et høyt kokepunkt som er 100 ° C. Det må utsettes for varmt slik at den kan varme og koke eller nå kokepunktet.
Vannet har da en høy spesifikk varme, eller også kalt varmekapasitet, noe som gjør det forsinkelse i oppvarmingen; Men også for å avkjøle, det vil si at prosessen som kreves for å miste den ervervede varmen er treg.
Denne egenskapen gjør den veldig nyttig i kjølesystemer, i kroppstemperaturreguleringssystemer, blant annet relatert.
Elektrisk konduktivitet
Vann er en god strømleder. Imidlertid vil rent vann alltid ha en viss mengde ioner, noe som gir den egenskapen til å ha en av de høyeste dielektriske konstanter blant ikke -metalliske væsker.
Samhold
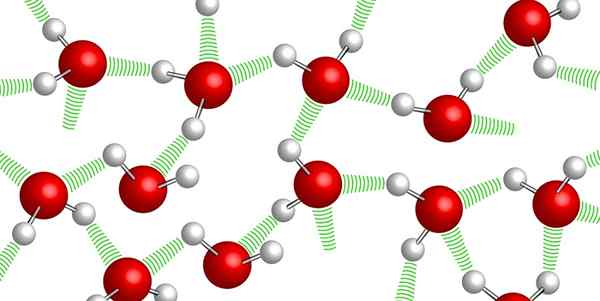 Hydrogenbroer mellom vannmolekyler
Hydrogenbroer mellom vannmolekyler Vannmolekyler forblir sammen med hverandre takket være de så -kallede hydrogenbroene: svake bindinger som er etablert mellom ett og et annet vannmolekyl. På grunn av dette høye samholdsnivået er det veldig vanskelig å komprimere vann.
Kan tjene deg: 7 dokumentariske forskningsinstrumenterTiltredelse

Det er lett for vann å feste seg, for eksempel til den godt rene overflaten av et glass, og danner en film, som vi kaller fuktighet eller "våt". Også vann overholder oss raskt, så vi blir våte så snart vi kommer inn i et basseng. Ellers ville vi tørke på få sekunder.
Overflatespenning
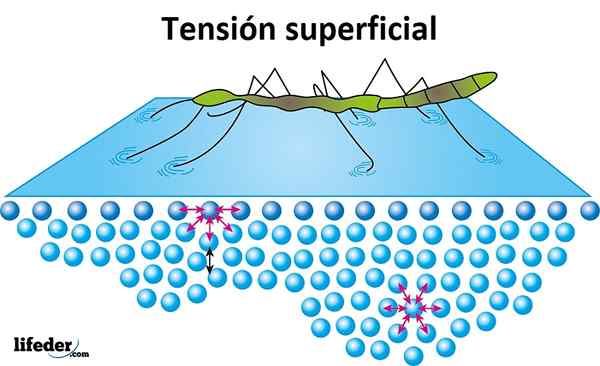
Overflatespenningen er motstanden som tilbys av væsken på overflaten for å bli penetrert. Vann har en høy overflatespenning, produkt av samholdet som eksisterer mellom molekyler, noe som gjør at det enkelt dannes, i stedet for fritt å spre en glatt overflate.
Overflatespenningen bevises når insekter ser ut til å bevege seg eller gå på vannet uten å synke, og det er grunnen til at noen blader eller andre lette gjenstander kan flyte over vannet.
Kapillaritet

Den enkle vannet stiger med eller lavt gjennom et kapillærrør beskriver vannets kapillaritetsegenskap. Denne egenskapen skyldes også de høye egenskapene til samhold og vedheft som vann har.
Kapillariteten utnyttes av plantens natur for å levere vann til bladene på de høyeste grenene til et tre, samt letter dets absorpsjon av røttene til plantene.
På samme måte gjør egenskapene til overflatespenning og kapillaritet vannet til en strukturell del av cellene, som er en del av blodet, og som renner eller flyter lett gjennom de forskjellige blodkarene.
Løsningsmiddelhandling

Vann kan løse opp mange stoffer, noe som er viktig for levende organismer, siden alle de kjemiske reaksjonene fra levende vesener forekommer i et vandig miljø. I levende organismer fungerer det som en transport av næringsstoffer, ioner og mange andre stoffer.
Det tjener også til transport av avfall, for eksempel urea, som elimineres i urinvann. Når et stoff oppløses og blandes godt med vann, sies det at det er hydrofil eller hydrosoluble. Hvis du ikke blander eller løses godt opp, sies det at stoffet er hydrofob eller uoppløselig i vann.
Kjemiske vannegenskaper
Kjemiske egenskaper eller egenskaper er de som skjer når endringer i den kjemiske vannstrukturen produseres. Det er da viktig å ta en kort titt på molekylstrukturen.
Kjemisk natur
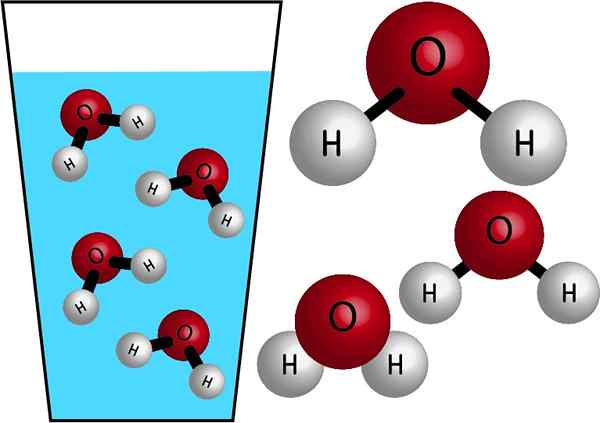
Vann er et uorganisk molekyl, fordi det ikke inneholder C (karbon), og dens kjemiske formel er h2ENTEN. Atomene deres blir forbundet med å dele elektroner som danner kovalente bindinger, sterke og veldig stabile koblinger. Molmassen er 18 g/mol, det vil si at en mol vann har en masse på 18 gram.
Kan tjene deg: vitenskapelig forskningPolaritet
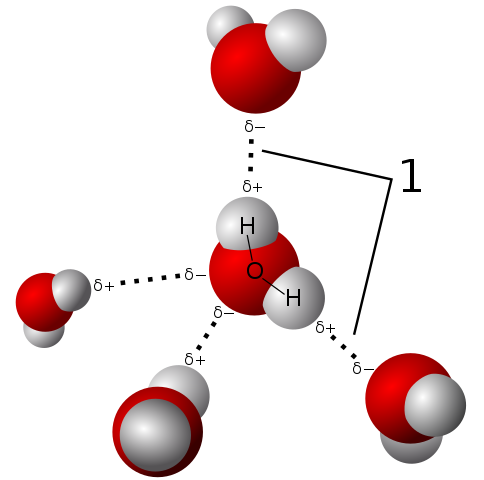 Vannpolaritet lar molekylet etablere veldig sterke hydrogenbroer
Vannpolaritet lar molekylet etablere veldig sterke hydrogenbroer Vannmolekylet er nøytralt, men det presenterer en viss polaritet, fordi delingen av elektronene ikke er så rettferdig.
Ettersom oksygen tiltrekker seg sterkere de delte elektronene for seg selv, er vannmolekylet med denne siden der oksygen er med en tendens til å ha en viss negativ belastning; Og derfor forblir det med en positiv delvis belastning der hydrogenene er (observer det overlegne bildet).
Denne polariteten letter foreningen med hverandre av vannmolekylene og vannforeningen med andre molekyler som også har belastningsforskjeller i strukturen deres, som fremmer de fysiske egenskapene beskrevet i de tidligere seksjonene.
Ionisering
Spontant i flytende vann er det en svak ionisering eller selvdissosiasjon. Det betyr at noen av molekylene blir omorganisert ved å endre sin normale molekylstruktur som genererer nye elektrisk belastede molekyler, for eksempel hydroniumioner (H3ENTEN+) og hydroksyl (OH-).
Reaktiv kapasitet
Vann reagerer med mange stoffer, og danner et stort mangfold av kjemiske forbindelser. Ved elektrolyse kan vann brytes ved å skille oksygen fra de to hydrogenene. Denne prosessen oppstår når en elektrisk strøm går gjennom vann. Selv vann i sin faste form kan også være en del av noen kjemiske reaksjoner.
Ph
 pH nær 7
pH nær 7 Rent vann har en nøytral pH (lik 7), mens sjøvann er litt alkalisk (større enn 7). Regnvann blir surgjort (pH mindre enn 7) litt når de blandes med komponentene som finnes i atmosfæren, for eksempel karbondioksid eller CO2, For eksempel.
Anfoterisme
Vann er amfotat, det vil si at det kan oppføre seg som en syre eller som en base avhengig av pH i løsningen. Denne kjemiske egenskapen støtter sin rolle som PH -regulator.
Referanser
- Shiver & Atkins. (2008). Uorganisk kjemi. (Fjerde utgave). Mc Graw Hill.
- Whitten, Davis, Peck & Stanley. (2008). Kjemi. (8. utg.). Cengage Learning.
- Castillero m. ENTEN. (2020). Psykologi og sinn. De 15 fysiske og kjemiske egenskapene til vann. Gjenopprettet fra: psykologi og.com
- Wikipedia (2020). Vannegenskaper. Hentet fra: i.Wikipedia.org
- Skarp k. TIL. (s.F.). Vann: Struktur og egenskaper. Gjenopprettet fra: krystall.Med.Upenn.Edu
- Byju's. (s.F.). Fysiske og kjemiske egenskaper ved vann. Gjenopprettet fra: Byjus.com
- Skoleenergi og miljø. (s.F.). Vann var en ressurs. Gjenopprettet fra: Eariscuola.nett

