Syntese reaksjonstyper, faktorer, eksempler
- 2183
- 578
- Magnus Sander Berntsen
De Synteseaksjon Det er en der to eller flere reagenser reagerer for å kunne opprinnelig, kvantitativt, ett eller flere produkter, enten på laboratorium eller industrielt nivå. Dette er en av de mest grunnleggende reaksjonene i kjemi, og dens typer og design grenser til nesten uendelig.
Generisk måte kan representeres med skjemaet: a+b → c. I en enkel synteseaksjon reagerer et reagens for å reagere med et annet B -reagens, for å produsere et C -produkt. Det sies at det består av et enkelt trinn. Imidlertid kan det skje at å reagere først med E, etterfulgt av F, og til slutt med G (andre reagenser), for å transformere til produkt C; det vil si at den samme reaksjonen finner sted i flere trinn.

Uansett et enkelt trinn eller mange, er alle synteseaksjoner basert på effektivitet (termodynamikk og kinetisk) som reagenser reagerer på å transformere til produkter, samt eksperimentell ytelse. Det er ønsket at en synteseaksjon passerer vellykket og produserer så mange produkter som mulig.
[TOC]
Typer synteseaksjoner
Enkel eller flere
Syntese reaksjoner er ikke helt enkle å klassifisere. Det kan være et problem relatert til kjemikerens kriterier. Fordi? Anta at flere reaksjoner som er kommentert ovenfor:
A + E → P1
P1 + F → p2
P2 + G → c
Å være s1 Og s2 formidlere som ikke er av interesse. Reaksjonen av produktsyntese eller forbindelse C, med start fra A som hovedreagens (begrensende eller begrensende reagens), er flere eller kompleks, fordi den oppstår i flere trinn, der andre reagenser deltar: E, F og G og G.
Hver av de tre foregående reaksjonene kan bestå og en type kjemisk reaksjon i seg selv. Det vil si at en synteseaksjon kan være av enhver annen type kjemiske reaksjoner (dobbel forskyvning, redoks, forbrenning, nøytralisering, nitrering, substitusjon, etc.), så lenge et produkt har sin opprinnelse og har en eksperimentell ytelse tilknyttet.
Så:
A + E → P1
Det kan sees på som en enkel synteseaksjon for produkt P1, uavhengig av typen reaksjon som er. Og også:
P1 + F → p2
Det er en annen enkel synteseaksjon for produkt P2.
Uorganisk eller organisk
Syntese reaksjoner kan være av noe slag når det gjelder reaksjonens natur og dens molekylære mekanisme. Imidlertid kan disse deles i henhold til den kjemiske naturen til reagenser og produkter.
Kan tjene deg: natriumacetat: struktur, egenskaper, syntese, brukFor eksempel, hvis reagenser er uorganiske stoffer, snakker vi om uorganisk syntese; Selv om de var organiske stoffer, ville vi allerede snakket om organisk syntese.
Feltet for organisk syntese er kolossal, ettersom det dekker produksjonene av medisiner, fargestoffer, plast, insektmidler, lim, parfymer, konserveringsmidler, blant tusenvis av andre produkter.
Faktorer involvert i synteseaksjoner
Faktorene som er involvert i synteseaksjoner er alle parametrene eller variablene, fysiske og kjemiske, noe som direkte påvirker reaksjonsytelsen og kvaliteten på produktene oppsto. Noen av dem er følgende:
Temperatur
Temperaturen er essensiell i enhver syntesereaksjon. Avhengig av termodynamikken din, kan det være praktisk for den å forbli lav eller høy. På samme måte er det temperaturområder der uønskede laterale reaksjoner er sannsynlige, så det er viktig å kontrollere det og bekrefte det til enhver tid.
Tid
Tid er også viktig i synteseaksjoner, fordi det må sikre at det er nok til å garantere etablering av balanse. Etter en viss tid vil mer produkt opphøre å oppnås, og det er når det avgjøres for å stoppe syntesen helt.
Konsentrasjoner og kvalitet på reagenser
Jo mer konsentrert reagensene er, jo raskere vil reaksjonene være. Imidlertid er det også viktig å være tydelig på andelen av konsentrasjonene, så vel som størrelsen, siden minimumsendringen vil påvirke den endelige ytelsen.
På den annen side må reagensene være så rene som mulig, ellers vil feilaktige konsentrasjoner antas; Eller verre, produktene vil være forurenset, eller uønskede reaksjoner vil oppstå.
Opphisselse
Måten reaksjonsmediet omrøres på, vil påvirke rapides av synteseaksjoner.
Press
Trykket, som konsentrasjon, spiller en avgjørende rolle, spesielt når reagenser er brusarter eller stoffer. Jo større trykk, jo større er kollisjonene eller interaksjonene mellom reagensene, og det vil derfor være mer sannsynlig å reagere.
Ph
PH (syre eller basisk) påvirker direkte mekanismen for en reaksjon, så det er en nøkkelfaktor for å definere hvilke produkter som vil oppnås ved slutten av syntesen.
Kan tjene deg: Kokingspunkt: Konsept, beregning og eksemplerKatalysatorer
Katalysatorer er stoffer som akselererer kjemiske reaksjoner, men uten konsumert under prosessen. Det er en syntese at uten ditt inngripen ville det være umulig.
Syntese reaksjoner eksempler
Neste, og til slutt, kjemiske ligninger for synteseaksjoner av flere forbindelser vil bli sitert.
Bordsalt (natriumklorid)
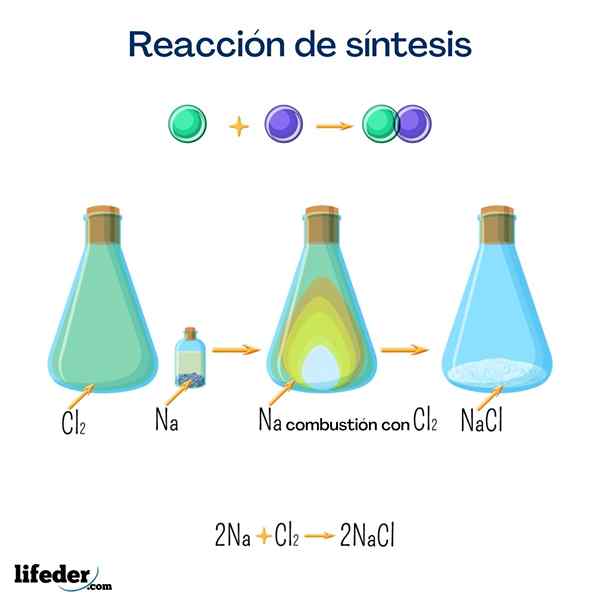
Dette saltet er et av de mest kjente av alle for sin store innenlandske bruk. Det oppnås fra natrium og klor, og selv om det kan oppnås ved følgende reaksjon, er det veldig enkelt å finne den naturlig.
2 Na+CL 2 → 2 NaClGlukose
Dette er en av de viktigste reaksjonene for livet å eksistere slik vi kjenner det. Planter bruker karbondioksid og miljø i miljøet med sollys for å produsere glukose og oksygen.
Reaksjonen på en veldig generell måte kan sees nedenfor, men det er viktig å forstå at det bak det er flere reaksjoner og mekanismer for at dette er mulig.
6CO2 + 6H2O → C6H12O6 + O2
Sakkarose
Denne synteseaksjonen forekommer i levende organismer og gis når polymeriserende glukose med fruktose. På grunn av strukturen deres, samhandler disse to molekylene, og det endelige resultatet er sukrose og vann, som det kan sees i følgende ligning:
C6H12O6 + C6H12O6 → C12H22O11 + H2O
Ammoniakk
3 H2(g) + n2(g) → 2 nh3(g)
Reagensene h2 og n2 De er gassformige. Trykket må være høyt for at molekylene dine skal reagere og stamme ammoniakk, NH3. Dette er en av de viktigste syntesereaksjonene i industriell kjemi.
Vann
2 h2(g) + eller2(g) → 2 H2O (g)
H2 Jeg2 reagere eksotermisk for å produsere vanndamp. Mengden av energi som frigjøres er slik at hydrogen er et av de mest lovende drivstoffene i luftfartsapplikasjoner.
Alkohol
C2H4(g) + h2Eller (l) → cho3Ch2Å (l)
Etanol er kjent som alkohol, bare å være bare en av de mange alkoholer som finnes. Dens synteseaksjon består i hydrering av etylen, C2H4 eller h2C = Ch2, Hvor et vannmolekyl tilsettes dobbeltbindingen.
Svovelsyre
Svovelsyre har flere effektive syntetiske ruter. Imidlertid består den enkleste av flere trinn:
Kan tjene deg: karboksymetylcelluloseS (s) +o2(g) → Så2(g)
2 Så2(g)+eller2(g) ⇌ 2 Så3(g)
SW3(g)+h2Eller (l) → h2SW4(g)
H2SW4(g) → h2SW4(L)
Svovel forbrenninger med overflødig oksygen for å først forvandle seg til SO2, Og så i det3. Så så3 er hydrert for å produsere H -damper2SW4, som til slutt kondenserer i h2SW4 væske. Denne syntesen er så viktig at den i seg selv indikerer hvor sterk.
Metanol
CO (g) + 2 H2(g) → CH3Å (l)
Gassene co og h2 reagere og kondensere på metallkatalysatorer for å gi opphav til metanol, den enkleste alkoholen av alle.
Magnesiumsulfat
Det kan oppstå fra en veldig enkel reaksjon som består av magnesium og svovelsyre. Det er veldig vanskelig å finne det i naturen uten vann.
Mg + H2SO4 → H2 + MgSO4
Karbondioksid
Det skjer naturlig i flere prosesser, når karbondioksid produseres med karbondioksidmolekyl.
Det er til stede i naturlige prosesser som å puste, som et reagens i fotosyntesen og forekommer lett i forbrenningsreaksjoner.
C +O2 → CO2
Saltsyre
Saltsyre brukes mye som en billig syre og som et reaktivt middel for syntese av andre forbindelser.
Cl2+H2 → 2HCl
Kalsiumkarbonat
Det er kjent som et veldig rik middel i naturen, hovedsakelig i steiner, mineraler og skjell i havet. Reaksjonen er basert på interaksjonen mellom kalsiumoksyd med karbondioksid.
CAO +CO2 → CACO3
Referanser
- Whitten, Davis, Peck & Stanley. (2008). Kjemi. (8. utg.). Cengage Learning.
- Shiver & Atkins. (2008). Uorganisk kjemi. (Fjerde utgave). Mc Graw Hill
- Graham Solomons t.W., Craig f. Yngel. (2011). Organisk kjemi. (10th Utgave.). Wiley Plus.
- Carey f. (2008). Organisk kjemi. (Sjette utgave). Mc Graw Hill.
- Morrison og Boyd. (1987). Organisk kjemi. (Femte utgave). Addison-Wesley Iberoamericana.
- Metler Toledo. (s.F.). Synteseaksjoner. Gjenopprettet fra: MT.com
- Helmestine, Anne Marie, PH.D. (27. august 2020). Syntese reaksjonsbeskrivelse pluss eksamener. Hentet fra Thoughtco.com
- Wikipedia. (2020). Kjemisk syntese. Hentet fra: i.Wikipedia.org
- Danielle Reid. (2020). Synteseaksjon: Definisjon, formel og eksempel. Studere. Gjenopprettet fra: Studie.com

