Torio -struktur, egenskaper, innhenting, bruker

- 4354
- 972
- Dr. Andreas Hopland
Han Torio Det er et metallisk element som tilhører serien med aktinider, av de så -kalt sjeldne jordene, og hvis kjemiske symbol er th. Den har et atomnummer på 90 og en atomvekt på 232 g/mol. Torio -forbindelser inneholder det vanligvis med oksidasjonsnummer +4 (th4+).
Torio -dioksidforbindelsen, tho2, Det er kjent industrielt som Toria, og brukes i de fleste av Torium -applikasjonene, preget av å være den kjemiske forbindelsen med det største smeltepunktet (3.300 ºC).
 Metallisk thoriumprøve lagret i en glassblemmer under argon. Det svartaktig belegget skyldes oksydet. Kilde: Alchemist-HP (snakk) (www.PSE-MENDELEJEW.de) / fal
Metallisk thoriumprøve lagret i en glassblemmer under argon. Det svartaktig belegget skyldes oksydet. Kilde: Alchemist-HP (snakk) (www.PSE-MENDELEJEW.de) / fal Torio ble oppdaget i 1828 av Mortar Thrane Esmark, som fant på den norske øya Løvøya, et svart mineral. Esmark leverte mineralet til Jöns Jacob Berzelius, som analyserte ham og fant et ukjent metall i ham.
Han kalte det svarte mineralet som Torita (Thorita) til ære for den skandinaviske guden Thor. I mellomtiden ble det ukjente metallet kalt Torio (Thorium). Thoriums radioaktive karakter ble opprettet av Anton Edward van Arkel og Jan Hendrik de Boer, og uavhengig av Pierre Curie og Marie Curie.
[TOC]
Toriumegenskaper
Fysisk
Thorium er et radioaktivt, lys, moderat hardt, sølv, duktil og formbar hvitt metall, som tåker veldig sakte i luften, og blir grå og senere svart. Det tilhører gruppen av aktinider, identifiserer seg med atomnummeret 90 og en atomvekt på 232 g/mol.
Radioaktivitet
Torio-232 (232Th90) utgjør mer enn 99% av det totale thoriumelementet som er til stede i jordens cortex. Det kan vurderes at det er en stabil isotop, til tross for at han er radioaktiv, siden halvlivet er 1.405 x 1010 år. Radioaktivt avtar ved utslipp av α- og ß -partikler, og γ -stråling.
Torio-232 blir forvandlet til radio-268 (268Ra88) ved å utstede en alfapartikkel, sammensatt av to protoner og to nøytroner. Thorium kan lide en serie radioaktive oppløsninger til det blir et stabilt element: Lead-208.
Kan tjene deg: blyklorid: egenskaper, struktur, brukTorio-232 er i stand til å fange nøytroner for å forvandle seg til det uran-233 radioaktive elementet, og avgir β-type stråling. Uran, derimot, brukes i kjernefysiske reaktorer for energiproduksjon.
Reaktivitet
Thorium er et elektropositivt og svært reaktivt metall. Det oksiderer veldig sakte i luften, selv om korrosjon kan oppstå etter flere måneder. Når den blir oppvarmet i luften, slås den på, og avgir et sterkt hvitt lys mens produksjonen av Torio -dioksid, tho2.
Under standard temperatur- og trykkforhold blir thorium sakte angrepet av vann. På samme måte er thorium ikke oppløst i de fleste vanlige syrer, med unntak av saltsyre, der det oppløses og etterlater en svart, uoppløselig rest.
Det er også oppløst i konsentrert salpetersyre med en liten mengde katalytisk eller fluorosylikatfluorid. Thorium er et pyroforisk metall: når det blir pulverisert er det i stand til å tenne spontant.
Struktur
Torio -atomer danner en kubikkstruktur krystall sentrert på ansikter (FCC) ved romtemperatur. Når det varmes opp over 1360 ºC, lider glasset en overgang til kubikkfasen sentrert på kroppen (BCC), med lavere tetthet. I mellomtiden får thorium under høyt trykk (100 GPa eller mer) en tett tetragonal struktur sentrert på kroppen (BCT).
Elektronisk konfigurasjon
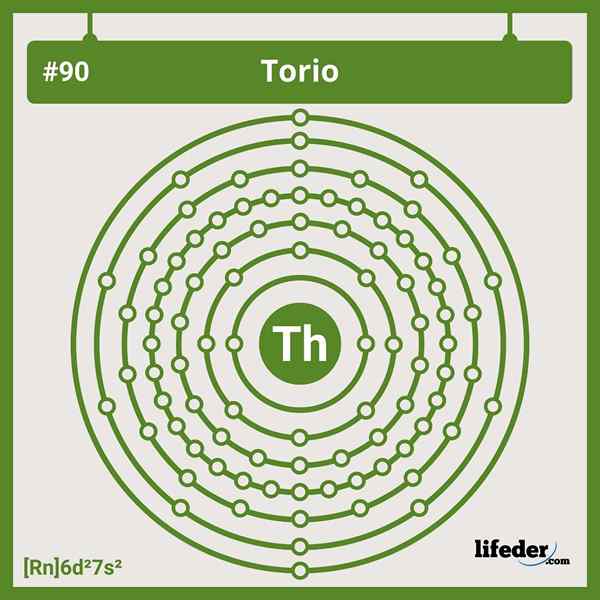 Elektroniske toriuminnstillinger
Elektroniske toriuminnstillinger Den forkortede elektroniske konfigurasjonen for thorium er som følger:
[RN] 6D2 7s2
Å miste sine fire Valencia -elektroner forvandles til THR -kationen4+. Legg merke til at til tross for at de er en skuespill, mangler den elektroner i sine 5F orbitaler, i motsetning til de andre aktinidene.
Kan tjene deg: SpredningsfaseÅ skaffe
Det viktigste mineralet som brukes til å oppnå thorium er monacitten. Det første trinnet er dets separasjon fra dets primære forekomst: Pegmatita. Alkalinotrous metaller Karbonater elimineres fra pegmatitten ved reaksjon av deres fragmenter med hydrogenklorid.
De resulterende fragmentene blir kalsinert og filtrert, og deretter gjennomgår en magnetisk separasjon. Dermed oppnås et sandsmateriale av monacita. Denne sanden blir utsatt for en fordøyelse på 93%svovelsyre, ved en temperatur fra 210 til 230 ° C, og i flere timer. Den dannede syreoppløsningen blir senere fortynnet med vann ti ganger volumet.
Monacitas forblir synker til bunnen, mens thorium og de andre elementene i sjelden jord flyter i syreforberedelse. PH til 1 justeres.3, som produserer nedbøren av thorium som fosfat, mens resten av det sjeldne landet i suspensjon forblir i løsning.
For øyeblikket blir separasjon og rensing utført ved hjelp av flytende løsningsmidler, for eksempel hyllest fosfat i Queroseno.
Torio -metall kan forekomme i kommersielle mengder ved metallotermisk reduksjon i totrafluoruro de Torio (THF4) og Torio -dioksid (tho2), eller ved elektrolyse av thorium tetraklorid (THCL4).
applikasjoner
Thorium har hatt mange applikasjoner, hvorav mange har blitt forkastet siden 1950 -tallet, fordi den radioaktive karakteren utgjorde en helserisiko.
Industriister
Legeringer
Thorium har blitt legert med wolfram som elektrode i TIG -sveisingen (wolfram inert gass), som utgjør 2% av legeringen.
I små mengder er Torio blitt tilsatt til wolframfilamenter for å redusere krystalliseringen, og dermed tillate utslipp av elektroner å lavere temperaturer. Tungsten-Torio-ledninger har blitt brukt i elektroniske rør og i elektrodene til røntgen- og likeretterørene rør.
Torio -dioksid har blitt brukt i wolframbuesveising, siden wolframresistens mot høye temperaturer av metallelektroder øker. Imidlertid er den erstattet i denne applikasjonen av Circumlisher, Cerio eller Lantano Oxides.
Kan tjene deg: hvor kommer plast fra? Historie og typerLyn
Totrafluoruro de Torio, derimot, har blitt brukt som materiale for å redusere refleksene i multicapa optiske belegg, som er gjennomsiktige til lys med en bølgelengde mellom 0.350 til 1.2 um. Torio -salt er imidlertid erstattet i denne bruken av Tetrafluoruro de Lantano.
Torio -dioksid har blitt brukt i lysbelysningen, for å avgi et strålende lys som tilsvarer synlig lys. Selv om thorium fremdeles brukes i denne applikasjonen, har den delvis blitt erstattet av ITE.
Ildfaste materialer
Thorium har også blitt brukt til utdyping av ildfaste materialer for den metallurgiske industrien og i keramiske crisols for undervisnings- og forskningslaboratorier.
Atomreaktorer
Torio-232 brukes i kjernefysiske reaktorer for å fange sakte filmnøytroner, siden det blir forvandlet til uran-233. Dette radioaktive elementet er fysisk og brukes til energiproduksjon.
Utviklingen av atomreaktorer basert på Torio-32 har vært treg, og skapt den første reaktoren med denne egenskapen i Indian Point Energy Center, som ligger i Buchanan USA, i 1962 år 1962. Torio-232 kjernefysiske reaktorer avgir ikke plutonium, noe som gjør dem til mindre forurensninger.
Referanser
- Shiver & Atkins. (2008). Uorganisk kjemi. (Fjerde utgave). Mc Graw Hill.
- Wikipedia. (2020). Thorium. Hentet fra: i.Wikipedia.org
- National Center for Biotechnology Information (2020). Thorium. Pubchem Comunund sammendrag for CID 23974. Gjenopprettet fra: Pubchem.NCBI.NLM.NIH.Gov
- Dr. Doug Stewart. (2020). Thoriumelement fakta. Gjenopprettet fra: Chemicool.com
- Redaktørene av Enyclopaedia Britannica. (2020). Thorium. Gjenopprettet fra: Britannica.com
- Lentech b.V. (2020). Thorium. Gjenopprettet fra: Lentech.com
- Rachel Ross. (1. mars 2017). Fakta om thorium. Gjenopprettet fra: Livescience.com
- Advameg. (2020). Thorium. Gjenopprettet fra: ChemistryExplaed.com

