Transformasjoner av materie
- 3652
- 411
- Dr. Andreas Hopland
 Transformasjonene av materie er de transformasjonene som det lider uten å endre sammensetningen. For eksempel forblir vann i sin væske, fast (is) eller brus (damp) vann vann
Transformasjonene av materie er de transformasjonene som det lider uten å endre sammensetningen. For eksempel forblir vann i sin væske, fast (is) eller brus (damp) vann vann Hva er transformasjonene av materie?
Transformasjonene av materie er endringene som dette lider uten at sammensetningen endrer seg. Det vil si at saken blir transformert når det går gjennom fysiske og kjemiske endringer.
Eksempler på fysiske forandringer er isdannelsen når temperaturen går ned, dugg på bladene som vises om morgenen, utvidelsen av gjenstandene når de blir oppvarmet og magnetiseringen av en kropp.
For sin del er oksidasjon av skruer og negler en kjemisk endring, siden oksyd er et stoff som er forskjellig fra det opprinnelige jernet. I alle fall er endringer i energi nødvendige slik at disse transformasjonene finner sted.
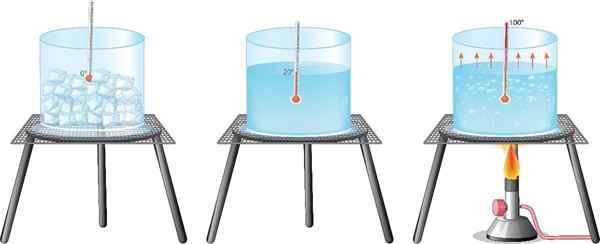
Iskransformasjon er en tilstandsendring der vann stivner, men det er flere muligheter. Saken forekommer i naturen og i laboratoriet i forskjellige stater, hvorav gass, væske og faststoff er de tre vanligste, i det minste under jordiske forhold.
Men siden saken endrer seg, har forskere møtt flere stater, av en noe eksotisk karakter, på eksperimentelt og teoretisk grunnlag.
Det kan bekreftes at det er fem grunnleggende tilstander av materie:
- Fast
- Væske
- Gass
- Plasma
- Bose-Einstein kondensat
Av disse er de tre første stabile i forholdene til planeten vår, mens de to siste krever teknologiske midler for å oppstå, selv om de i universet er hyppige. Plasma er faktisk den vanligste tilstanden av materie i kosmos.
De grunnleggende tilstandene for materie
Under jordens trykk og temperaturforhold presenteres materie normalt i tre stater: fast, væske og gass, mens plasma- og kondensattilstandene til Bose-Einstein oppnås under forskjellige forhold, som kan oppnås i laboratoriet.
Kan tjene deg: ukonvensjonelle tiltakFor å forklare hvorfor, er det nødvendig å huske at saken er sammensatt av partikler, koblet gjennom krefter, både attraktive og frastøtende. Attraksjonskrefter, som navnet tilsier, har en tendens til å sette sammen partiklene, mens de frastøtende har motsatt effekt.
Faststoffer, væsker og gasser
Når tiltrekningskreftene råder mellom partiklene, forblir de nær hverandre, sammen i mer eller mindre faste stillinger, og gir opphav til faste stoffer. Partiklene kan vibrere, men ikke forlate sin posisjon i det faste stoffet, derfor opprettholder dette en definert form og volum.
I Væsker, Attraksjonskrefter lar partikler fortsette i nærheten, men er mindre intense enn i faste stoffer ved å gi dem muligheten til å "skli" hverandre på en viss måte. Av denne grunn tilpasser væsker formen til beholderen som inneholder dem, men opprettholder deres faste volum.
Til slutt, i Gasser, Attraktive krefter er enda svakere, overveiende frastøtningskrefter. Dette gjør at partiklene forblir godt borte fra hverandre, og med mye mer bevegelsesfrihet. Av denne grunn utvides gassene til volumet som er tilgjengelige helt okkuperer.
Bose-Einstein kondensat og kondensat
Ved tilstrekkelig oppvarming av gass, skiller ioner og elektroner i en prosess som kalles ionisering, På denne måten a plasma på laboratoriet. Plasmatilstanden er ikke lett å se naturlig nær jorden, men den kan sees fra den i det nordlige og sørlige lyset.
Dette vakre naturfenomenet oppstår når partiklene i solvinden, et ganske diffust plasma, påvirker jordens atmosfære, ioniserende.
I den andre enden av skalaen, avkjøling mye, rett over det absolutte null, vises en ny tilstand av materie der de fleste partikler er i den grunnleggende tilstanden, som er den laveste energien.
Det kan tjene deg: Det viktigste aspektet ved liten vitenskap, stor vitenskap og teknovitenskapDenne tilstanden av materie kalles Bose-Einstein kondensat, av fysikerne Satyendra Bose og Albert Einstein, som spådde deres eksistens i 1924.
Mange år senere, i 1995, klarte flere forskere å føre svært utvannede gasser til denne tilstanden, en enkel oppgave, med tanke på at temperaturer av bare nano-kelvin er nødvendig over det absolutte null.
Tilstandsendringer i saken
I naturen er det veldig vanlig at saken går fra en stat til en annen. Normalt skyldes disse fysiske endringene variasjoner i trykk og temperatur, avledet fra økningen eller reduksjonen i partikler energi.
Når termisk energi tilsettes et materiale, øker den kinetiske energien til dens partikler, og reduserer attraksjonskraften som holder dem i samhold. Hvis materialet var i fast tilstand, kan det gå til flytende tilstand, eller til og med gå direkte til gassformig tilstand.
Tvert imot, fjerning av nok termisk energi, er det mulig å gjøre et gassformig materiale transformasjon til væske, eller at det går fra væske til fast. I alle fall endres ikke sammensetningen av stoffet.
Det mest kjente eksemplet for alle er vann: det er velkjent at en del av flytende vann blir forvandlet til damp når det kokes, mens det går til iskjøling til en fryser.
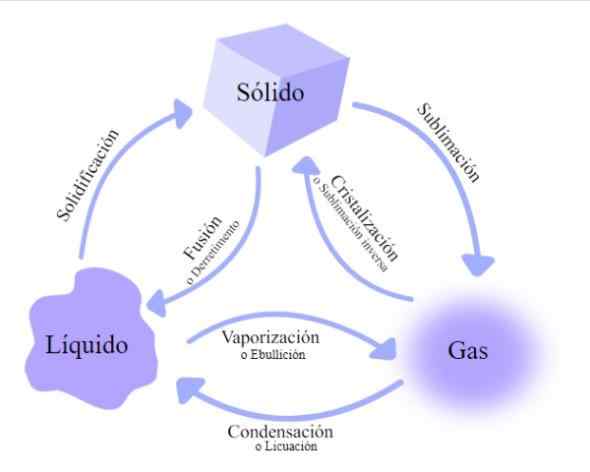 Endringer i tilstanden til materie. Kilde: Wikimedia Commons
Endringer i tilstanden til materie. Kilde: Wikimedia Commons Det er flere valutakurser som materien passerer, klassifisert i henhold til om termisk energi øker eller reduseres:
- Progressiv, De finner sted når materialet absorberer termisk energi.
- Regressiv, Det er de som oppstår når materialet gir energi.
Progressive transformasjoner
Blant de forskjellige progressive transformasjonene som foregår i saken ved å tilsette energi, er:
Fusjon
Endring som oppstår når materialet går fra den faste fasen til sin flytende fase. For eksempel ved å smelte en isblokk eller varme eller vokse i en panne.
Fordampning
I dette tilfellet blir saken transformert av flytende tilstand til gassformig tilstand.
Kan tjene deg: MetodikkFordampning forekommer på to måter:
- Kokende, foregår når materialet når sitt Kokende temperatur, På denne måten er energi nok til å overvinne intermolekylære krefter som holder partikler i flytende tilstand. Hvert stoff har en karakteristisk koketemperatur, med et visst trykk.
- Fordamping, Bare overfladiske partikler endrer tilstand, fordi materialet ikke er på den temperaturen som er nødvendig for å koke i koke. Det mest kjente eksemplet er fordampning av vann som er igjen i en beholder, ved romtemperatur.
Flyktighet
Ringte også sublimering, Det foregår når materialet konverterer direkte fra gass faststoff, uten å gå gjennom væskefasen.
For eksempel er tørris karbondioksid2 flyktig ved romtemperatur. Naftalen, som brukes til å beskytte insektklær, går sakte fra å være solid til å være en gass.
Ionisering
Det er passering av en plasmagass.
Regressive transformasjoner
Er transformasjonene forårsaket av nedgangen i partiklene termisk energi. Blant dem er:
Størkning
Det er endring av materie fra flytende tilstand til det faste stoffet ved avkjøling, som det skjer når du legger vann i fryseren. Prosessen skyldes at stoffet gir energi til det kalde miljøet, og danner is.
Kondensasjon
Det oppstår når den går fra gassformig tilstand til væskefasen, som med vanndampen i luften, når du tar kontakt med den kalde overflaten på bilen sin frontrute.
Flytende
Det er transformasjonen av materie når du går fra gass til væske, som det skjer, avkjølende ammoniakk eller karbondioksid med høyt trykk.
Inverse sublimering
Dette er passering av materie i en gassformig til fast tilstand, som med den gassformige jod som kolliderer mot en kald overflate, noe. Det er også kjent som krystallisering.
Desionisering
Endring av plasmatilstand til den gassformige tilstanden.
Referanser
- Chang, R. (2013). Kjemi. 11va. Utgave. McGraw Hill Education.
- Giancoli, d. (2006 =. Fysikk: Prinsipper med applikasjoner. 6. Ed Prentice Hall.
- Materie og dens egenskaper. Gjenopprettet fra: Elbibliote.com.
- Opentax. Kjemi. Hentet fra: OpenStax.org.
- Shipman, J. (2009). En introduksjon til fysisk vitenskap. Tolvte utgave. Brooks/Cole, Cengage Editions.

