Voltamperometri
- 4191
- 484
- Thomas Karlsen
 Voltamperometry er en elektrokjemisk metode som måler strømmen til en elektrode
Voltamperometry er en elektrokjemisk metode som måler strømmen til en elektrode Hva er voltamperometri?
De voltamperometri Det er en elektroanalytisk teknikk som bestemmer informasjon fra en kjemisk eller analytart fra de elektriske strømningene som genereres av variasjonen av et anvendt potensial. Det vil si at den potensielle E (V) anvendt, og tiden (t), er de uavhengige variablene; Mens strømmen (a), den avhengige variabelen.
Den kjemiske arten skal normalt være elektroaktiv. Dette betyr at det må tape (oksidere) eller vinne (redusere) elektroner. For reaksjonen for å sette i gang, må arbeidselektroden gi det nødvendige potensialet teoretisk av Nernst -ligningen.
Denne metoden er mye brukt i uorganisk, biokjemi og fysisk kjemi, spesielt for å analysere oksidasjons-, reduksjons- eller adsorpsjonsprosesser, blant andre.
Hvordan voltamperometri fungerer?
Voltamperometry ble utviklet takket være oppfinnelsen av Nobelkjemi i 1922 Nobel, Jaroslav Heyrovsky (1890-1967). I den blir kvikksølvdråpeelektroden (EGM) stadig fornyet og polarisert.
De analytiske manglene ved denne metoden på den tiden ble løst med bruk og utforming av andre mikroelektroder. Disse varierer veldig fra materiale, fra kull, edle metaller, diamant og polymerer, selv i design, plater, sylindere, ark; Og i tillegg, på den måten de samhandler med løsningen: stasjonær eller roterende.
Alle disse detaljene er ment1). Dette er proporsjonalt med konsentrasjonen av analytten, og halvparten av kraften E (E (E1/2) for å nå halvparten av denne strømmen (i1/2) er karakteristisk for arten.
Så bestemme verdiene til e1/2 I kurven der strømmen oppnådd med variasjonen av E er graf, kalt Voltamperaogram, Tilstedeværelsen av en analyt kan identifiseres. Det vil si at hver analyt, gitt forholdene i eksperimentet, vil ha sin egen verdi av e1/2.
Kan tjene deg: ekvivalenspunktVoltamperometrisk bølge
I voltamperometri jobber vi med mange grafer. Den første er kurven E vs. T, som lar deg overvåke potensielle forskjeller som brukes som en funksjon av tid.
Men samtidig registrerer den elektriske kretsen C -verdiene produsert av analytten når du mister eller får elektroner i nærheten av elektroden.
Fordi elektroden er polarisert, kan mindre analyt spres fra barmen til løsningen på den. For eksempel, hvis elektroden har en positiv ladning, art x- Han vil bli tiltrukket av dette og vil lede ham for bare elektrostatisk attraksjon.
Men x- er ikke alene: det er andre ioner til stede i miljøet ditt. Noen kationer m+ De kan hindre veien til elektroden ved å lokalisere den i "klynger" av positive ladninger; og også anioner n- De kan bli stjålet rundt elektroden og forhindre x- Jeg kommer til ham.
Summen av disse fysiske fenomenene fører til at strømmen går tapt, og dette er observert i C vs. E og dens form som ligner på en S, kalt sigmoidform. Denne kurven er kjent som voltamperometrisk bølge.
Instrumentering
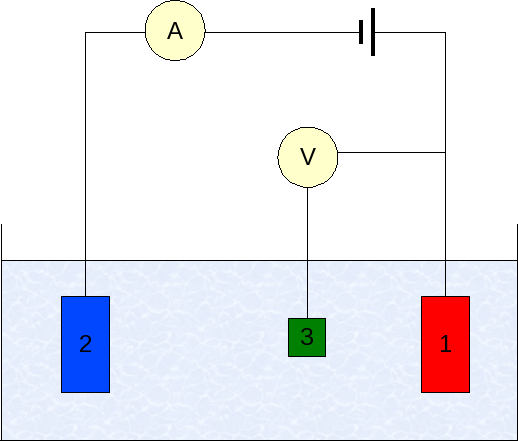 Elektroder i voltamperometri. Kilde: Wikimedia Commons
Elektroder i voltamperometri. Kilde: Wikimedia Commons Instrumenteringen av voltamperometri varierer i henhold til analytten, løsningsmidlet, typen elektrode og påføring. Men de aller fleste av dem er basert på et system som består av tre elektroder: ett av arbeidet (1), hjelpe (2) og referansen (3).
Hovedreferanseelektroden som brukes er Calomenanos -elektroden (ECS). Dette, sammen med arbeidselektroden, gjør det mulig å etablere en potensiell forskjell ΔE, siden potensialet til referanseelektroden forblir konstant under målinger.
Kan tjene deg: selen: historie, egenskaper, struktur, innhenting, brukPå den annen side er hjelpeelektroden ansvarlig for å kontrollere belastningen som går til arbeidselektroden, for å opprettholde den innenfor de akseptable verdiene. Den uavhengige variabelen, den anvendte potensielle forskjellen, er den som er oppnådd ved summen av potensialene til arbeidselektrodene og referansen.
Typer voltamperometri
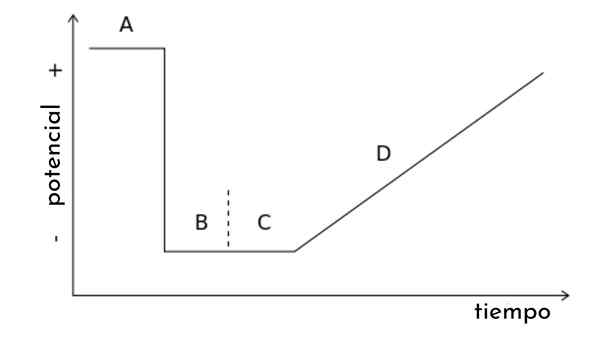
I bildet av artikkelen vises en graf. t, også kalt potensiell bølge for lineær skanningsvoltamperometri.
Det kan sees at når tiden går, øker potensialet. På sin side genererer dette sveipet en svarkurve, eller Voltamperaogram C vs. E, hvis form vil være sigmoid. Et poeng vil komme der uansett hvordan det øker, vil det ikke være en økning i strømmen.
Andre typer voltamperometri kan utledes fra denne grafen, og endre den potensielle bølgen. t av plutselige potensielle pulser etter visse mønstre. Hvert mønster er assosiert med en type voltamperometri, og omfatter sin egen eksperimentelle teori og forhold.
Puls voltamperometri
I denne typen voltamperometri kan du analysere blandinger av to eller flere analytter hvis e e1/2 er veldig nær hverandre.
Dermed en analyt med E1/2 av 0.04V kan identifiseres i selskap med en annen med en e1/2 av 0.05V. Mens i lineær skanning voltamperometri, må forskjellen være større enn 0.2V.
Derfor er det større følsomhet og lavere deteksjonsgrenser; det vil si at analytter kan bestemmes ved veldig lave konsentrasjoner.
Potensielle bølger kan ha lignende mønstre som trapper, skrå trapper og trekanter. Det siste tilsvarer syklisk voltamperometry (CV).
Kan tjene deg: begrensende og overdreven reagensI CVen et potensial og anvend på en måte, positivt eller negativt, og deretter, med en viss verdi av E i en tid, blir det samme potensialet, men i motsatt forstand brukes på nytt. Når du studerer de genererte voltampeogrammer, avslører maksimumene tilstedeværelsen av mellommenn i en kjemisk reaksjon.
Redisolution Voltamperometry
Dette kan være av den anodiske eller katodiske typen. Den består av elektrodeponering av analytten på en kvikksølvelektrode. Hvis analytten er et metallion (som CD -en2+), vil et amalgam bli dannet; Og hvis det er en anion (som moo42-), et uoppløselig kvikksølvsalt.
Deretter blir potensielle pulser brukt for å bestemme konsentrasjonen og identiteten til elektrodeposarten. Dermed er amalgamet Redisuelve, akkurat som kvikksølvsalter.
Voltamperometri -applikasjoner
- Anodisk redisolusjon Voltamperometri brukes til å bestemme konsentrasjonen av væskedisserte metaller.
- Det gjør det mulig å studere kinetikken til redoks eller adsorpsjonsprosesser, spesielt når elektrodene er modifisert for å oppdage en spesifikk analyt.
- Den teoretiske basen har tjent for fremstilling av biosensorer. Med disse kan tilstedeværelsen og konsentrasjonen av biologiske molekyler, proteiner, fett, sukker, etc. bestemmes.
- Til slutt oppdager det deltakelse av mellommenn i reaksjonsmekanismene.
Referanser
- González m. (2010). Voltamperometri. Gjenopprettet fra: Kjemi.Laguia2000.com
- Kjemi og vitenskap (2011). Voltamperometri. Hentet fra: Thequimica Andlaciencia.Blogspot.com
- Quiroga a. (2017). Syklisk voltammetri. Gjenopprettet fra: Chem.Librettexts.org
- Samuel s. Kouves (s.F.). Voltammetriske teknikker. [PDF]. Tufts University. Gjenopprettet fra: brun.Edu
- Dag r. & Underwood a. Kvantitativ analytisk kjemi (Femte utg.). Pearson Prentice Hall.

