Aluminiumacetat (Al (CH3CO) 3) Struktur, egenskaper, bruk
- 1964
- 564
- Mathias Aas
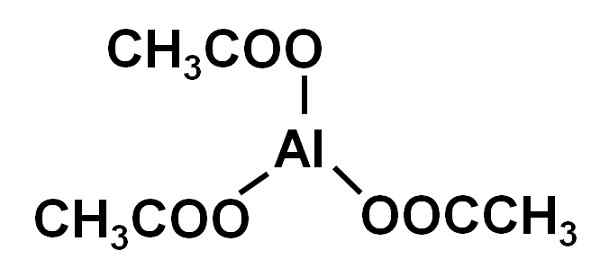
Han aluminiumacetat Det er en organisk forbindelse dannet av et aluminiumion til3+ og tre acetate ioner cho3COO-. Den kjemiske formelen er AL (Cho3Coo)3. Det er også kjent som aluminium triacetat. Det er et litt hygroskopisk og oppløselig vann som er fast i vann.
For å oppnå denne forbindelsen, må totalt vannfrie forhold brukes, det vil si vannfri3Coo)2.
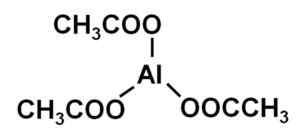 Aluminium triacetat AL (CH3Coo)3. Forfatter: Marilú Stea.
Aluminium triacetat AL (CH3Coo)3. Forfatter: Marilú Stea. Aluminiumacetatløsninger har antibakterielle og soppdrepende egenskaper, så siden det nittende århundre ble de brukt til å behandle infeksjoner spesielt av ørene.
Den mest kjente er Burows løsning, designet av en tysk lege. Imidlertid har bruken noen ganger drevet til skade på mellomøret.
Denne løsningen har også blitt brukt til å behandle hudproblemer som kløe og utbrudd. Det brukes til og med som solbrentløse beroligende.
Aluminiumacetat og dets derivater brukes til å oppnå veldig små strukturer eller partikler av aluminiumoksyd til2ENTEN3. Disse strukturene eller nanopartiklene kan være i form av blader, blomster eller nanorør.
[TOC]
Struktur
Aluminium triaseat dannes av en aluminiumskation til3+ og tre acetatanioner cho3COO-. Det er aluminiumsaltet av eddiksyre CH3COOH.
Aluminium er knyttet til acetatanioner gjennom oksygenet til disse. Med andre ord er det knyttet til tre oksygen. Disse fagforeningene er ioniske.
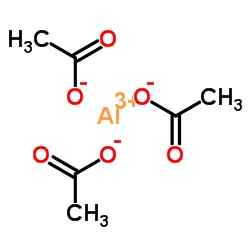 Ionisk struktur av aluminiumacetat. N4tr!UMBR [CC BY-S (https: // CreativeCommons.Org/lisenser/by-SA/4.0)]. Kilde: Wikimedia Commons.
Ionisk struktur av aluminiumacetat. N4tr!UMBR [CC BY-S (https: // CreativeCommons.Org/lisenser/by-SA/4.0)]. Kilde: Wikimedia Commons. Nomenklatur
- Aluminiumacetat
- Aluminium triacetat
- Aluminiumetanoate
- Burow Solution (engelsk oversettelse Burows løsning): Det er en aluminiumacetatløsning.
Egenskaper
Fysisk tilstand
Hvitt faststoff.
Molekylær vekt
204.11 g/mol
Løselighet
Løselig i vann.
Kjemiske egenskaper
I vandig løsning blir aluminiumtriaseat oppløst og har en tendens til å danne (OH) diacetat (CH)3COO) og noen ganger monoacetat på (OH)2(Ch3Coo). Alt avhenger av pH og mengden eddiksyre ch3Cooh til stede i løsningen.
Kan tjene deg: overflatespenning: årsaker, eksempler, anvendelser og eksperimenterAl (kap3Coo)3 + H2Eller ⇔ al (oh) (cho3Coo)2 + Ch3COOH
Al (kap3Coo)3 + 2 h2Eller ⇔ al (OH)2(Ch3COO) + 2 CH3COOH
Andre egenskaper
Aluminiumacetat er litt hygroskopisk, det vil si at det har en tendens til å absorbere luftvann.
Å skaffe
Aluminiumacetat oppnås fortrinnsvis under strengt vannfrie forhold, det vil si totalt vannfravær. Dette inkluderer også fravær av luft, da dette kan inneholde fuktighet.
En blanding av iseddiksyre CH varmes opp3COOH og eddikanhydrid (CH3Co)2Eller under slike forhold som tillater å eliminere alt det nåværende vannet. Til denne varme blandingen tilsettes aluminiumklorid ALCL3 Ashidro fast (uten vann).
Et hvitt fast stoff av Al (CH3Coo)3.
Alcl3 + 3 Ch3COOH → AL (CH3Coo)3 + 3 HCl
Det totale fraværet av vann er viktig for å unngå dannelse av aluminiummonoacetatsalter ved (OH)2(Ch3COO) og aluminiumdiacetat på (OH) (Cho3Coo)2.
Det kan også oppnås ved reaksjon av aluminiumhydroksid til (OH)3 og eddiksyre ch3COOH.
Bruker innen medisin
Øreinfeksjoner
Aluminiumacetat har blitt brukt siden det nittende århundre for å behandle otitis, som er en betennelse i det ytre eller mellomstore øret generelt ledsaget av infeksjon. Bruken skyldes dens antibakterielle og soppdrepende effekt.
Det har blitt brukt i form av en 13%aluminiumacetatløsning, opprinnelig utviklet av den tyske legen Karl August von Burow, så det kalles Burow Solution.
Det er funnet som hemmer veksten av mikroorganismer som ofte finnes i middels eller ekstern otitis, slik som Pseudomonas aeruginosa, han Staphylococcus aureus og Proteus mirabilis.
 Øreinfeksjoner har blitt behandlet i mange år med aluminiumacetat. Forfatter: Ulrike Mai. Kilde: Pixabay.
Øreinfeksjoner har blitt behandlet i mange år med aluminiumacetat. Forfatter: Ulrike Mai. Kilde: Pixabay. Imidlertid er det de som rapporterer at disse løsningene kan være skadelige for øret. Noen studier på dyr undersøker deres giftige effekter for øret, men har rapportert motstridende resultater.
Det kan tjene deg: sinkhydroksid (Zn (OH) 2)Enkelte forskere anbefaler å ikke bruke aluminiumacetat når trommehinnen er perforert, siden det har blitt observert at det utøver en inflammatorisk effekt på mellomøret.
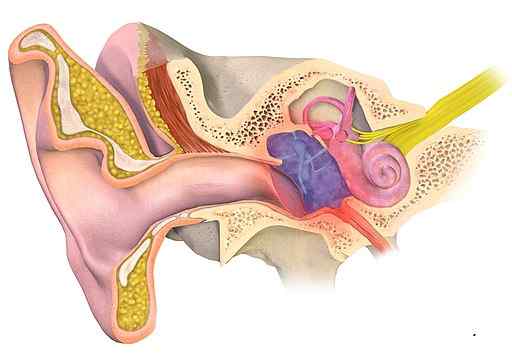 Det er ikke praktisk å behandle otitis media (blåaktig sone i figuren) med aluminiumacetat. Bruceblaus [CC By-SA (https: // CreativeCommons.Org/lisenser/by-SA/4.0)]. Kilde: Wikimedia Commons.
Det er ikke praktisk å behandle otitis media (blåaktig sone i figuren) med aluminiumacetat. Bruceblaus [CC By-SA (https: // CreativeCommons.Org/lisenser/by-SA/4.0)]. Kilde: Wikimedia Commons. Hudsykdommer
Burows løsning brukes som et antiseptisk middel, snerpende og som en aktuell løsning for å behandle alvorlige utbrudd, dermatitt, betennelse, kløe, brenning og solbrenthet. Utøver en beroligende og reduserende effekt av irritasjoner.
 Noen ganger kan solbrentheter behandles med en aluminiumacetatløsning. Forfatter: Tumisu. Kilde: Pixabay.
Noen ganger kan solbrentheter behandles med en aluminiumacetatløsning. Forfatter: Tumisu. Kilde: Pixabay. Andre bruksområder
Aluminium triaseat og dets derivater brukes til mange kvalitative og kvantitative kjemiske eksperimenter.
Et derivat av aluminium triacetat, diacetat ved (OH) (CH3Coo)2 Også kalt aluminiumhydroksydacetat, det brukes som en forløper for å oppnå nanostrukturer for gamma-aluminiumoksyd (y-al2ENTEN3).
I dette tilfellet betyr forløper at fra aluminiumdiacetatet (oppnådd på en bestemt måte) er y-Al-nanostrukturene utarbeidet2ENTEN3, Og dette oppnås ved å varme det opp ved veldig høye temperaturer.
Nanostrukturer er veldig små partikler som bare kan observeres gjennom spesielle mikroskop som elektroniske mikroskop. Med aluminiumacetat som forløper er nanostrukturer av y-til blitt oppnådd2ENTEN3 I likhet med blader, blomster, fibre og til og med nanorør.
 Alumina nanofriboer kan oppnås ved bruk av et aluminiumacetatderivat. Aleksei TR [CC By-SA (https: // CreativeCommons.Org/lisenser/by-SA/4.0)]. Kilde: Wikimedia Commons.
Alumina nanofriboer kan oppnås ved bruk av et aluminiumacetatderivat. Aleksei TR [CC By-SA (https: // CreativeCommons.Org/lisenser/by-SA/4.0)]. Kilde: Wikimedia Commons. Avbryt bruk
På begynnelsen av det 20. århundre ble aluminiumacetat brukt som matbevarende som hermetiske pølser.
En aluminiumacetatoppløsning ble fremstilt ved å blande aluminiumsulfat til2(SW4)3, Caco kalsiumkarbonat3, Eddiksyre Ch3COOH og AGUA H2Eller, og lagt til mat.
Når denne løsningen kommer i kontakt med kjøtt, er aluminium festet i bestanddelene av den i form av en forbindelse som er uoppløselig i kokende vann, men at i magesaft løses opp med omtrent 80%.
Det kan tjene deg: Bromousyre (HBRO2): Fysiske og kjemiske egenskaper, og brukerAllerede i 1904 ble det kjent at aluminiumsalter forsinker fordøyelsen, både i mage og tarmer. Derfor er det en ikke -følsom praksis å legge til aluminiumacetatløsninger til hermetikk.
 Tidligere ble aluminiumacetat brukt som konserveringsmiddel for hermetisert pølse. Det er foreløpig kjent at det er skadelig og at den ikke lenger brukes til det. Forfatter: Changglc. Kilde: Wikimedia Commons.
Tidligere ble aluminiumacetat brukt som konserveringsmiddel for hermetisert pølse. Det er foreløpig kjent at det er skadelig og at den ikke lenger brukes til det. Forfatter: Changglc. Kilde: Wikimedia Commons. Skadelige effekter
Siden det er studier som rapporterer om at aluminiumacetat kan være giftige, er det blitt utført tester der aluminiumacetat er blitt injisert i laboratoriemus.
Resultatene indikerer at denne forbindelsen gir skade på ryggraden i disse dyrene, samt skade på kromosomene og sædene til dyrene. Med andre ord er det genotoksisk.
Dette advarer om mulige helsefare som kan forårsake overeksponering for aluminiumacetat og omsorgen som må tas under bruk.
Referanser
- Mac-kay chace, og. (1904). Bruken av grunnleggende aluminiumacetat som konserveringsmiddel i pølse. Journla of the American Chemical Society 1904, 26, 6: 662-665. Gjenopprettet fra puber.ACS.org.
- Hette, g.C. og ihde, a.J. (1950). Aluminiumacetater og propionater - Forberedelse og sammensetning. Journal of the American Chemical Society 1950, 72, 5: 2094-2095. Gjenopprettet fra puber.ACS.org.
- Pitaro, J. et al. (2013). Ototoksisitet av aluminiumacetat/benzenethonium klorid otisk løsning i chinchilla -dyremodellen. Laryngoscope, 2013; 123 (10): 2521-5. NCBI kom seg.NLM.NIH.Gov.
- Thorp, m.TIL. et al. (2000). Burows løsning i behandlingen av aktivt mye kronisk supuritive otitis media: Bestemme en effektiv fortynning. Journal of Laryngology & Otology, juni 2000, Vol. 114, s.432-436. NCBI kom seg.NLM.NIH.Gov.
- D'Ouza, MR.P. et al. (2014). Vurdering av genotoksi av studie achetat i benmarg, mannlige kimceller og fosterleverceller fra sveitsiske albino mus. Mutation Research 766 (2014) 16-22. NCBI kom seg.NLM.NIH.Gov.
- Basal, og. et al. (2015). Effektene av aktuelle Burows og Castellanis løsninger på Middle Ear Mucosa av rotter. J. Int adv otol 2015; 11 (3): 253-6. Gjenopprettet fra Advancedotology.org.
- ELLER.S. National Library of Medicine. (2019). Stilling acetat. Gjenopprettet fra Pubchem.NCBI.NLM.NIH.Gov.
- Buttaravoli, p. Og Leffler, S.M. (2012). Solbrenthet. Hva å gjøre. I mindre nødsituasjon (tredje utgave). Gjenopprettet fra Scientedirect.com.
- Thompson, e. og Kalus, til. (2017). Actte hudreaksjoner og bakterieinfeksjoner. Behandling. I Travel and Tropical Medicine Manual (femte utgave). Gjenopprettet fra Scientedirect.com.
- Kim, t. et al. (2010). Morfologi Kontrollerbar syntese av gamma-alumin. Crystal Growth & Design, Vol.10, nei. 7, 2010, s.2928-2933. Gjenopprettet fra puber.ACS.org.
- Rajala, J.W. et al. (2015). Kjerne-skall elektrospun hul aluminiumoksyd keramiske fibre. Fibre 2015, 3, 450-462. MDPI kom seg.com.
- « Komponenter i det geografiske rommet som er oppført og hvordan de forholder seg
- Fosforoksyd (V) Struktur, egenskaper, innhenting, bruk, risiko »

