Isoamilo struktur, egenskaper, syntese og bruker acetat

- 2845
- 11
- Thomas Karlsen
Han Isoamiloacetat Det er en ester hvis molekylære formel er cho3COO (kap2)2Ch (Ch3)2. Ved romtemperatur består den av en fet, klar, fargeløs, brennbar og flyktig væske. Faktisk er det en for flyktig og velduftende ester.
Dets viktigste kjennetegn er å ta farvel med en lukt som bidrar til aromaen av mange frukt, spesielt den av bananer eller banan. Også denne siste frukten utgjør en av dens naturlige kilder par excellence.
 Bananer, hvis karakteristiske aroma skyldes isoamilo -acetat. Kilde: Pixabay.
Bananer, hvis karakteristiske aroma skyldes isoamilo -acetat. Kilde: Pixabay. Derfra navnet på bananolje som gis til en isoamilacetatoppløsning, eller en blanding av isomylacetat med nitrocellulose. Forbindelsen er mye brukt som en smak av mat, is og søtsaker.
I tillegg brukes det til utdyping av dufter med forskjellige jobber. Det er også et løsningsmiddel som brukes i ekstraksjon av metaller og organiske forbindelser som eddiksyre.
Isoamiloacetat er resultatet av sterifisering av isoamylalkohol med eddiksyre. I organisk kjemi som underviser laboratorier, representerer denne syntesen en interessant opplevelse for å implementere forestringen, mens du oversvømmer laboratoriet med bananduft.
[TOC]
Isoamilo acetatstruktur
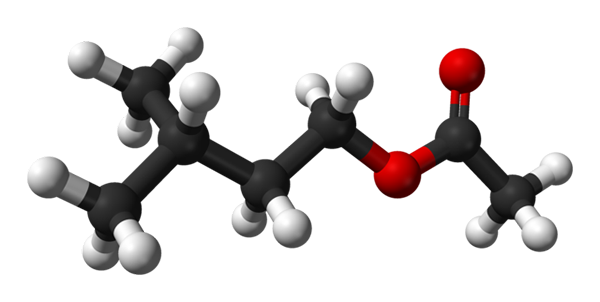 Isoamilo acetatstruktur. Kilde: Ben Mills [Public Domain]
Isoamilo acetatstruktur. Kilde: Ben Mills [Public Domain] I det øvre bildet har du molekylstrukturen til isoamilacetatet ved hjelp av en kuler og barer -modell. De røde kulene tilsvarer oksygenatomer, spesielt de som identifiserer denne forbindelsen som ester; dens del av eter, r-o-r, og karbonylgruppen, c = o, og har deretter den strukturelle formelen r'Coor.
Til venstre, r', Du har den isopentile alkliske radikale, (Cho3)2Chch2Ch2; Og til høyre, r, til metylgruppen, som 'acetatet' med navnet på denne esteren skyldes. Det er en relativt liten ester, i stand til å samhandle med de kjemiske reseptorene i lukten av nesen, noe som forårsaker signaler som hjernen tolker som en duft.
Kan tjene deg: forgrenede alkanerIntermolekylære interaksjoner
Isoamilacetatmolekylet i seg selv er fleksibelt; Men den isopentilradikal.
Disse to oksygenene kan ikke akseptere hydrogenbroer; Strukturelt sett har ikke molekylet hvordan du donerer dem. Overfor de avbrutte dipolene kan isoamilacetat samhandle intermolekylært gjennom London -spredningskrefter; som er direkte proporsjonale med molekylmassen.
Dermed er det molekylmassen til esteren som er ansvarlig for at molekyler danner en væske med et høyt kokepunkt (141 ° C). På samme måte er det ansvarlig for det faste dekket til en temperatur på -78 ° C.
Bananskuft
Dens intermolekylære krefter er så svake at væsken er flyktig nok til å gjennomsyre omgivelsene med bananer lukter. Interessant nok kan den søte lukten av denne esteren endre seg hvis antallet karbonatomer er redusert eller økt.
Det vil si at hvis han i stedet for å ha seks alifatiske karbonatomer hadde fem (med den radikale isobutilen), ville lukten ligne den av bringebær; Hvis radikalen var secbutil, ville lukten bli lastet med spor av organiske løsningsmidler; Og hvis jeg hadde mer enn seks karbonatomer, ville lukten begynne å bli såpe og metallisk.
Egenskaper
Kjemiske navn
-Isoamiloacetat
-Isopentile etanoate
-3-metylbutilo-acetat
-Isopentilo -acetat
-Bananolje eller banan.
Molekylær formel
C7H14ENTEN2 eller Ch3COO (kap2)2Ch (Ch3)2
Molekylær vekt
130.187 g/mol.
Fysisk beskrivelse
Det er en fet, klar og fargeløs væske.
Lukt
Ved romtemperatur har den en intens og behagelig lukt av banan.
Smak
Den har en smak som ligner den som presenteres av pære og eple.
Kokepunkt
124,5 ºC.
Smeltepunkt
-78,5 ºC.
tenningspunkt
92 ºF lukket kopp (33 ºC); Kopp åpen 100 ºF (38 ºC).
Kan tjene deg: krystallinske faste stoffer: struktur, egenskaper, typer, eksemplerVannløselighet
2.000 mg/l a 25 ºC.
Løselighet i organiske løsningsmidler
Blandbar med alkohol, eter, etylacetat og amylalkohol.
Tetthet
0,876 g/cm3.
Damptetthet
4.49 (i luftforhold = 1).
Damptrykk
5,6 mmHg ved 25 ºC.
Selv -tisningstemperatur
680 ºF (360 ºC).
Goo
-1.03 CPOISE ved 8,97 ºC
-0,872 CPOISE ved 19,91 ºC.
Forbrenningsvarme
8.000 kalk/g.
Lukt terskel
Luft = 0,025 ul/l
Vann = 0,017 mg/l.
Brytningsindeks
1400 til 20 ° C.
Relativ fordampningshastighet
0,42 (i forhold til butylacetat = 1).
Dialektrisk konstant
4.72 til 20 ºC.
Oppbevaring
Isoamilo acetat er en brennbar og flyktig forbindelse. Derfor må det være kaldt i helt hermetiske beholdere, langt fra brennbare stoffer.
Syntese
Det produseres ved forestring av isoamylalkohol med iseddik, i en prosess kjent som Fishers estterifisering. Svovelsyre brukes vanligvis som katalysator, men også p-toluenosulfonsyre katalyserer reaksjonen:
(Ch3)2Ch-ch2-Ch2Ch2Oh + Ch3COOH => CH3Cooch2-Ch2-Ch2-Ch (Ch3)2
applikasjoner
Mat og drikke smakstilsetning
Det brukes til å gi en pæresmak i vann og sirup. Det brukes i Kina for å tilberede fruktsmaker, som jordbær, bjørnebær, ananas, pære, eple, drue og banan. Dosene som brukes er: 190 mg/kg i konditor; 120 mg/kg i kringle; 56 mg/kg i iskrem; og 28 mg/kg i brus.
Løsningsmiddel og fortynningsmiddel
Det er et løsningsmiddel for:
-Nitrocellulose og celluloid
-Vanntette lakker
-Estergummi
-Vinylharpiks
-Cummarona harpiks og ricinusolje.
Det brukes som et løsningsmiddel for krombestemmelse og brukes som et jern, kobolt og nikkelekstraksjonsmiddel. Det brukes også som et løsningsmiddel av oljemalerier og gamle lakker. I tillegg brukes det i utdypingen av neglelakk.
Denne esteren brukes som fortynningsmiddel i eddiksyreproduksjon. Olje brukes som råstoff i en oksidasjonsprosess som produserer en vandig oppløsning av eddiksyre og andre forbindelser, så som maursyre og propionsyre.
Kan tjene deg: Etylenglykol: egenskaper, kjemisk struktur, brukSom en løsningsmiddel og bærer av andre stoffer ble det brukt i begynnelsen av luftfartsindustrien for å beskytte stoffene mot luftvingene.
Dufter
-Det brukes som en atmosfære for å dekke over de dårlige luktene.
-Det brukes som parfyme i sko.
-For å bevise effektiviteten til antigasemasker, siden isoamilacetat har en veldig lav lukt terskel og ikke er veldig giftig.
-Det brukes i dufter som Chipre; den myke aromaen Osmanthus; Jacinto; og den sterke orientalske smaken, brukt i lave doser, lavere enn 1%.
Andre
Det brukes til utdyping av silke og kunstige perler, fotografiske filmer, vanntett og bronseringslakk. Det brukes også i tekstilindustrien innen farging og etterbehandling. Det brukes i tørr vask av kjoleartikler og tøymøbler.
I tillegg brukes isoamiloacetat i Rayon -utdyping, et syntetisk stoff; I penicillinekstraksjon, og som et standardkromatografistoff.
Risiko
Isoamilo -acetat kan irritere huden og øynene ved fysisk kontakt. Innånding kan forårsake neseirritasjon, hals og lunger. I mellomtiden kan eksponering for høye konsentrasjoner forårsake hodepine, døsighet, svimmelhet, svimmelhet, tretthet og besvimelse.
Langvarig kontakt med huden kan forårsake tørrhet og sprekker.
Referanser
- Bilbrey Jenna. (30. juli 2014). Isoamylacetat. Kjemi verden av Royal Society of Chemistry. Gjenopprettet fra: Chemistryworld.com
- Nasjonalt senter for bioteknologiinformasjon. (2019). Isoamylacetat. PubChem -database. Gjenopprettet fra: Pubchem.NCBI.NLM.NIH.Gov
- Wikipedia. (2019). Isoamylacetat. Hentet fra: i.Wikipedia.org
- Royal Society of Chemistry. (2015). Isoamylacetat. Chemspider. Gjenopprettet fra: Chemspider.com
- New Jersey Department of Health and Senior Services. (2005). Isoamylacetat. [PDF]. Gjenopprettet fra: NJ.Gov
- Kjemisk bok. (2017). Isoamylacetat. Gjenopprettet fra: ChemicalBook.com
- « 4 perioder med kjemi fra forhistorie til i dag
- Politiske taleegenskaper, typer, spørsmål og eksempler »

