Alanina -egenskaper, struktur, funksjoner, biosyntese
- 1973
- 113
- Jonathan Moe
De til jenta (Vinge) er en av de 22 kjente aminosyrene som utgjør strukturen til proteinene til alle organismer, fra bakterier til menn. Som organismen kan syntetisere, er dette klassifisert som en ikke -essensiell aminosyre.
Proteiner har en basisk eller primær struktur som består av en aminosyrekjede kalt polypeptidkjede, i disse kjedene er hver aminosyre dannet av et sentralt karbon kalt karbon α.
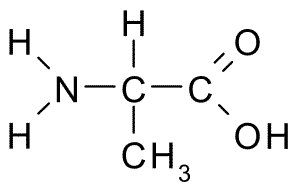
 Kjemisk struktur av alaninaminosyre (kilde: Borb, via Wikimedia Commons)
Kjemisk struktur av alaninaminosyre (kilde: Borb, via Wikimedia Commons) Α-karbonet blir sammen med fire grupper: en aminogruppe (-NH2), en karboksylgruppe (-COH), et hydrogenatom (-H) og en gruppe eller sidekjede (-R) som identifiserer hver aminosyre. I sidekjeden tar karbonatomer sekvensielt bokstavene ß, γ, Δ og ε.
Aminosyrer er klassifisert av polariteten i sidekjedene, og det er dermed hydrofobe og hydrofile polare aminosyrer som igjen kan være nøytrale, basiske og sure. Alanin er en hydrofob apolar aminosyre og er den enkleste aminosyren etter glycin og den mest tallrike i de fleste proteiner.
Alanin kan dannes i muskelen og transporteres til leveren, hvor den introduseres til den glukoneogene ruten, det vil si ruten for glukosedannelse fra ikke -glukosidiske stoffer. Alanin kan også syntetiseres i leveren gjennom katabolismen av tryptofan og uracil og kan forringes for å danne pyruvat.
Delta i syntesen av tryptofan, pyridoksin (vitamin B6) og kjøtt.
Det brukes som et kostholdstilskudd for å forbedre sportsprestasjoner og finnes naturlig i ku, svinekjøtt og fiskekjøtt, så vel som i melk og deres derivater og egg. Noen belgfrukter, frukt og nøtter er også rike på alanin.
[TOC]
Struktur
Det ble tidligere kommentert at alanin, som alle aminosyrer, har et α-karbon med fire grupper forenet til det, som R-gruppen A metylgruppe (-Ch3).
Derfor til kroppens pH (rundt 7.4) α-karbonet til alaninet er knyttet til en aminoprotongruppe (-NH3+), til en karboksylgruppe som har mistet et proton (-co-), til et hydrogen og en metylgruppe (-Ch3).
De fleste aminosyrene er ioniserbare til pH 7.0 Og geometrisk kan de ha isomerer, som er kjent som enantiomerer, som er spekulære bilder, som med høyre og venstre hånd.
Kan tjene deg: histokjemi: fundament, prosessering, fargingDeretter kan alle aminosyrer finnes som "chirale par" betegnet som henholdsvis d eller L (henholdsvis dextro og levo), i henhold til atomene som omgir karbon α.
Imidlertid alanin, som med mest aminosyre.
Denne aminosyren kan også bli funnet som ß-alanin, der aminogruppen er festet til dets β-karbon, det vil si til det første karbonet i sidekjeden.
Β-alanin finnes i pantotensyre (vitamin B5) og i noen naturlige peptider. D-alanin finnes i noen polypeptider som er en del av veggene i noen bakterieceller.
Gruppe R (Metilo, CH3)
Metylen til den alaninkjeden er et mettet hydrokarbon som gir den apolare hydrofobe karakteristikken til denne aminosyren. Denne egenskapen til alanin er vanlig med de andre aminosyrene i denne gruppen som glycin, valin, leucin og isoleucin.
Aminosyrene som utgjør gruppen av alifatiske er kjemisk nøytrale aminosyrer og spiller en veldig viktig rolle i dannelsen og vedlikeholdet av den tre -dimensjonale strukturen til proteiner siden de har en tendens til å reagere på hverandre unntatt vannet.
Disse aminosyrene, inkludert alanin, inneholder samme antall ioniserbare grupper med motsatte belastninger, slik at de ikke har nettbelastning og kalles "Zwitterions ".
Funksjoner
Som mest kjente aminosyrer brukes alanin i syntesen av peptider og proteiner generelt, og deltar i etableringen av polypeptidstrukturen og i den tertiære strukturen til noen proteiner.
En annen av de viktige funksjonene til alanin er å delta indirekte i glykemi -kontroll:
Det kan gi opphav til pyruvat og omvendt, det kan også nå leveren og bli glukose gjennom glukoneogenese for å bli oppdaget til sirkulasjon eller å bli brukt i glykogensyntese, etter behov etter behov som nødvendig.
Alanin deltar som ammoniumtransportør fra muskelen til leveren, siden den kan syntetiseres ved aminering fra pyruvat, transportere leveren og det blir transaminering ved transaminering.
Dette skjer samtidig med transformasjonen av a-zotoglutarat til glutamat, som kan komme inn i ureasyklusen og bli pyruvat.
Andre funksjoner
Denne aminosyren er uunnværlig for syntese av tryptofan og pyridoksin. Selv om det er kjemisk veldig lite reaktivt, kan alanin ha en anerkjennelse av underlag og enzymatisk reguleringsgjenkjenning.
Kan tjene deg: parafiletisk gruppeEn av funksjonene til ß-alanin er kostholdstilskuddet, ettersom det brukes som en ergogen hjelp av øvelsen. P-alanininntaket øker konsentrasjonen av kjøttfullt (et dipéptid dannet av ß-alanin og histidin) i skjelettmuskelen, og fungerer som "buffer".
Normalt bidrar ikke Fleshy nevneverdig til den totale bufferkapasiteten til muskelcellen, og dette skyldes dens lave konsentrasjon. Administrasjonen av ß-alanin øker denne konsentrasjonen og derfor bufferkapasiteten, så den forbedrer motstanden ved å redusere trettheten.
Biosyntese
Den viktigste syntesen av alanin i menneskekroppen skjer ved en reduktiv aminering av pyruvinsyre. Denne reaksjonen krever et enkelt enzymatisk trinn.
Pyruvatet gir karbonskjelettet og glutamatet gir aminogruppen som overføres til pyruvatet. Enzymet som katalyserer denne reversible reaksjonen er transaminase alanin.
Som et resultat av denne reaksjonen produseres alanin og α-Cetoglutarat. Alanin kan da være til stede i glukoneogenese, glykolyse og i Krebs -syklusen.
En annen kilde til alanin kommer fra nedbrytningen av tryptofan til acetyl-CoA. På denne ruten, når kinureninase-enzymet hydrolyserer ved 3-hydroxi-kinureninet dannes 3-hydroksy antranilat og alanin. Alanin frigjøres og 3-hydroksy antranilat følger den metabolske ruten.
Uracil -nedbrytning er en annen kilde til alanin. I dette tilfellet er det ß-alanin som kan følge flere metabolske veier, en av dem er å bli acetyl-CoA.
Nedbrytning
Generell prosess for nedbrytning av aminosyren
Aminosyrer lagres ikke som karbohydrater og fett, så de som frigjøres under nedbrytning av proteinnet.
På den annen side kan aminosyrer bli degradert og deres kullsyreholdige skjeletter kan brukes i kataboliske eller anabole reaksjoner.
Når aminosyrer blir nedbrutt, er overflødig nitrogen ammoniakkform, som er et giftig stoff som må elimineres og det første trinnet med nedbrytning av aminosyren er eliminering av nitrogen.
Hos pattedyr skjer denne nedbrytningen i leveren; Der blir all aminosyre som er i overkant og ikke kan brukes degradert.
Alaninforringelse
Alanin -nedbrytning skjer ved konvertering av alanin til pyruvat. Denne reaksjonen katalyseres av transaminase alanin og krever tilstedeværelse av a-zotoglutarat som en akseptor for aminogruppen og den påfølgende glutamatformasjonen; Det er en reversibel reaksjon.
Kan tjene deg: virulensfaktorerDisse alaninformasjonsreaksjonene fra pyruvat og alanin -nedbrytning for å danne pyruvat er en del av en syklus som involverer skjelettmuskel og lever.
Leveren tar glukose til muskler og muskler, gjennom glykolyse, omdanner glukose til pyruvat for å generere ATP; Denne pyruvatet kan komme inn i syntesen av alanin, som kan helles i den sirkulasjonsstrømmen og går tilbake til leveren som gjør det igjen pyruvat, som kommer inn i glukoneogenese for å danne glukose.
Om nødvendig blir syklusen gjentatt. I leveren genererer produksjonen av pyruvat fra alanin ammoniumioner som ser på glutamin og glutamat, og de kommer inn i ureasyklusen. Da elimineres urea av urin.
Alanin, glykin, cystein, serin og treonin er glykogene aminosyrer siden nedbrytningen deres kan gi opphav til pyruvat, a-zetoglutarat, succinyl-CoA, til fumarat eller oksalacetat, alle glukoneogenforløpere av glukose.
Mat rik på alanina
De viktigste kildene til aminosyrer er magert kjøtt, fisk, skalldyr, egg og meieriprodukter, men alanin finnes også i mange matvarer med planteopprinnelse. Eksempel på mat rik på alanina er:
- Kjøtt som ku, svinekjøtt, sauer, kylling, kalkun, kanin, fisk; Egg, melk og derivater.
- Tørre frukt som hasselnøtter, nøtter, kastanjer, mandler og peanøtter er alanina -kilder.
- Kokosnøtt, avokado, asparges, aubergine, kassava eller kassava, rødbeter, gulrot og søtpoteter.
- Belgfrukter som mais, bønner og erter.
- Korn som ris, rug, hvete, kakao, havre og rug.
Referanser
- Caruso, J., Charles, J., Unruh, k., Giebel, r., Learmonth, l., & Potter, w. (2012). Ergogene effekter av ß-alanin og karnosin: foreslått fremtidig forskning for å kvantifisere effekten. Næringsstoffer, 4(7), 585-601.
- Gille, c., Bölling, ca., Hoppe, a., Bulik, s., Hoffmann, s., Hübner, k.,... Holzhütter, h. G. (2010). Hepatonet1: En omfattende metabolsk rekonstruksjon av den menneskelige hepatocytten for analyse av leverfysiologi. Molekylære systembiologi, 6(411), 1-13.
- Mathews, c., Van Holde, K., & Ahern, K. (2000). Biokjemi (3. utg.). San Francisco, California: Pearson.
- Murray, r., Bender, d., Botham, k., Kennelly, p., Rodwell, v., & Weil, P. (2009). Harpers illustrerte biokjemi (28. utg.). McGraw-Hill Medical.
- Nelson, d. L., & Cox, m. M. (2009). Lehninger prinsipper for biokjemi. Omega -utgaver (5. utg.).
- « Elektromagnetisk forurensningsårsaker, konsekvenser
- Glutaminsyreegenskaper, funksjoner, biosyntese »

