Syreanhydrider Hvordan dannes, applikasjoner og eksempler

- 1156
- 270
- Prof. Oskar Aas
De Syreanhydrider De anses av stor betydning blant det store utvalget av forbindelser med organisk opprinnelse som finnes. Disse presenteres som molekyler som har to syregrupper (organiske substituenter hvis formel er rco-, hvor r er en karbonkjede) forent til det samme oksygenatom.
Det er også en klasse av syreanhydrider som ofte finnes: karboksylanhydrider, kalt fordi startsyren er en karboksylsyre. For å nevne den av denne typen hvis struktur er symmetrisk, må bare en erstatning av vilkår utføres.

Syreuttrykket må erstattes i nomenklaturen til den opprinnelige karboksylsyren ved anhydridbegrepet, som betyr "uten vann", uten å endre resten av navnet på det dannede molekylet. Disse forbindelsene kan også genereres basert på en eller to syregrupper fra andre organiske syrer, for eksempel fosfonsyre eller sulfonsyre.
Tilsvarende kan syreanhydrider være forårsaket basert på en uorganinsyre, for eksempel fosforsyre. Imidlertid avhenger dens fysiske og kjemiske egenskaper, dens anvendelser og andre egenskaper av syntesen utført og anhydridstrukturen.
[TOC]
Hvordan dannes sure anhydrider?
Noen syreanhydrider stammer fra forskjellige måter, enten i laboratoriet eller i bransjen. I industriell syntese blir eddikanhydrid tatt som et eksempel, som hovedsakelig produseres ved karboniseringsprosessen til metylacetatmolekylet.
Et annet eksempel på disse syntesen er den fra Anhydride Malico, som genereres gjennom oksidasjon av benzenmolekylet eller butan.
Det kan tjene deg: sinkhydroksid (Zn (OH) 2)I syntesen av syreanihydrider i laboratoriet legges imidlertid det vekt på dehydrering av de tilsvarende syrene, slik som produksjon av etanisk anhydrid, der to molekyler av etainsyre er dehydrert for å gi opphav til den nevnte forbindelsen.
En intramolekylær dehydrering kan også oppstå; Det vil si innenfor det samme molekylet til en syre med to karboksyl (eller dikarboksyliske) grupper, men hvis det motsatte oppstår og en syreanhydrid lider av hydrolyse, regenerering av syrene som oppsto den oppstår.
Syreanhydrider hvis acylsubstituenter er like, mens i anhydrider av denne typen anses som blandet, er disse molekylene forskjellige er forskjellige.
Imidlertid genereres disse artene også når det oppstår en reaksjon mellom en syresalur (hvis generelle formel er en (RCOX)) med et karboksylatmolekyl (hvis generelle formel er R'Cooo-))))))). [2]
Generell formel
Den generelle formelen for syreanhydrider er (RC (O))2Eller, som bedre observeres i bildet plassert i begynnelsen av denne artikkelen.
For eksempel for eddiksanhydrid (fra eddiksyre) er den generelle formelen (CH3Co)2Eller, skriver på samme måte for mange andre lignende syreanhydrider.
Som nevnt ovenfor, har disse forbindelsene nesten samme navn på forløpersyrene, og det eneste som endres er begrepet syre med anhydrid, siden de samme reglene for nummerering av atomer og substituenter må følges for å lykkes med sin nomenklatur.
applikasjoner
Syreanhydrider har mange funksjoner eller applikasjoner avhengig av feltet som studeres, ettersom de har høy reaktivitet, kan de være forløperreagenser eller være en del av mange viktige reaksjoner.
Kan tjene deg: pyrolyseEt eksempel på dette er industrien, der eddikanhydrid produseres i store mengder fordi det er den enkleste strukturen som kan isoleres. Dette anhydridet brukes som et viktig organisk reagens, for eksempel acetatestere.
Industriell bruk
På den annen side vises anhydrid Maleico med en syklisk struktur, som brukes i produksjonen av dekning for industriell bruk og som en forløper for noen harpikser gjennom kopolymetiseringsprosessen med Stretus -molekyler. I tillegg fungerer dette stoffet som en dienofil når Diels-Alder-reaksjonen blir utført.
Tilsvarende er det forbindelser som har to syreanhydrider molekyler i strukturen, for eksempel ethystarboxylic eller dianhydride dianhydrid.
I tillegg til disse er det et blandet anhydrid kalt 3'-fosfoadenosín-5'-fosfosulfat, fra fosforiske og svovelsyrer, som utgjør det vanligste koenzym i biologiske sulfatoverføringsreaksjoner.
Eksempler på syreanhydrider
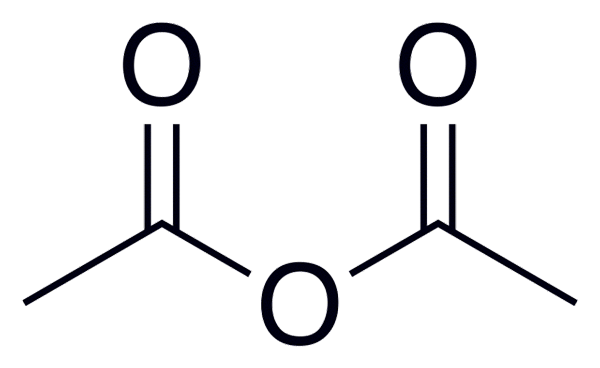 Eddikanhydrid
Eddikanhydrid Nedenfor er en liste med navnene på noen syreanhydrider, for å gi noen eksempler på disse viktige forbindelsene i organisk kjemi som kan danne forbindelser av lineær struktur eller ringer til flere medlemmer:
- Eddikanhydrid.
- Propanisk anhydrid.
- Benzoisk anhydrid.
- Malico -anhydrid.
- Succinic Anhydride.
- Ftalisk anhydrid.
- Naftalent -tracarboxylic dianhydride.
- Ethytertarboxylic dianhydride.
- Benzoquinontenterarboxylic dianhydride.
Akkurat som disse anhydridene med oksygen dannes, blir det gitt andre forbindelser der et svovelatom kan erstatte oksygen både i karbonylgruppen og sentral oksygen, for eksempel: for eksempel:
Kan tjene deg: Acetanylide (C8H9NO)- Tioacetisk anhydrid (velg3C (s)2ENTEN)
Det er til og med tilfellet med to syremolekyler som danner koblinger med det samme svovelatomet; Disse forbindelsene kalles Tioanhydrider, nemlig:
- Eddik Tioanhydrid ((CH3CO))2S)
Referanser
- Wikipedia. (2017). Wikipedia. Innhentet fra.Wikipedia.org
- Johnson, a. W. (1999). Invitasjon til organisk kjemi. Gjenopprettet fra bøker.Google.co.gå.
- Acton, q. TIL. (2011). Syreanhydridhydrolas: Fremskritt innen forskning og anvendelse. Gjenopprettet fra bøker.Google.co.gå
- Bruckner, r., Og Harmata, m. (2010). Organiske mekanismer: reaksjoner, stereokjemi og syntese. Gjenopprettet fra bøker.Google.co.gå
- Kim, J. H., Gibb, h. J., og Iannucci, til. (2009). Syklinsyreanhydrider: Menneskelige helseaspekter. Gjenopprettet fra bøker.Google.co.gå

