Karbokasjonsdannelse, egenskaper, typer, stabilitet
- 4178
- 1196
- Dr. Andreas Hopland
EN Carbocation, Som navnet tilsier, er det et organisk ion som har et positivt lastet karbonatom, som er preget av å være svært ustabilt, eksisterende i kort tid. Det er vanligvis en mellomledd i organiske reaksjoner, det vil si at den stammer som uunnværlige trinn for de respektive molekylære mekanismene.
Historisk sett har det vært konfliktpunkter i komprimering av hva karbokasjon er. Dette er fordi det er symfiner av reaktive molekyler som av en eller annen grunn skaffer seg en positiv belastning i en av karbonene deres. Klassisk karbokasjon, så å si, er en som kan representeres med den generelle formelen til bildet nedenfor.
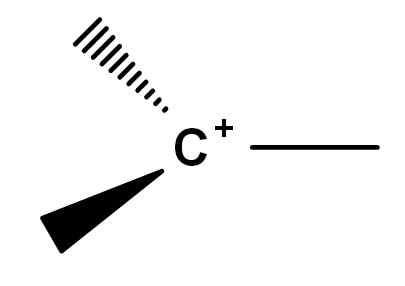 Generell formel for en karbokasjon. Kilde: Gabriel Bolívar.
Generell formel for en karbokasjon. Kilde: Gabriel Bolívar. Legg merke til hvordan den positive belastningen ligger nøyaktig på karbonatomet, og mangler også en lenke. Derfor er karbokasjon dårlige elektroner, dette er årsaken til den høye reaktiviteten.
Anta at metan, Cho4. Hvis karbon mistet et av sine hydrogenatomer, ville vi eliminere en av de fire C-H-bindingene. Da oppsto metylkarbokasjonen, CH3+, som vi kan representere bare ved å plassere hydrogenatomer i endene av stripene i den øvre formelen. Ch3+ Det er den enkleste av alle karbokasjoner.
[TOC]
Opplæring
Hvordan dannes karbokasjoner? Svaret finnes i reaksjonsmekanismer. Imidlertid deler de aller fleste til felles et av følgende to aspekter:
-Heterolytisk brudd
-Tilsetning av elektroner π til en elektrofil
Heterolytisk brudd
I det heterolitiske bruddet C-G-bindingen, G er et hvilket som helst atom eller gruppe, er det ødelagt på en ulik måte: elektronene til bindingen blir igjen G, mens karbonatomet skaffer seg en positiv belastning. For eksempel:
Kan tjene deg: arsen: historie, struktur, egenskaper, bruksområder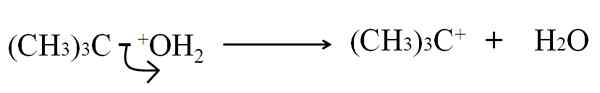 Heterolytisk brudd i tertbutanoldehydrering. Kilde: Gabriel Bolívar.
Heterolytisk brudd i tertbutanoldehydrering. Kilde: Gabriel Bolívar. Nå kan denne pausen gis for flere metoder, som igjen vil endre mekanismen og reaksjonen som vurderes.
Tilsetning av elektroner π til en elektrofil
Den andre prosessen som en karbokasjon dannes, og er veldig vanlig i aromatiske alkener og forbindelser, er ved å angripe elektroner av en dobbeltbinding til en elektrofil. De vanligste tilfellene er hydrogenering av alkener ved virkning av en syre:
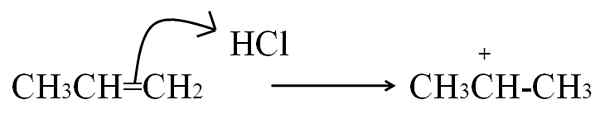 HCl -reaksjon med Propeno for å danne en karbokasjon som mellomledd. Kilde: Gabriel Bolívar.
HCl -reaksjon med Propeno for å danne en karbokasjon som mellomledd. Kilde: Gabriel Bolívar. Denne ligningen tilsvarer dannelsen av karbokasjon, som det er en formidler, Ikke et produkt. Dobbeltbindingselektronene angriper HCl -hydrogen, elektrofilen. Hydrogen tilsettes karbon til høyre for dobbeltbindingen, så gruppen -CH er dannet3, Mens karbonet til venstre skaffer seg den positive belastningen.
Kjennetegn
Hybridisering
Den generelle formelen presentert i begynnelsen avdekker en trigonal flat geometri rundt karbonatomet. Dette skyldes at hybridiseringen har lidd av karbonatomiske orbitaler for å bli hybrid SP -orbitaler2, som er atskilt i en vinkel på 120º. Selv om det ikke er representert, har Carbocation en orbital p Ren og tom, i stand til å akseptere elektroner.
Surhet
Carbocation er en sur art, enten i henhold til definisjonen av Brönsted eller Lewis. Deres positive ladningskravelektroner eller hydrogenatomer som er gitt. Det er av denne grunn at karbokasjoner ikke kan dannes i veldig grunnleggende medier, siden de umiddelbart ville reagere på stammer fra andre produkter.
Stabilitet
Hybridiseringen sp2 av Carbocation gjør det sårbart for angrep av rike arter i elektroner. Denne funksjonen fremheves videre av den store surheten. Følgelig er karbokasjon en veldig reaktiv art, som knapt dannes og snart (i et spørsmål om nanosekunder) reagerer for å gi opphav til det sanne produktet av den kjemiske reaksjonen.
Kan tjene deg: sulfaminsyre: struktur, egenskaper, syntese, brukTyper karbokasjoner
Det er flere typer karbokasjoner. Disse kan imidlertid klassifiseres som følger:
-Hoved
-Sekundær
-Tertiær
-Aromatiske eller arillos
-Vinyl og Alilic
Hoved
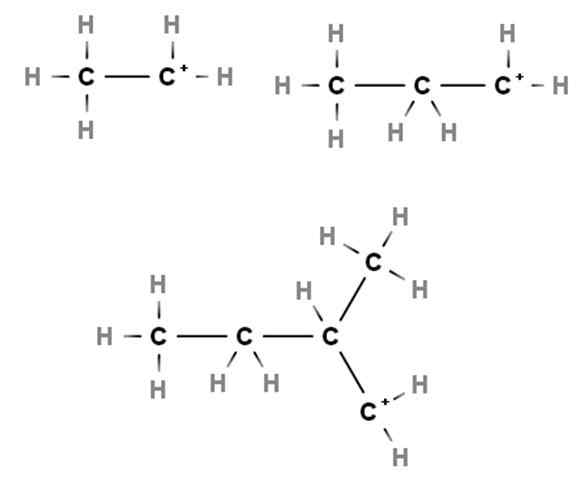 Primære karbokasjoner. Kilde: Gabriel Bolívar via Molview.
Primære karbokasjoner. Kilde: Gabriel Bolívar via Molview. Arrivals viser eksempler på primære karbokasjoner. De kalles det fordi den positive belastningen ligger i et primært karbon, 1., så den bare er knyttet til et karbonatom. Etano, kap3Ch3, Når en H mister noen av sine mål, kan CarboCation Cho3Ch2+ enten +Ch2Ch3.
Sekundær
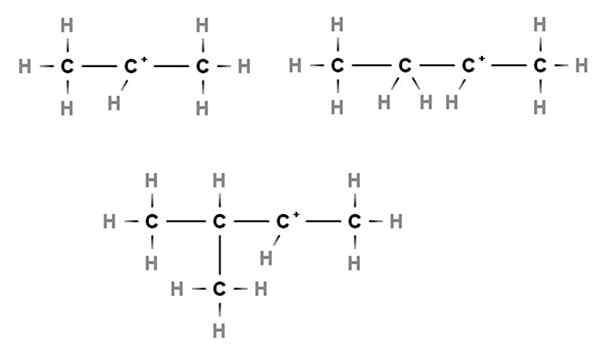 Sekundære karbokasjoner. Kilde: Gabriel Bolívar via Molview.
Sekundære karbokasjoner. Kilde: Gabriel Bolívar via Molview. I sekundære karbokasjoner er den positive belastningen lokalisert i et sekundært karbon, 2., som er knyttet til to karbonatomer. For eksempel, hvis propan, cho3Ch2Ch3, Vi tar bort en H av det sentrale karbonet, vi vil ha Carbocation Cho3Ch2+Ch3.
Tertiær
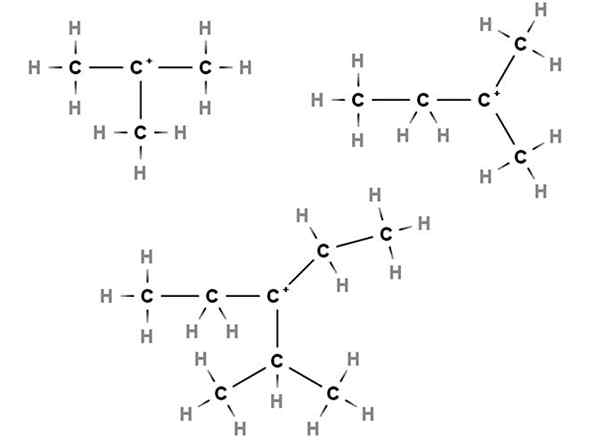 Tertiære karbokasjoner. Kilde: Gabriel Bolívar via Molview.
Tertiære karbokasjoner. Kilde: Gabriel Bolívar via Molview. I tertiære karbokasjoner er den positive belastningen lokalisert i et tertiært karbon, 3. plass, knyttet til tre karbonatomer. Legg merke til at i motsetning til de to første typene karbokasjoner, mangler de hydrogenatomer.
Dermed har vi metylpropan eller isobutan, CH (CH (velg3)3, Som ved å miste et hydrogen det sentrale karbonet danner karbokasjon +C (kap3)3.
Aromatisk
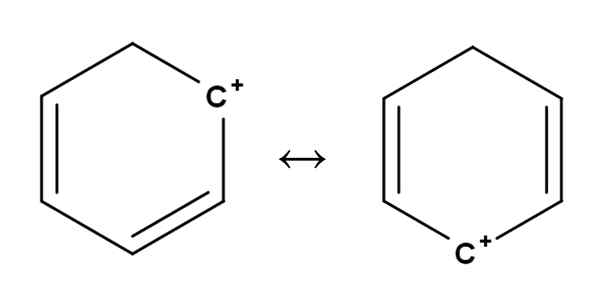 Benzen Carbocat. Kilde: Gabriel Bolívar.
Benzen Carbocat. Kilde: Gabriel Bolívar. Aromatiske eller aromatiske karbokasjoner er kanskje den mest spesielle av alle. Treningen din er veldig lik den som er beskrevet for alkener i den første delen.
I dem er den positive belastningen i prinsippet lokalisert, i en av karbonene i en aromatisk ring, for eksempel benzen. Den positive belastningen er imidlertid ikke fast, men er spredt i andre ringposisjoner ved resonans.
Det kan tjene deg: ribulosa-1,5-bifosfat (RUBP): Karakteristikker, karbolixeringSlik passerer den positive belastningen, som sett ovenfor, fra en karbon til et annet inne i benzenringen. Denne egenskapen gir denne karbokasjonen stor stabilitet mot de andre typene karbocations.
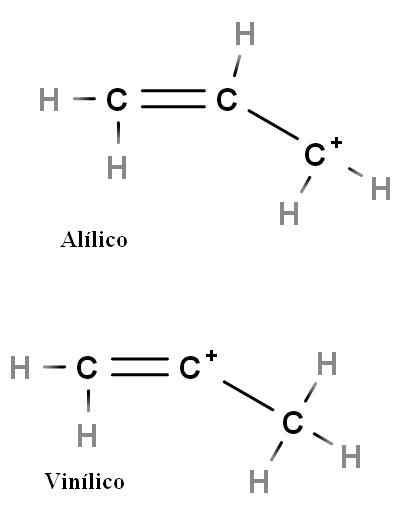
Allylic og vinyl
 Allylic og vinylkarbokasjon. Kilde: Gabriel Bolívar.
Allylic og vinylkarbokasjon. Kilde: Gabriel Bolívar. Andre spesielle typer karbokasjoner er aliliske og vinyl. Forskjellen mellom dem (over) er plasseringen av den positive ladningen relatert til dobbeltbinding.
I vinylkarbokasjon finnes den positive belastningen i en av dobbeltbindingskarbonene; Mens du er i allyisk karbokasjon, ligger den positive belastningen i karbonet etter dobbeltbindingen. Det er nok å erstatte hydrogener med andre grupper, og vi vil ha en enorm familie av allierte og vinylkarbokasjoner.
Relativ stabilitet
Når de vet hvilke som er hovedtyper av karbokasjoner, kan de bestilles basert på deres relative stabilitet:
Vinyl < Primario < Secundario < Alílico < Terciario < Aromático
Nå kan det være allikarbokasjoner som er mer stabile enn en spesifikk tertiær. Alt vil avhenge av deres substituenter.
Hvorfor denne stabiliteten? Til molekylets evne til å spre eller redusere den positive belastningen av karbokasjon. For å gjøre dette, trenger du nære atomer som gir en del av dens elektroniske karbokasjonstetthet ved hyperkonjugering. I mellomtiden, i alumiske og aromatiske karbokasjoner, oppnås dette ved resonans.
Når det2, Noe som gjør det veldig ustabilt.
Referanser
- Graham Solomons t.W., Craig f. Yngel. (2011). Organisk kjemi. (10th Utgave.). Wiley Plus.
- Carey f. (2008). Organisk kjemi. (Sjette utgave). Mc Graw Hill.
- Morrison og Boyd. (1987). Organisk kjemi. (Femte utgave). Addison-Wesley Iberoamericana.
- Wikipedia. (2020). Carbocation. Hentet fra: i.Wikipedia.org
- James Ashenhurst. (20. februar 2020). 3 faktorer som stabiliserer karbocations. Gjenopprettet fra: MasterorganicChemistry.com
- Clark Jim. (2000). Karbokasjoner (eller karboniumioner). Gjenopprettet fra: Chemguide.co.Storbritannia
- Dr. Kennepohl, prof. S. Farmer & t. Soderberg. (10. august 2020). Karbokasjonsstruktur og stabilitet. Kjemi librettexts. Gjenopprettet fra: Chem.Librettexts.org
- « Miljøetiske koder konsept, egenskaper og eksempler
- Årets 4 stasjoner i Mexico og dets egenskaper »

