Elektrolytiske celler
- 671
- 71
- Oliver Christiansen
 Elektrolytiske celler er en elektrokjemisk enhet for å øke ikke -spontane oksydreaksjoner gjennom elektrisitet
Elektrolytiske celler er en elektrokjemisk enhet for å øke ikke -spontane oksydreaksjoner gjennom elektrisitet Hva er elektrolytiske celler?
De Elektrolytiske celler De er enheter som brukes til å øke kjemiske reaksjoner av ikke -spontan reduksjon ved hjelp av bruk av elektrisitet. Med andre ord, de er celler der elektrolyseprosessen blir utført, og derav navnet.
Det er en bestemt type elektrokjemiske celler. Dette betyr at de er enheter der arten som oksiderer og den som er redusert, ikke er i direkte kontakt, men finnes i forskjellige rom eller reagerer i fysisk separate elektroder.
Av denne grunn forekommer ikke utveksling av elektroner mellom oksidasjons- og reduksjonsartene direkte, men gjennom en ekstern leder.
I tilfelle redoksreaksjonen skjer spontant, det vil si uten hjelp av en ekstern energikilde, snakker vi om galvaniske celler.
Et eksempel er et bilbatteri. På den annen side, hvis reaksjonen krever en ekstern energikilde, er det en elektrolytisk celle.
Drift av elektrolytiske celler
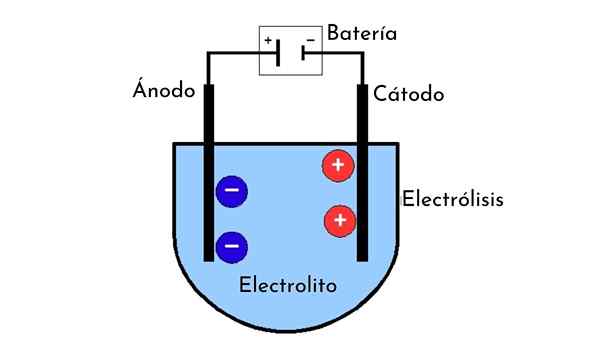
Hver elektrolytisk celle dannes av noen grunnleggende elementer som er:
- To elektroder kalt anode og katode.
- En løsning av stoffet som vi har til hensikt å underkaste oss elektrolyse eller, som ikke klarer det, det samme stoffet i flytende tilstand (for eksempel et smeltet salt).
- Elektriske ledere.
- En elektrisk strømkilde.
Prosessen utføres for reaksjoner som under normale forhold ikke er spontan. Dette betyr at de er rustreaksjoner reduksjon hvis cellepotensial, gitt konsentrasjonene av arten og temperatur- og trykkforholdene, er negative.
Dette innebærer at elektroner ikke har en tendens til å gå fra arten som vi ønsker å oksidere som vi ønsker å redusere, men snarere i motsatt retning. Ved å bruke en ekstern spenning på det motsatte tegnet, kan vi investere tegnet på cellepotensialet, og tvinger reaksjonen til å oppstå.
Kan tjene deg: løselig materialerSom enhver redoksreaksjon, oppstår elektrolyse i form av to semi -reaksjoner som forekommer separat i de to elektrodene. Disse kalles katode og anode.
Katoden
Katoden er elektroden som er koblet til den negative polen til energikilden, og det er der semi -reaksjonen av reduksjon oppstår. Det er også elektroden som positive ioner er rettet under elektrolyse. Faktisk er det her navnet på kationer kommer fra.
Når du representerer elektrolyseprosessen i form av et cellediagram, er reduksjonen semi -lys som oppstår i katoden alltid plassert på høyre side.
Anoden
Anoden er elektroden i motsetning til katoden. Det vil si at det er elektroden koblet til den positive kraften til energikilden og der oksidasjon semi -lys oppstår. Det er også stedet som ionene med negativ belastning (anionene) er rettet og er alltid representert på venstre side av cellediagrammet.
Elektronstrøm i elektrolytisk celle
Når elektrodene er koblet til de motsatte polene til en energikilde som har et potensial nok, lukkes kretsen og en elektrisk strøm genereres. Denne strømmen begynner ved anoden, der den reduserende arten oksiderer og mister elektroner.
Disse elektronene strømmer gjennom den elektriske lederen, drevet av potensialforskjellen til de når katoden. En gang på overflaten av katoden, passerer elektronene til oksidantarten, reduserer den og fullfører redoksreaksjonen.
Slik at strømmen av strøm kan fortsette, beveger ionene i løsningen eller det smeltede saltet fra den ene elektroden til den andre. Kationer strømmer til katoden og anioner mot anoden.
Kan tjene deg: kjemiske reaksjoner i hverdagenSelv om de ser ut til å være to strømmer i motsatte retninger, går begge strømningene i virkeligheten i samme retning. Dette er fordi belastningsbærerne som beveger seg i motsatte retninger også har motsatte belastninger.
Typer elektrolytiske celler
Elektrolyttceller med vandig løsning
Dette er de vanligste cellene. De består ganske enkelt av to elektroder av noen inert metall nedsenket i en vandig saltoppløsning som vi ønsker å underkaste oss elektrolyse.
De tjener bare til å redusere arter som har et mer positivt reduksjonspotensial enn hydrogen, forutsatt at pH er nøytralt.
På den annen side tjener de bare til å oksidere arter som har et oksidasjonspotensial større enn vannet bortsett fra oksygenoverskriver.
Elektrolytiske celler av smeltede salter
I tilfeller der arten vi ønsker. Dette krever en spesiell celle, for eksempel Downs celle.
Elektrolytiske celleapplikasjoner
Elektrolytiske celler er av stor betydning i bransjen. Noen av de viktigste applikasjonene er:
Energilagring
Elektrolyse gjør det mulig å konvertere elektrisk potensiell energi til potensiell kjemisk energi. Reduserte og oksiderte arter under elektrolyseprosessen blir nye arter som er i stand til å reagere spontant, og frigjør energien omvendt igjen.
Produksjon av elementære halogener
Halogener er av stor industriell betydning. De er imidlertid ikke i naturen elementært, siden de er veldig reaktive oksiderende stoffer. Av denne grunn kan mange av halogenene bare oppstå gjennom elektrolyse.
Kan tjene deg: SpredningsfaseRen metallproduksjon
Det samme som kan sies om halogener kan også sies om de mest reaktive metaller i det periodiske bordet. Elementer som alkaliske og kobbermetaller kan bare oppnås ved elektrolyse av smeltede salter og vandige oppløsninger.
Eksempler på elektrolytiske celler i dagliglivet
Natriumfluoridelektrolyse
Smeltet natriumnatriumfluoridelektrolyse brukes industrielt for produksjon av elementær natrium og fluor. Fluor kan deretter brukes til å oppnå andre mindre reaktive halogener.
Kobbernitratelektrolyse
I den industrielle kobberproduksjonen oppnås dette gjennom elektrolyse av vandige oppløsninger av saltene. I tillegg blir kobber også renset ved elektrolyse, oksiderende og oppløst det fra en elektrode og avsetter den i den andre.
Vannelektrolyse
Elektrolysen av en vandig løsning av svovelsyre dekomponerer oksygen og hydrogenvann og er en av de enkleste måtene å oppnå dette siste elementet i ren form.
Referanser
- Korint - generell kjemi (s. F.). Elektrolytiske celler. Hentet fra Korint.PUCP.Edu.PE.
- ECURED (s. F.). Elektrolytisk celle. Hentet fra Ecured.Cu.
- Luis Manuel (2014). Typer elektrokjemiske celler. Hentet fra Prezi.com.
- Stopp s., Yo. (2021). Hva er en elektrolytisk celle? Hentet fra Yubrain.com.

