Syklobutanstruktur, egenskaper, bruksområder og syntese
- 797
- 24
- Prof. Joakim Johansen
Han Cyclobutane Det er et hydrokarbon som består av en fire -karbon cyclocano, hvis molekylære formel er c4H8. Du kan også kalles tetrametylen, med tanke på at det er fire FN -enheter2 som utgjør en ring med firkantet geometri, selv om cyclobutan -navnet er mer akseptert og kjent.
Ved romtemperatur er det en fargeløs, brennbar gass som brenner med en lys flamme. Den mest primitive bruken er som en kilde til varme ved å brenne den; Imidlertid dekker den strukturelle basen (kvadratet) dype biologiske og kjemiske aspekter, og samarbeider på en viss måte med egenskapene til nevnte forbindelser.
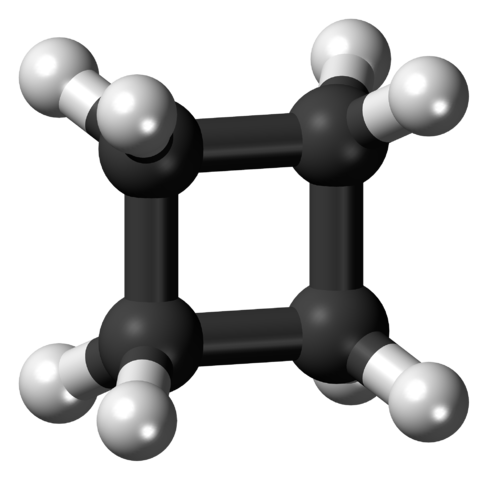 Syklobutanmolekyl i anspent konformasjon. Kilde: Jynto [CC0].
Syklobutanmolekyl i anspent konformasjon. Kilde: Jynto [CC0]. I det øvre bildet vises et syklobutanmolekyl med firkantet struktur. I neste avsnitt vil det bli forklart hvorfor denne konformasjonen er ustabil, siden koblingene er anspente.
Etter Cyclopropo er det den mest ustabile cycloalcan, siden jo mindre størrelse på ringen, desto mer reaktiv vil være. I følge dette er syklobutanen mer ustabil enn pentan- og heksano -syklusene. Imidlertid er det nysgjerrig å være vitne til i sine derivater et kjerne- eller firkantet hjerte, som, som det vil bli sett, er dynamisk.
[TOC]
Syklobutanstruktur
I det første bildet ble strukturen til syklobutanen adressert som et enkelt karbon og hydrogenert kvadrat. I dette perfekte firkanten lider imidlertid orbitalene en alvorlig forstuing i de opprinnelige vinklene: de er atskilt med en vinkel på 90º sammenlignet med 109,5º for et karbonatom med spa -hybridisering SP3 (Vinkelspenning).
Spåheter med karbon3 De er tetrahedraler, og for noen tetrahedra ville det være vanskelig å bøye begge orbitalene deres for å skape en vinkel på 90º; Men det ville være enda mer for karbonatomer med SP -hybridiseringer2 (120º) og SP (180º) avleder de originale vinklene. Av denne grunn har syklobutanen SP -karbonatomer3 i hovedsak.
Kan tjene deg: sekundær alkohol: hva er, struktur, egenskaper, brukOgså hydrogenatomer er veldig nær hverandre, formørket i verdensrommet. Dette resulterer i en økning i sterisk hindring, som svekker det påståtte firkanten for sin høye torsjonsspenning.
Derfor gjør vinkel- og torsjonsspenninger (innkapslet i begrepet 'ringformet spenning') denne konformasjonen ustabil under normale forhold.
Syklobutanen.
Sommerfugler eller rynkete konformasjoner
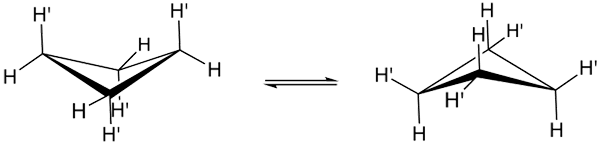 Cyclobutane -konformasjoner. Kilde: Smokefoot.
Cyclobutane -konformasjoner. Kilde: Smokefoot. De sanne konformasjonene av cyclobutano er vist ovenfor. I dem avtar vinkel- og torsjonsspenninger; Siden, som kan sees, er ikke alle hydrogenatomer formørket. Imidlertid er det en energikostnad: vinkelen på koblingene forverres, det vil si lavt fra 90 til 88º.
Merk at den kan sammenlignes med en sommerfugl, hvis trekantede vinger er dannet av tre karbonatomer; og den fjerde, plassert i en vinkel på 25º med hensyn til hver vinge. Piler med dobbel sans påpeker at det er en balanse mellom begge konformatorene. Det er som om sommerfuglen ned og klatrer opp vingene.
Hos de som er avledet fra syklobutanen, kan det derimot forventes at denne flagringen ville være mye treg og romlig forhindret.
Intermolekylære interaksjoner
Anta at du glemmer noen få øyeblikk av rutene, og erstatt dem på plass med kullsyreholdige sommerfugler. Du er i deres fladder kan bare holdes sammen i væsken ved hjelp av spredningskrefter i London, som er proporsjonale med området av vingene og dens molekylmasse.
Det kan tjene deg: karbonylgruppe: egenskaper, egenskaper, nomenklatur, reaktivitetEgenskaper
Fysisk utseende
Fargeløs gass.
Molekylmasse
56.107 g/mol.
Kokepunkt
12,6 ºC. Derfor i kalde forhold kan det i prinsippet manipuleres som en hvilken som helst væske; Med den eneste detaljene, at den ville være svært ustabil, og deres damper vil fortsatt representere en risiko for å ta hensyn til.
Smeltepunkt
-91 ºC.
tenningspunkt
50 ºC en lukket kopp.
Løselighet
Uoppløselig i vann, som ikke er overrasket gitt dens apolare natur; Men det er litt løselig i alkoholer, eter og aceton, som er mindre polare løsningsmidler. Det forventes å være oppløselig (selv om det ikke er rapportert) logisk i apolare løsningsmidler som karbontetraklorid, benzen, xylen, etc.
Tetthet
0.7125 til 5 ºC (i forhold til 1 fra vann).
Damptetthet
1.93 (i forhold til 1 i luften). Dette betyr at det er tett enn luften, og med mindre det er strømmer, vil trenden ikke stige opp.
Damptrykk
1.180 mmHg ved 25 ºC.
Brytningsindeks
1.3625 til 290 ºC.
Forbrenning entalpi
-655,9 kJ/mol.
Formasjonsvarme
6,6 kcal/mol a 25 ºC.
Syntese
Syklobutanen syntetiseres ved hydrogenering av syklobutadien, hvis struktur er nesten den samme, med den eneste forskjellen at den har en dobbeltbinding; Og derfor er det enda mer reaktivt. Dette er kanskje den enkleste syntetiske ruten for å skaffe den, eller i det minste bare for ham og ikke til et derivat.
I råoljen er det lite sannsynlig å oppnå siden det vil ende opp med å reagere på en slik måte at den brøt ringen og linjekjeden ble dannet, det vil si n-butan.
En annen metode for å oppnå syklobutan er å påvirke ultrafiolett stråling på etylenmolekyler, CH2= Ch2, som måles. Denne reaksjonen er fotokjemisk foretrukket, men ikke termodynamisk:
Kan tjene deg: Benchilo Benzoate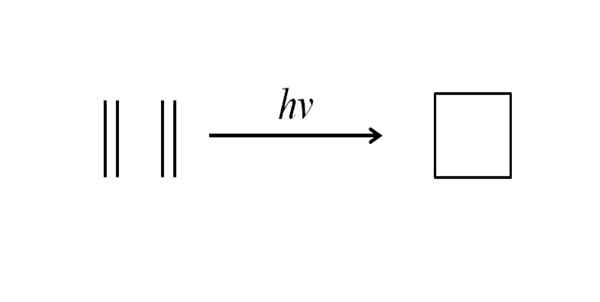 Cyclobutane syntese ved ultrafiolett stråling. Kilde: Gabriel Bolívar.
Cyclobutane syntese ved ultrafiolett stråling. Kilde: Gabriel Bolívar. Det øvre bildet oppsummerer det som ble sagt i avsnittet ovenfor. Hvis det i stedet for etylen for eksempel var to alkener, ville en erstattet syklobutan oppnås; eller hva som er det samme, et syklobutanderivat. Faktisk har mange derivater med interessante strukturer blitt syntetisert gjennom denne metoden.
Andre derivater innebærer imidlertid en serie kompliserte syntetiske trinn. Derfor er cyclobuta (som deres derivater kalles), gjenstand for studier for organisk syntese.
applikasjoner
Cyclobutane alene har ikke mer bruk enn å tjene som en kilde til varme; Men dets derivater inngår intrikate land i organisk syntese, med applikasjoner innen farmakologi, bioteknologi og medisin. Uten å utdype for komplekse strukturer, er Penitrems og Grandisol eksempler på syklobutanger.
Cyclobutans har generelt egenskaper som er gunstige for metabolismen av bakterier, planter, marine virvelløse dyr og sopp. De er biologisk aktive, og det er grunnen til at bruken av dem er veldig varierte og vanskelige å spesifisere, siden hver enkelt har sin spesielle effekt på visse organismer.
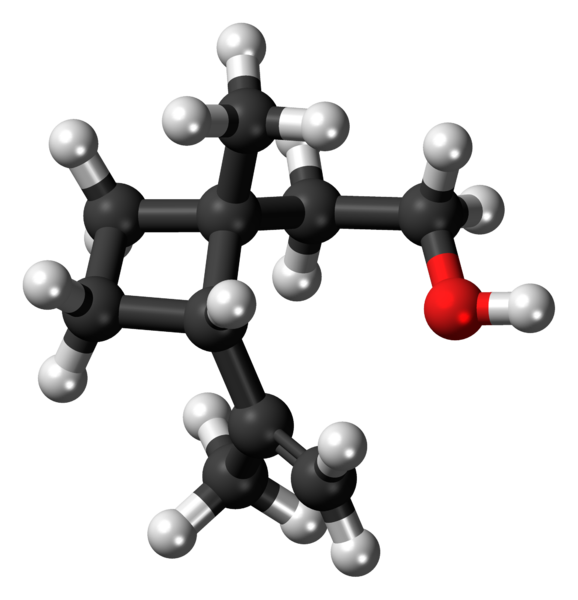
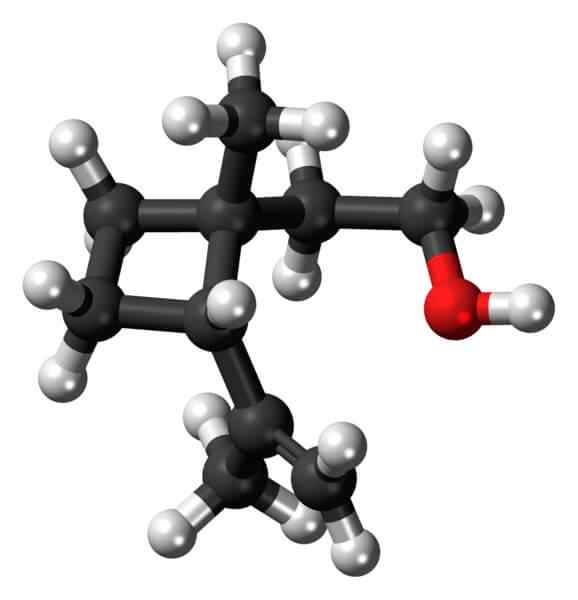 Grandisol: Et eksempel på et syklobutanderivat. Kilde: Jynto [CC0].
Grandisol: Et eksempel på et syklobutanderivat. Kilde: Jynto [CC0]. Grandisol, for eksempel, er en gorgjo feromon (en type bille). Over, og til slutt, blir strukturen vist, betraktet som en monoterpen med en firkantet base av syklobutan.
Referanser
- Carey f. (2008). Organisk kjemi. (Sjette utgave). Mc Graw Hill.
- Graham Solomons, t.W.; Craig f. Yngel. (2011). Organisk kjemi. (elleveth utgave). Wiley.
- Wikipedia. (2019). Cyclobutane. Hentet fra: i.Wikipedia.org
- Pubchem. (2019). Cyclobutane. Gjenopprettet fra: Pubchem.NCBI.NLM.NIH.Gov
- Peiris Nicole. (29. november 2015). Fysiske egenskaper til cycloalkanes. Kjemi librettexts. Gjenopprettet fra: Chem.Librettexts.org
- Wiberg b. Kenneth. (2005). Syklobutan-fysiske egenskaper og teoretiske studier. Department of Chemistry, Yale University.
- Klement Foo. (s.F.). Cyclobutanes i organisk syntese. Hentet fra: Scripps.Edu
- Myers. (s.F.). Cyclobutanes syntese. Chem 115. Gjenopprettet fra: hwpi.Harvard.Edu
- « Silver Bromuro (AGBR) struktur, egenskaper og bruk
- Syntetiske medikamentegenskaper, typer og effekter »

