Fluorhorsyre (HF)
- 2121
- 420
- Prof. Oskar Aas
Hva er fluorhorinsyre?
Han hydrofluorsyre (HF)Det er en vandig løsning der hydrogenfluoridet oppløses. Denne syren oppnås hovedsakelig fra reaksjonen av svovelsyre konsentrert med fluorittmineral (CAF2). Mineralet blir nedbrutt av virkningen av den gjenværende syren og vannet løser opp hydrogenfluoridgassene.
Fra det samme sure vannet kan det rene produktet destilleres, det vil si anhydrid hydrogenfluorid. Avhengig av mengden oppløst gass, oppnås forskjellige konsentrasjoner, og derfor flere tilgjengelige produkter av fluorhorinsyre i markedet.
I en konsentrasjon på mindre enn 40 %har den et skillebart krystallinsk utseende av vann, men ved høyere konsentrasjoner sier det farvel til hvite hydrogenfluoriddampene. Fluorhorinsyre er kjent som en av de mest aggressive og farlige kjemikaliene.
Det er i stand til å "spise" nesten alle materialer du har kontakt med: fra glass, keramikk og metaller, til steiner og betong. Der beholderen deretter lagres? I plastflasker, inerte syntetiske polymerer til handlingen din.
Formel
Hydrogenfluoridformelen er HF, men fluorhorsyre er representert i et vandig medium, HF (AC), for å skille seg fra den første.
Dermed kan fluorhorinsyre betraktes som hydrathydrogenfluorid, og dette er anhydrid.
Struktur av hydrofluorsyre
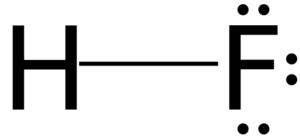 3D -modell av fluorhydronsyre
3D -modell av fluorhydronsyre All syre i vann har evnen til å generere ioner i en balansereaksjon. Når det3ENTEN+ og f-.
Anion f- Sannsynligvis danner en veldig sterk hydrogenbro med et av kationhydrogenene (F-H-O+-H2). Dette forklarer hvorfor fluorhoric acid er en svak breesyre (Proton Donor, h+), til tross for sin høye og farlige reaktivitet; det vil si at i vann frigjør ikke så mange h+ Sammenlignet med andre syrer (HCl, HBR eller HI).
Det kan tjene deg: hvor mange forvaringselektroner har karbon?I imidlertid konsentrerte fluorhorsyre -interaksjoner mellom hydrogenfluoridmolekyler er imidlertid effektive nok til at de kan slippe ut i en gassfase.
Det vil si at de i vannet kan samhandle som om de var i flytende anhydrid, og dermed danne hydrogenbroer mellom disse. Disse hydrogenbroene kan assimileres som nesten lineære kjeder (H-F-F-H-F- ...) omgitt av vann.
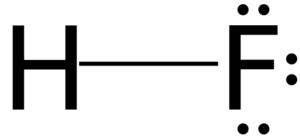
I det overordnede bildet er det ikke-delte dreiemomentet av elektroner orientert i motsatt retning av lenken (H-F :) samhandler med et annet HF-molekyl for å sette sammen kjeden.
Egenskaper til hydrofluorsyre
Fordi det er fluorhorsyre en vandig løsning, avhenger dens egenskaper av konsentrasjonen av anhydrid oppløst i vann. HF er veldig løselig i vann og er hygroskopisk, og kan produsere en rekke løsninger: fra veldig konsentrert (røyking og med gule toner) til veldig fortynnet.
Når konsentrasjonen avtar, vedtar HF (AC) egenskaper mer lik rent vann enn anhydrid. Imidlertid er H-F-H hydrogenbroer sterkere enn de i vann, h2ÅH ÅH.
Begge eksisterer i harmoni i løsninger, løfter kokepunkter (opptil 105 ºC). På samme måte øker tettheten etter hvert som mer hinhydrid blir oppløst. Av resten har alle HF (AC) -løsninger sterke og irriterende lukter og er fargeløse.
Reaktivitet
Så hva er den korrosive oppførselen til fluorhorinsyre? Svaret er i H-F-lenken og i evnen til fluoratomet med å danne veldig stabile kovalente koblinger.
Ettersom fluor er et veldig lite og elektronegativt atom, er det en kraftig Lewis -syre. Det vil si at det skiller seg fra hydrogen for å knytte arter som tilbyr flere elektroner til en lav energikostnad. For eksempel kan disse artene være metaller, for eksempel silisium som er til stede i glasset.
Det kan tjene deg: Nukleær kjemi: Historie, studieretning, områder, applikasjonerSio2 + 4 HF → SIF4(g) + 2 H2ENTEN
Sio2 + 6 HF → H2Sif6 + 2 h2ENTEN
Hvis dissosiasjonsenergien til H-F-koblingen er høy (574 kJ/mol), hvorfor er den ødelagt i reaksjoner? Svaret har kinetiske, strukturelle og energi nyanser. Generelt, jo mindre reaktivt det resulterende produktet er, desto mer favoriserte formasjonen.
Hva som skjer med f- i vann? I konsentrerte løsninger av fluorhorisk syre kan en annen HF -molekyl danne en hydrogenbro med F- av paret [h3ENTEN+F-].
Dette resulterer i generering av defluoridionene [FHF]-, som er ekstra surt. Det er grunnen til at all fysisk kontakt med dette er ekstremt skadelig. Den minste eksponering kan utløse en uendelig skade på byrået.
Det er mange sikkerhetsstandarder og protokoller for tilstrekkelig styring, og unngår dermed potensielle ulykker til de som opererer med denne syren.
Bruker/anvendelser av fluorhorsyre
Det er en sammensatt med mange applikasjoner i bransjen, i forskning og i forbrukernes arbeid:
- Fluorhorinsyre genererer organiske derivater involvert i aluminiumsrensingsprosessen.
- Det brukes i separasjonen av uran -isotoper, som for uranheksafluoruro (UF6). Det brukes også i ekstraksjon, prosessering og raffinering av metaller, bergarter og oljer, og brukes også til hemming av muggvekst og fjerning av formen.
- Etsende syreegenskap.
- Det brukes i fremstilling av silikon -halvledere, med flere bruksområder i utviklingen av databehandling og informatikk, ansvarlig for menneskelig utvikling.
- Det brukes i bilindustrien som en renholder, og brukes som en moldfjerner i keramikk.
- I tillegg til å tjene som mellomledd i noen kjemiske reaksjoner, brukes fluorhorinsyre i noen ionevekslere involvert i rensing av mer komplekse metaller og stoffer.
- Delta i oljeprosessering og dens derivater, som har tillatt innhenting av løsningsmidler for bruk i fremstilling av produkter for rengjøring og eliminering av fett.
- Det brukes i generering av midler for finér og overflatebehandling.
- Forbrukere bruker mange produkter der fluorhorinsyre har deltatt i utdypet; For eksempel noen nødvendige for bilpleie, rengjøringsprodukter for møbler, elektriske og elektroniske komponenter og drivstoff, blant andre produkter.
Referanser
- Pubchem. (2018). Hydrofluorsyre. Hentet 3. april 2018, fra: Pubchem.NCBI.NLM.NIH.Gov.
- Kat Day. (16. april 2013). Syren som virkelig spiser gjennom alt. Hentet 3. april 2018, fra: Chronicleflask.com
- Wikipedia. (28. mars 2018). Hydrofluorsyre. Hentet 3. april 2018, fra: In.Wikipedia.org.
- Shiver & Atkins. (2008). Uorganisk kjemi. (Fjerde utgave., p. 129, 207-249, 349, 407). Mc Graw Hill.
- Hydrofluorsyre. Musk. Medical University of South Carolina. Hentet 3. april 2018, fra: AcademicDepartments.Musk.Edu