Sulfonsyrestruktur, nomenklatur, egenskaper, bruk
- 2988
- 573
- Daniel Skuterud
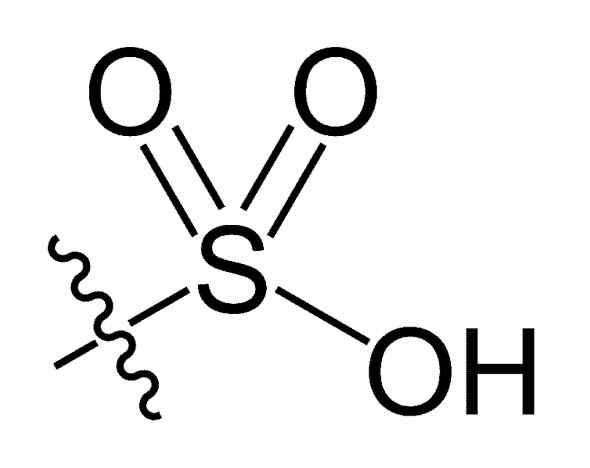
Det kalles sulfonsyre I det hele tatt tilhørende en familie av organiske syrer som har en eller flere grupper -så3H. Enkelte forfattere indikerer at farforbindelsen er h-s (= o)2-Å, eller H-SO3H, kalt av noe "sulfonsyre", er imidlertid dens eksistens ikke blitt bevist, og heller ikke den for dens ho -s tautomer (= o) -oh kjent som "svovelsyre" (h2SW3), verken i løsning eller i fast tilstand.
Sistnevnte skyldes at svoveldioksidgass (iv) (så2) I vandig løsning blir det bisulfittioner (HSO3-) og pyrosulfite (s2ENTEN52-) Og ikke til h-s (= o)2-Oh eller ho -s (= o) -oh, som allerede er bevist av mange kjemiske forskere.
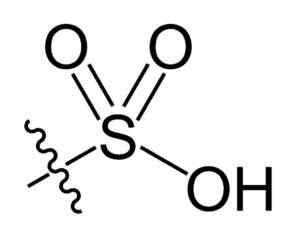 Sulfonilgruppe. Choij [Public Domain]. Kilde: Wikipedia Commons
Sulfonilgruppe. Choij [Public Domain]. Kilde: Wikipedia Commons I R-SO Chemical Formula3H av sulfonsyrer, gruppe R kan representere hydrokarbonskjeletter som alkan, alqueno, alchene og/eller sand. Disse kan inneholde sekundære funksjoner som ester, eter, keton, amino, amido, hydroksyl, karboksyl og fenolgrupper, blant mange andre.
Sulfonsyrer er sterke syrer, sammenlignbare med svovelsyre (H2SW4). Imidlertid avhenger resten av dens egenskaper i stor grad av gruppen R.
Noen har en tendens til å avsvømme ved høye temperaturer. Dette betyr å miste gruppen -så3H, spesielt når R er en sand, det vil si med benzenring.
Sulfonsyrer har mange bruksområder avhengig av deres kjemiske formel. De brukes til å produsere fargestoffer, blekk, polymerer, vaskemidler, overflateaktive midler og som katalysatorer, blant mange andre bruksområder.
[TOC]
Struktur
Sulfonsyrer har følgende generelle struktur:
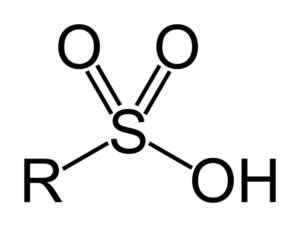 Generell formel av sulfonsyrer. Benjah-BMM27 [Public Domain]. Kilde: Wikipedia Commons
Generell formel av sulfonsyrer. Benjah-BMM27 [Public Domain]. Kilde: Wikipedia Commons Nomenklatur
- Sulfonilgruppe: -so3H
- Leid eller arilsulfonsyre: r-so3H
Egenskaper
De er faste eller væske avhengig av gruppe R. Ingen gassformige sulfonsyrer er kjent.
Dens fysiske og kjemiske egenskaper avhenger av arten av gruppen R. Til sammenligning er det noen fysiske egenskaper til flere sulfonsyrer, hvor P.F. Det er smeltepunktet og P.og. Det er kokepunktet ved et trykk på 1 mm Hg:
- Metanosulfonsyre: P.F. 20 ºC; p.og. 122 ºC
- Etanosofonsyre: P.F. -17 ºC; p.og. 123 ºC
- Proposulfonsyre: P.F. -37 ºC; p.og. 159 ºC
- Butanosulfonsyre: P.F. -15 ºC; p.og. 149 ºC
Kan tjene deg: jernholdig klorid (FECL2): Struktur, bruksområder, egenskaper- Pentosulfonsyre: P.F. -16 ºC; p.og. 163 ºC
- Heksanosulfonsyre: P.F. 16 ºC; p.og. 174 ºC
- Benzefonsyre: P.F. 44 ºC; p.og. 172 ºC (ved 0,1 mm Hg)
- P-toluensulfonsyre: P.F. 106 ºC; p.og. 182 ºC (ved 0,1 mm Hg)
- 1-naftalensulnsyre: P.F. 78 ºC; p.og. Det dekomponerer
- 2-naftalensulfonsyre: P.F. 91 ºC; p.og. Det dekomponerer
- Trifluormetanosulfonsyre: P.F. ingen; p.og. 162 ºC (ved 760 mm Hg)
De fleste er veldig løselige i vann.
Sulfonsyrer er enda flere syrer enn karboksylsyrer. De har surhet som ligner på svovelsyre. De oppløses i vandig natriumhydroksyd og vandig bikarbonat.
De har en tendens til å lide termisk nedbrytning, og oppstår deres avkonasjon. Imidlertid er flere av alkosulfonsyrene termisk stabile. Spesielt er trisk syre eller trifluormetansulfonsyre en av de sterkeste og mest stabile syrene.
Å skaffe
Arilsulfonsyrer
Ailsulfonsyrer oppnås generelt gjennom sulfoneringsprosessen som består av å tilsette et overskudd av røyksulfovinsyre (h2SW4 + SW3) Til den organiske forbindelsen vi vil ha sulfonar. For eksempel når det gjelder benzen:
C6H6 + H2SW4 C6H5SW3H + h2ENTEN
ARH + H2SW4 Arso3H + h2ENTEN
Sulfonering er en reversibel reaksjon, for hvis vi tilfører benzeulfonsyre en fortynnet syre og passerer damp på blandingen3 Og benzen blir destillert ved flyktning med damp, og fortrenger balansen mot avkonasjon.
Sulfonantmiddelet kan også være klorosulfursyre, sulfaminsyre eller sulfittioner.
Alkylofonsyrer
Disse er vanligvis fremstilt ved sulfo-oksidasjon, det vil si behandling av alkylforbindelser med svoveldioksid SO2 og oksygen eller2, eller direkte med svoveltrioksid så3.
RH + 2SO2 + ENTEN2 + H2Eller r-so3H + h2SW4
applikasjoner
Sulfonsyrer for overflateaktive midler og vaskemidler
Alkybenfinsyrer brukes i fremstilling av vaskemidler, og er en av de mest utbredte bruksområdene.
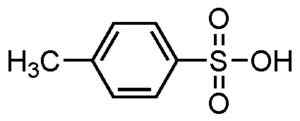 P-metylbenzefonsyre. Su-no-g. Kilde = Selvlaget. *Dato = 21. august 2006. *Laget med ChemDraw. Kilde: Wikipedia Commons.
P-metylbenzefonsyre. Su-no-g. Kilde = Selvlaget. *Dato = 21. august 2006. *Laget med ChemDraw. Kilde: Wikipedia Commons. De brukes til pulveriserte og flytende vaskemidler, vaskemidler for tunge eller lette oppgaver, hender og sjampo såper.
De aktive komponentene er generelt den alkybenzen lineære og sulfonerte fettsestere.
Ettersom overflateaktive midler er vanlige alfa-olefin-sulfonater, disulfonater, sulfosuccinater.
Kan tjene deg: natriumoksalat (Na2C2O4): Struktur, egenskaper, bruksområder, risikoDisse overflateaktive midlene finner bruk i husholdningsrengjøringsprodukter, kosmetikk, polymerisasjon i emulsjoner og kjemisk produksjon for landbruk.
Ligosulfonatene er avledet sulfonert fra lignin, en komponent av tre, og brukes som disperging, fuktighetsgivende, bindende midler i veipau, betongtilsetningsstoffer og tilsetningsstoffer i dyremat.
En 2-naftalanosulfonsyre avledet brukes til å øke sementfluiditet og styrke.
Sulfonsyrebasert fargelegging
Disse er generelt preget av å inneholde AZO-grupper (R-N = N-R).
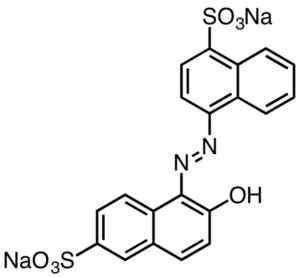 Syre rød fargelegging. Smokefoot [CC By-SA 4.0 (https: // creativecommons.Org/lisenser/by-SA/4.0)]. Kilde: Wikipedia Commons.
Syre rød fargelegging. Smokefoot [CC By-SA 4.0 (https: // creativecommons.Org/lisenser/by-SA/4.0)]. Kilde: Wikipedia Commons. Sulfonsyre -avledede fargestoffer har nytteverdi i papirindustrien, blekk som injeksjonstrykk, tekstiler som bomull og ull, kosmetikk, såper, vaskemidler, mat og lær.
Et 2-naftalanosulfonsyrederivat brukes også som en fargelegging ingrediens for polyesterfibre og læring av lær.
Amider basert på sulfonsyrer
Denne applikasjonen fremhever akrylamidfonsyrene, som har polymerer, i metallelektrode, for eksempel overflateaktive midler og i transparente anti -kompanioner belegg.
De brukes også i forbedret oljeutvinning, som sammensatte liberende midler på jord, i hydrauliske sementblandinger og som aminoplastiske harpikser herdende akseleratorer.
Noen sulfonamider brukes også i insektmiddelformler.
Fluorerte og klorfluorsulfonsyrer
Denne gruppen fremhever trifluormetanosulfonsyre (CF3SW3H), også kalt trisk syre. Denne forbindelsen har en organisk syntese og polymerisasjonsreaksjoner katalyse.
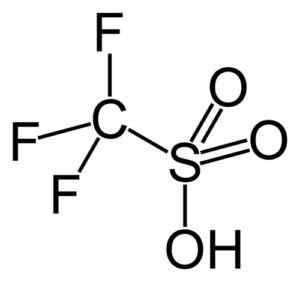 Trific Acid. Capacio [CC By-SA 3.0 (https: // creativecommons.Org/lisenser/by-SA/3.0)]. Kilde: Wikipedia Commons.
Trific Acid. Capacio [CC By-SA 3.0 (https: // creativecommons.Org/lisenser/by-SA/3.0)]. Kilde: Wikipedia Commons. For eksempel brukes det i polymerisasjon av aromatiske olefiner og i fremstilling av sterkt forgrenede parafiniske hydrokarboner med et høyt oktannummer for å bruke dem som drivstofftilsetningsstoffer.
En annen av anvendelsene er i syntesen av ledende polymerer, ved hjelp av polyacetylendoping, produserer for eksempel halvledere p.
Pentafluoroetanosulfonsyre (CF3Jfr2SW3H), kjent som pentaplinsyre, brukes som organisk katalysator.
Trific acid reagerer med antimon pentafluorid (SBF5) Genererer den så -kalt "magiske syre", en supersikre katalysator som tjener for alkylering og polymerisasjon.
Kan tjene deg: Jod Tinktur: Egenskaper, bruksområder, kontraindikasjonerNafion-H er en ionebytteharpiks av en parfymert polymersulfonsyre. Det har karakteristikken ved å være inert mot sterke syrer, sterke baser og redusere eller oksidere midler.
I biologiske anvendelser
En av få sulfonsyrer som finnes i naturen er 2-aminoetanosulfonsyre, bedre kjent som tyrefekting, en i hovedsak aminosyre, spesielt for katter.
Syntetisk og naturlig tyrefekting brukes som kosttilskudd i kjæledyrmat og farmasøytiske produkter.
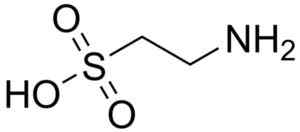 Bullfighting Molecule. Harbinary. Kilde: Wikipedia Commons
Bullfighting Molecule. Harbinary. Kilde: Wikipedia Commons Taurokolsyre er en gallekomponent og deltar i fordøyelsen av fett. 8-anilino-1-naftalanosulfonsyre, en syntetisk forbindelse, brukes i studiet av proteiner.
Urea -kopolymerer og bifenyldisulfonsyre har blitt brukt som herpes simplex virusinhibitorer.
Noen sulfonsyrederivater, så som sulfonert polystyren og noen azokompiesto.
I oljeindustrien
Enkelte blandinger av oljederivater, som inkluderer en variert kombinasjon av aromatiske, parafiner og polynukleære aromatiske, kan sulfoneres og deretter riktig nøytralisert generering av de SO -kalt oljesulfonater.
Disse oljesulfonatene har eiendom til å senke operasjonsspenningen i vann. I tillegg er produksjonen veldig lave kostnader.
Av denne grunn blir oljesulfonater injisert i eksisterende oljebrønner som hjelper utvinning av råolje som er okkludert mellom bergarter under overflaten.
I formulering av smøremidler og antikorrosiv
Magnesiumsulfonater har bred bruk i smøremiddelformler som dispergering-detetersgent-tilsetningsstoffer og for å unngå slitasje.
Bariumsulfonater brukes i anti -flint smøremidler for bruk som brukes i høyhastighetsapplikasjoner. Natrium- og kalsiumsulfonater har smøremidler og fettfett for å forbedre ekstreme trykkegenskaper.
Sulfonsyre magnesiumsalter er også nyttige i antikorrosive anvendelser som belegg, fett og harpikser.
Referanser
- Falk, Michael og Giguer, Paul A. (1958). På arten av svovelsyre. Canadian Journal of Chemistry, Vol. 36, 1958. Gjenopprettet fra NRCResearchPress.com
- Betts, r.H. og Voss, r.H. (1970). Kinetikken til oksygenutveksling mellom sulfittion og vann. Canadian Journal of Chemistry, Vol. 48, 1970. Gjenopprettet fra NRCResearchPress.com
- Bomull, f.TIL. Og Wilkinson, g. (1980). Avansert uorganisk kjemi. Fjerde utgave. Kapittel 16. John Wiley & Sons.
- Kirk-Ohmer (1994). Encyclopedia of Chemical Technology. Volum 23. Fjerde utgave. John Wiley & Sons.
- Kosswig, Kurt. (2012). Overflateaktive midler. Ullmanns Encyclopedia of Industrial Chemistry Vol. 35. Wiley-VCH Verlag GmbH & Co.
- « Klordioksid (CLO2) struktur, bruk, innhenting, risiko, egenskaper
- Polyaktisk syrestruktur, egenskaper, syntese, bruker »

