Vinsyre
- 2106
- 474
- Magnus Sander Berntsen
Vi forklarer hva som er tartarsyre, dens fysiske og kjemiske egenskaper, dens struktur og dens anvendelser
Hva er ternarsyre?
Han vinsyre Det er en organisk forbindelse hvis molekylære formel er COOH (Choh)2COOH. Den har to karboksylgrupper; Det vil si at du kan gi ut to protoner (h+). Med andre ord, det er en diprotsyre. Det kan også klassifiseres som et aldarsyre (syresukker) og et ravsyrederivat.
Saltet er kjent siden uminnelige tid. Det er krystallisert som et hvitt sediment som er døpt som "vindiamanter", som akkumuleres i korken eller på bunnen av fatene og flaskene. Dette saltet er kaliumbiitartrat (eller kaliumsyre tartrato).
Tartarsyresalter har til felles tilstedeværelsen av ett eller to kationer (NA+, K+. NH4+, Ac2+, etc.) fordi den ved å slippe de to protonene, forblir negativt ladet med en belastning på -1 (som med biterrato -salter) eller -2.
På sin side har denne forbindelsen vært gjenstand for studier og undervisning i organiske teorier relatert til optisk aktivitet, mer presist med stereokjemi.
Hvor er ternarsyre?
Tartarsyre er en komponent i mange planter og mat, som aprikos, avokado, epler, tamarindos, solsikkefrø og druer.
I prosessen med å aldrende vinene er denne syren - til kalde temperaturer - kombinert med kalium for å krystallisere som tartrato. I røde viner er konsentrasjonen av disse tartratene mindre, mens de i hvite viner er rikere.
Tartrater er salter av hvite krystaller, men når de okkluderer urenheter i det alkoholholdige miljøet, får de rødlige eller lilla toner.
Kan tjene deg: ForskyvningsreaksjonTartarsyrestruktur
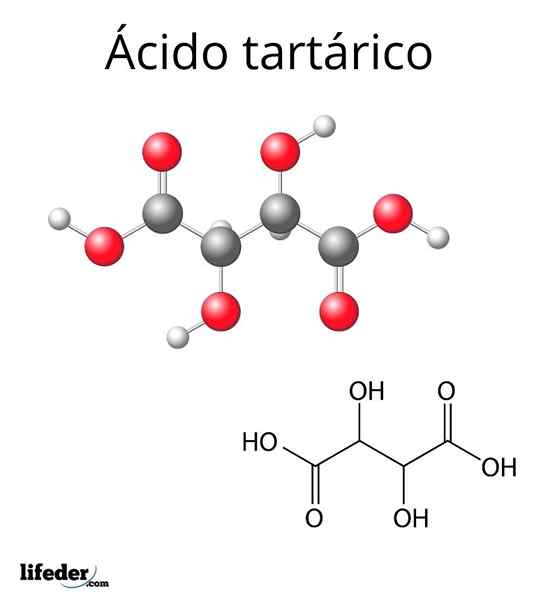
 Molekylær struktur av vinsyre
Molekylær struktur av vinsyre Molekylstrukturen til tartarsyre er representert i det øvre bildet. Karboksylgruppene (-COOH) er plassert i sideendene og er atskilt med en kort to karbonkjede (C2 og c3).
På sin side er hver av disse karbonatomeren knyttet til en H (hvit sfære) og en OH -gruppe. Denne strukturen kan rotere C -lenken2-C3, dermed generere flere konformasjoner som stabiliserer molekylet.
Det vil si den sentrale koblingen til det ødelagte molekylet som en roterende sylinder, veksler fortløpende den romlige disposisjonen til gruppene -COOH, H og OH (Newman -projeksjoner).
På bildet peker for eksempel de to OH -gruppene i motsatte retninger, noe som betyr at de er i anti -stillinger med hverandre. Det samme gjelder grupper -COOH.
En annen mulig konformasjon er av et par formørket grupper, der begge gruppene er orientert i samme retning. Disse konformasjonene ville ikke spille en viktig rolle i strukturen til forbindelsen hvis alle karbonegrupper C2 og c3 De var de samme.
Som i denne forbindelsen er de fire gruppene forskjellige (-COOH, OH, H, og den andre siden av molekylet), er karbonatomer asymmetriske (eller kiraler) og viser den berømte optiske aktiviteten.
Måten grupper er ordnet i karbon på2 og c3 av tartarsyre bestemmer noen forskjellige strukturer og egenskaper for samme forbindelse; det vil si tillater eksistensen av stereoisomerer.
Tartarsyreapplikasjoner
I matindustrien
Det brukes som en eulsjonsstabilisator i bakerier. Det brukes også som ingrediens til gjær, syltetøy, gelatin og brus. Det oppfyller også funksjoner som en forsurende, bibliotek og budgiver.
Det kan tjene deg: natriumbromid (NABR)Tartarsyre finnes i disse matvarene: søte informasjonskapsler, godteri, sjokolade, gassformig væsker, bakeriprodukter og viner.
I utdypingen av vinene brukes det til å gjøre dem mer balanserte, fra det gustatoriske synspunktet, ved å redusere pH -pH i disse.
I legemiddelindustrien
Det brukes til å skape piller, antibiotika og sprudlende piller, så vel som i medisiner som brukes i behandling av hjertesykdommer.
I den kjemiske industrien
Det brukes i fotografering, så vel som i galvanoteknikk og er en ideell antioksidant for industrifett.
Det brukes også som en metallion kidnapper. Som? Å rotere koblingene sine på en slik måte at du kan finne oksygenatomer i karbonylgruppen, rike på elektroner, rundt disse positivt belastede artene.
I byggebransjen
Forsink prosessen med å herde gipsen, sement og gips, noe som gjør manipulasjonen av disse materialene mer effektiv.
Tartarsyreegenskaper

De vanligste tartarsyreapplikasjonene er:
- Tartarsyre markedsføres i form av krystallinsk pulver eller litt ugjennomsiktige hvite krystaller. Den har en hyggelig smak, og denne egenskapen er en indikasjon på vin av god kvalitet.
- Smelter ved 206 ºC og brenner ved 210 ºC. Det er veldig løselig i vann, alkoholer, grunnleggende løsninger og boraks.
- Densiteten er 1,79 g/ml ved 18 ºC og presenterer to surhetskonstanter: PKA1 og PKA2. Det vil si at hver av de to syrene protoner har sin egen tendens til å frigjøre seg i det vandige miljøet.
- Som har -coh og OH -grupper, kan det analyseres ved infrarød spektroskopi (IR) for deres kvalitative og kvantitative bestemmelser.
- Andre teknikker som massespektroskopi og kjernemagnetisk resonans, tillater den forrige analysen av denne forbindelsen.
Stereokjemi

Tartarsyre var den første organiske forbindelsen som en enantiomer oppløsning ble utviklet. Hva betyr dette? Det betyr at stereoisomerer kan skilles manuelt takket være forskningsarbeidet til biokjemisten Louis Pasteur, i 1848.
Og hva er stereoisomerer av tartarsyre? Disse er: (r, r), (s, s) og (r, s). R og S er de romlige konfigurasjonene av karbonatomer C2 og c3.
Tartarsyre (R, R), den mest "naturlige", roterer det polariserte lyset til høyre; Tartarsyre (S, S) er ødelagt til venstre, i motsetning til klokken nåler. Og til slutt bryter ikke tartarsyre (r, s) det polariserte lyset, og er optisk inaktiv.
Louis Pasteur, ved hjelp av et mikroskop og pinsett, funnet og separerte tartarsyrekrystaller som viste "høyre -rett" og "venstrehåndte" mønstre, for eksempel i det overlegne bildet.
På denne måten er de "høyrehåndte" krystaller de som er dannet av enantiomeren (r, r), mens de "venstrehåndte" krystaller er de av enantiomeren (s, s).
Krystallene av tartarsyre (R, S) skiller seg imidlertid ikke fra andre, siden de viser dyktige og venstrehåndte egenskaper på samme tid; Derfor kunne de ikke bli "løst".
Referanser
- Wikipedia. (2018). Vinsyre. Innhentet fra.Wikipedia.org
- Pubchem. (2018). Vinsyre. Gjenopprettet fra Pubchem.NCBI.NLM.NIH.Gov.
- Forstå vinfarger. Gjenopprettet fra Jordanwinery.com
- Aktiv. Vinsyre. Gjenopprettet fra Actipedia.org
- Pochteca. Vinsyre. Pochteca kom seg.com.MX
- Dhanesshwar Singh et al. (2012). På opprinnelsen til den optiske inaktiviteten til meso-tartarsyre. Department of Chemistry, Manipur University, Canchipur, Imphal, India. J. Chem. Pharm. Storfekjøtt., 4 (2): 1123-1129.

