Sølvkromat (Ag2Cro4)
- 4026
- 712
- Prof. Oskar Aas
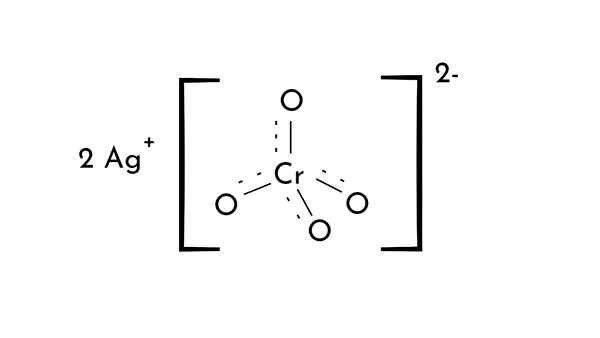
 Kjemisk struktur av sølvkromat. Med lisens
Kjemisk struktur av sølvkromat. Med lisens Hva er sølvkromat?
Han Sølvkromat Det er en kjemisk forbindelse av formel AG2Cro4. Det er en av kromforbindelsene i oksidasjonstilstand (VI), og det sies at det er forløperen for moderne fotografering.
Forbindelsesforberedelse er enkel. Det produseres ved en utvekslingsreaksjon med et løselig sølvsalt, slik som mellom kaliumkromat og sølvnitrat.
23(aq) + na2Cro4(AQ) → AG2Cro4(S) + 2nano3(En q)
Nesten alle alkaliske og nitratmetallforbindelser er oppløselige, men de fleste sølvforbindelser er uoppløselige (unntatt acetater, perklorater, klor og nitrater).
Derfor, når oppløselige salter blandes med sølvnitrat og natriumkromat, danner sølvkromat uoppløselig og bunnfall.
Fysiske og kjemiske egenskaper til sølvkromat
Sølvkromat er røde eller brune monokliniske krystaller uten karakteristisk lukt eller smak.
Forbindelsen har en molekylvekt på 331,73 g/mol og en tetthet på 5 625 g/ml. Det har et poeng på 1.550 ° C og er veldig lite oppløselig i vann og oppløselig i nitrogen og ammoniakksyre.
Som alle kromforbindelser (VI), er sølvkromat et sterkt oksidasjonsmiddel. De kan reagere med reduksjonsmidler for å generere varme og produkter som kan være gassformig (forårsaker press på lukkede beholdere).
Produkter kan være i stand til andre reaksjoner, for eksempel luftforbrenning. Den kjemiske reduksjonen av materialene i denne gruppen kan være rask eller til og med eksplosivt, men krever ofte initiering.
Reaktivitet og farer
Sølvkromat er en sterk, hygroskopisk oksidant (som absorberer fuktigheten i luften) og er følsom for lys. Eksplosive blandinger av uorganiske oksidasjonsmidler med reduksjonsmidler forblir ofte uendret i lange perioder hvis initiering unngås.
Kan tjene deg: etylenoksid: struktur, egenskaper, risikoer og brukSlike systemer er vanligvis blandinger av faste stoffer, men de kan innebære enhver kombinasjon av fysiske tilstander. Noen uorganiske oksidasjonsmidler er vannløselige metallsalter.
Som alle kromforbindelser (VI), er sølvkromat kreftfremkallende for mennesker, i tillegg til å være irriterende i tilfelle av hud- eller inntakskontakt.
Selv om det er mindre farlig, må det forhindres i tilfelle hudkontakt (etsende), øyekontakt (irriterende) og innånding. Langvarig eksponering kan forårsake hudforbrenninger og magesår. Innånding av overeksponering kan forårsake luftveisirritasjon.
Hvis forbindelsen kommer i kontakt med øynene, må kontaktlinsene sjekkes og fjernes, hvis de har. Øynene med rikelig med kaldt vann skal vaskes umiddelbart i minst 15 minutter.
I tilfelle hudkontakt, det berørte området med rikelig.
Du må dekke huden irritert med en mykgjørende lotion. Vask klær og sko før du bruker dem igjen. Hvis kontakten er alvorlig, vasker du med en desinfiserende såpe og dekker huden forurenset med en antibakteriell krem.
Ved innånding må offeret overføres til et nytt sted. Hvis du ikke puster, administreres kunstig pust. Hvis det er vanskelig å puste, gi oksygen.
Hvis forbindelsen er inntatt, skal oppkast ikke induseres med mindre det medisinske personalet indikerte det. Løsne tette klær, for eksempel skjortehals, belte eller slips.
I alle tilfeller må medisinsk behandling oppnås umiddelbart.
Kan tjene deg: spesifikke feilSølvkrombruk
Reagens i MOHR -metoden
Sølvkromat brukes som et reagens for å indikere sluttpunktet i mohr av argentometri. Reaktiviteten til kromatet med sølv er mindre enn Haluros (klorid og andre). Således vil i en blanding av begge ionene bli dannet sølvklorid.
Bare når det ikke er noen klorid igjen (eller noe halogen) vil danne sølvkromat (rødbrun) og bunnfall.
Før sluttpunktet har løsningen en melke sitronsult utseende, på grunn av fargen på kromatet og det allerede dannede sølvkloridutfellet. Når du nærmer deg det endelige punktet, fører sølvnitrat -tilsetninger til en progressiv nedgang i røde fargeasjoner.
Når den rødbrune fargen (med grå flekker av sølvklorid i den) forblir sluttpunktet i graden. Dette er for nøytral pH.
I veldig sur pH er sølvkromatet oppløselig, og i Alcalino La Plata PH -pH -presipitater som hydroksyd.
Cellulær farging
Sølvkromatformasjonsreaksjonen har vært viktig i nevrovitenskap, siden den brukes i Golgi -metoden for farging av nevroner for mikroskopi: sølvkromatet som produseres utfellinger inne i nevronene og gjør sin morfologi synlig.
Golgis metode er en sølvfargingsteknikk som brukes til å visualisere nervevev under optisk og elektronisk mikroskopi. Metoden ble oppdaget av Camillo Golgi, en italiensk lege og forsker, som publiserte det første fotografiet laget med teknikken i 1873.
Kan tjene deg: etyleterGolgi's farging ble brukt av den spanske neuroanatomist Santiago Ramón y Cajal (1852-1934) for å oppdage en serie nye fakta om organiseringen av nervesystemet, og inspirerte fødselen av nevronal doktrin.
I tillegg forbedret Ramón Y Cajal teknikken ved hjelp av en metode han kalte "dobbel impregnering". Ramón y Cajals fargingsteknikk, fremdeles i bruk, kalles Cajal Mancha.
Nanopartikkelstudie
AG -mikrokrystaller er blitt syntetisert2Cro4 ved hjelp av koprekipitasjonsmetoden.
Disse mikrokrystallene ble karakterisert ved XRD (XR) diffraksjon med Rietveld-analyse, elektronisk skanning av elektronisk mikroskopi ved feltemisjon (FE-SEEM), elektronisk overføringsmikroskopi (TEM) med energispredningsspektroskopi (EDS), mikromikro-Raman.
Fe-Seem-mikrografer avslørte morfologien og veksten av AG-nanopartikler på mikrokristige av AG2Cro4 Under bestråling med elektronstråle.
Teoretiske analyser basert på nivået av funksjonell teori om tetthet indikerer at inkorporering av elektroner er ansvarlig for strukturelle modifikasjoner og dannelse av defekter i klyngene [aug6] og [siden siden4], generere ideelle forhold for vekst av Ag nanopartikler.
Andre bruksområder
Sølvkromat brukes som utviklingsmiddel for fotografering. Det brukes også som en katalysator for aldoldannelse fra alkohol (sølvkromat (VI), S.F.) og som et oksidasjonsmiddel i forskjellige laboratorieaksjoner.
Referanser
- Nile kjemikalier (s.F.). Sølvkromat. Gjenopprettet fra nilechemicals.com.
- På tvers av organisk. Sikkerhetsdatablads sølvkromatmateriale, 99%. Gjenopprettet fra T3DB.Ac.

