Kjemisk delbarhet
- 5031
- 552
- Anders Mathisen
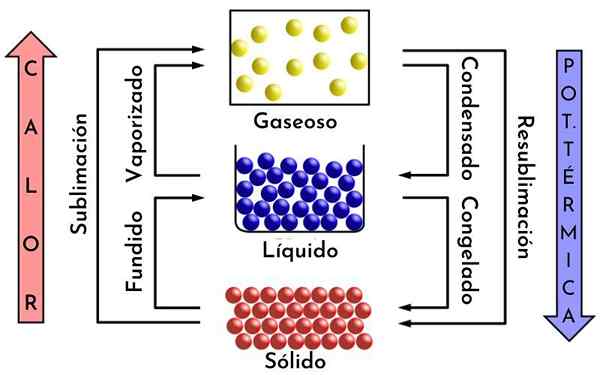
 Transformasjon av materie, et eksempel på delbarhet i kjemi. Kilde: Mikerun, CC BY-SA 4.0, Wikimedia Commons
Transformasjon av materie, et eksempel på delbarhet i kjemi. Kilde: Mikerun, CC BY-SA 4.0, Wikimedia Commons Hva er kjemisk delbarhet?
Vi kan definere Kjemisk delbarhet som en egenskap av materie som lar deg skille i mindre porsjoner. For å forstå konseptet kan vi gi et eksempel.
Hvis en isbit er smeltet, blir den vann, og når den blir utsatt for varme, blir den forvandlet til damp. Denne dampen kan deles på sin side til molekyler, og disse, til atomer.
Kjemisk delbarhet er da muligheten for å dele seg inn i stadig flere deler.
Opprinnelse og konsept for kjemisk delbarhet
I lang tid ble det diskutert hvis saken var sammensatt av partikler (det vi vet i dag som atomer), men den generelle ideen var at saken var et kontinuum som kunne deles.
Dette generaliserte konseptet gjorde et offer for hån mot strålende forskere som James Clerk Maxwell (av Maxwells ligninger) og Ludwig Boltzman (fra Boltzmans distribusjon) noe som dro den første til galskap og det andre til selvmord.
På 500 -tallet.C., Den greske filosofen Leucipo og hans demokritus -disippel brukte ordet atom for å utpeke det minste individuelle stykke materie, og foreslo at verden ikke består av mer enn å bevege atomer.
Denne tidlige atomteorien skilte seg fra senere versjoner, siden den inkluderte ideen om en menneskelig sjel sammensatt av en mer raffinert type atomet fordelt gjennom kroppen.
Atomteori falt i tilbakegang i middelalderen, men gjenopplivet i begynnelsen av den vitenskapelige revolusjonen i det syttende århundre.
Isaac Newton, for eksempel, mente at materie besto av "solide, massive, harde, ugjennomtrengelige og mobile partikler".
Kan tjene deg: Molekylær formel: Hvordan få det ut, eksempler og øvelserDelbarhet kan gis ved forskjellige metoder: det vanligste er delbarhet ved fysiske metoder, for eksempel å hakke et eple med en kniv.
Imidlertid kan delbarhet også gis ved kjemiske metoder, der materie vil bli separert i molekyler eller atomer.
Eksempler på kjemisk delbarhet
1. Oppløs salt
Når et salt oppløses, for eksempel, oppstår natriumklorid, i vann, oppstår et oppløsningsfenomen der de ioniske koblingene til salt er ødelagt:
NaCl → Na+ + Cl-
Ved å løse opp bare et saltkorn i vann, vil det bli separert i milliarder av natrium og kloridioner i løsning.
2. Oksidasjon av metaller i surt medium
Alle metaller, for eksempel magnesium eller sink, reagerer med syrer, for eksempel fortynnet saltsyre, for å gi hydrogenbobler og en fargeløs løsning av metallisk klorid.
Mg + hcl → mg2+ +Cl- + H2
Oxida til metallsyre ved å skille metallbindinger for å oppnå ioner i løsning.
3. Estere hydrolyse
Hydrolyse er brudd på en kjemisk binding ved hjelp av vann. Et eksempel på hydrolyse er hydrolyse av estere, der de er delt inn i to molekyler, en alkohol og en karboksylsyre.
4. Eliminasjonsreaksjoner
En eliminasjonsreaksjon gjør akkurat det den sier: den eliminerer atomene til et molekyl. Dette gjøres for å lage en karbon-karbon-dobbeltbinding. Dette kan gjøres ved hjelp av en base eller en syre.
Det kan oppstå i et enkelt samordnet trinn (abstraksjonen av protonet i Cα som oppstår samtidig som delingen av Cβ-X-koblingen), eller i to trinn (delingen av Cβ-X-koblingen skjer først for å danne En mellomliggende karbokasjon, som deretter "slår av" ved abstraksjon av protonet i alfakarbonet).
Kan tjene deg: darmstadtio: oppdagelse, struktur, egenskaper, bruk5. Aldolase enzymatisk reaksjon
I den preparative fasen av glykolyse er et glukosemolekyl delt inn i to glyseraldehydmolekyler 3-fosfat (G3P) ved bruk av 2 ATP.
Enzymet som har ansvaret for det snittet er aldolasen, som gjennom en omvendt kondens, deler 1,6-bifosfat fruktosemolekylet inn i et G3P-molekyl og et dihydroksyacetonfosfatmolekyl, som deretter isomeriseres for å danne en annen molekule av G3Pepe.
6. Nedbrytning av biomolekyler
Ikke bare glykolyse, men all nedbrytning av biomolekyler i katabolismreaksjoner, er eksempler på kjemisk delbarhet.
Dette skyldes det faktum at store molekyler som karbohydrater, fettsyrer og proteiner for å produsere mindre molekyler, for eksempel acetyl CoA, som kommer inn i Krebs -syklusen for å produsere energi i form av ATP.
7. Forbrenningsreaksjoner
Dette er et annet eksempel på kjemisk delbarhet, siden komplekse molekyler, som propan eller butan, reagerer med oksygen for å produsere CO₂ og vann:
C3H8 + 5. plass2 → 3CO2 + 4H2ENTEN
Nedbrytningen av biomolekyler kan sies at det er en forbrenningsreaksjon, siden sluttproduktene er co₂ og vann, men disse forekommer i mange trinn med forskjellige mellommenn.
8. Blodsentrifugering
Separasjonen av de forskjellige blodkomponentene er et eksempel på delbarhet. Til tross for å være en fysisk prosess, er eksemplet interessant, siden komponentene etter tetthetsforskjell er atskilt ved sentrifugering.
De tetteste komponentene, serumet med de røde blodlegemene, vil forbli i bunnen av sentrifugerøret, mens den mindre tette, plasmaet, vil forbli i den øvre delen.
Kan tjene deg: nøytralt atom9. Bikarbonatbuffer
Natriumbikarbonat, HCO3-, Det er den viktigste måten å transportere CO₂ i kroppsproduktet av metabolske nedbrytningsreaksjoner.
Denne forbindelsen reagerer med et middels proton for å produsere kullsyre, som deretter blir delt inn i CO₂ og vann:
HCO3- + H+ D h2Co3 D co₂ + h₂o
Siden reaksjonene er reversible, er dette en måte som kroppen har gjennom pust for å kontrollere den fysiologiske pH for å unngå alkalose- eller acidoseprosesser.
10. Nukleært atom- eller fisjonsdivisjon
I tilfelle at en massiv kjerne (som uran-235) er ødelagt (fisjon), vil føre til en netto energiytelse. Dette er fordi summen av massene til fragmentene vil være mindre enn massen av urankjernen.
I tilfelle at massen av fragmentene er lik eller større enn jern i toppen av koblingsenergikurven, vil de nukleære partiklene være nærmere koblet enn i urankjernen og at reduksjon i masse oppstår i energiform i henhold til til Einsteins ligning.
For elementer lettere enn jern vil fusjon produsere energi. Dette konseptet førte til opprettelsen av atombomben og kjernefysisk energi.
Referanser
- Reacions av syrer. BBC kom seg.co.Storbritannia.
- Foist, l. (S.F.). Eliminasjonsreaksjoner i organisk kjemi. Studie ble frisk.com.
- Nuclear Fision (s.F.). Gjenopprettet fra hyperfysikk.

