Elektrodialyse hvordan fungerer, fordeler, ulemper, bruker
- 2267
- 486
- Marius Aasen
De Elektrodialyse Det er ionebevegelsen gjennom en semipermeabel membran, drevet av en elektrisk potensialforskjell. Membranene som brukes i elektrodialyse har egenskapen til å være ionevekslere for kationer eller for anioner.
Kationutvekslingsmembraner har negative belastninger: de lar kationer passere og avvise anionene. I mellomtiden har anioniske utvekslingsmembraner en positiv ladning: de lar anionene og avvise kationer.
 Skjema for en pakke med fem elektrodialyseceller. Kilde: CommonShelper2 via Wikipedia.
Skjema for en pakke med fem elektrodialyseceller. Kilde: CommonShelper2 via Wikipedia. Elektrodialysekameraer eller celler er organisert i pakker med flere anion- og kationiske utvekslingsmembraner, som veksler med hverandre. Anioniske og kationiske utvekslingsmembraner avgrenser rommene der fortynning og konsentrasjonsprosesser for væsker blir utført.
Drivkraften til ionisk strømmer som krysser membranene til elektrodialyseceller er en forskjell i elektrisk potensial mellom en katode og en anode.
I mellomtiden, i motsatt osmose, skyldes strømmen av rommet med størst osmolaritet til det nedre osmolaritetsrommet en økning i hydrostatisk trykk, forårsaket av virkningen av en pumpe.
[TOC]
Hvordan fungerer i vannfortynning?
Beskrivelse av en pakke med fem elektrodialyseceller
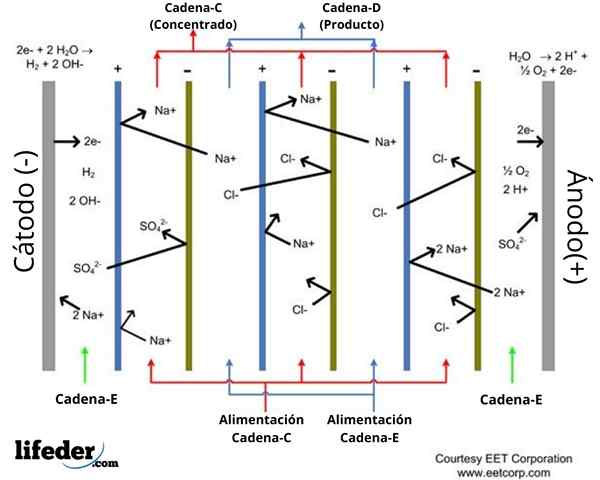
I ordningen vist (overlegen bilde) er plasseringen av seks ionebytte membraner indikert: tre kationutveksling og tre anionutveksling, som er ispedd hverandre. Disse membranene avgrenser fem rom der væsker involvert i elektrodialyse sirkulerer (se Røde og blålige piler).
Anioniske utvekslingsmembraner er positivt lastet, og vises i det blåfargede skjemaet. Disse lar anionene passere og avvise kationene for elektrostatisk frastøtning.
Kation -utvekslingsmembranene, mens, har en negativ belastning, som indikerer i det grønne ordningen. De krysses av kationer, men frastøter anionene.
Det kan tjene deg: Test: Kjennetegn, typer, eksempler på brukBegge typer membraner er vanntette til vann. Ordningen viser to mellomrom der en fortynning av saltinnholdet i vannet oppstår. I ordningen er de vandige strømningsstrømmene og utkjørselen til disse områdene indikert i blått, identifisert som strøm D.
I mellomtiden er det tre mellomrom der vann sirkulerer med høyt saltinnhold, og blir identifisert rødt. Inntekts- og utgangsstrømmer til disse rommene er angitt i ordningen som gjeldende C.
På samme måte er anoden (+) og katode (-) rom indikert i ordningen, gjennom hvilke strømmen og.
Elektrodialyseoperasjon
Kationene tiltrekkes av belastningen på katoden (-), mens de frastøt anoden (+). Anionene tiltrekkes av belastningen på anoden (+) og frastøttes av kattelasten (-).
Observasjonen, for eksempel av celler tre, fire og fem, indikerer følgende: I celler er tre og fem sirkulater konsentrert væske, mens i celle fire væske sirkulerer.
Ionet cl- av rom fire er tiltrukket av belastningen på anoden og krysser den anioniske utvekslingsmembranen som skiller den fra rom fem.
I mellomtiden naionen+ av rom fem blir frastøtt av den positive belastningen på anoden, men kan ikke gå inn i rommet fire. Dette er fordi membranen som skiller rom fire og fem er av anionisk utveksling, så den frastøter kationer.
På den annen side, NA+ av romfire er frastøtt av anoden (+) og krysser kationutvekslingsmembranen (-) som skiller den fra rommet tre.
Oppsummert: NA -konsentrasjon+ og cl- Fire rom har en tendens til å avta. Deretter reduserer saltvannskonsentrasjonen i fortynningsrom og økning i konsentrasjonsrom.
Det kan tjene deg: Applied Chemistry: Object of Study, grener, betydning, eksemplerFordeler og ulemper
Fordeler
-Elektrodialyse er enkel og kontinuerlig drift.
-Kjemisk behandling er ikke nødvendig for å regenerere utvekslingsmembraner.
-Det er lave driftskostnader og vedlikehold, og krever lite plass for driften.
Ulemper
-Partikler med en diameter større enn 1 um kan hindre ionebyttermembraner.
-Det anbefales ikke å bruke vann med en hardhet større enn 1, siden kalsiumkarbonat skaper en skorpe i konsentratceller.
-Krever karbondioksid eliminasjonsbehandling (CO2), siden dette når dissosiasjon kan endre vannkonduktivitet.
Forskjell mellom dialyse og elektrodialyse
Dialyse er vannstrøm gjennom en semipermeabel membran i det mindre osmolaritetsrommet til det større osmolaritetsrommet. Rommen med mindre osmolaritet har en større konsentrasjon av vannmolekyler.
Av denne grunn strømmer vann, til fordel for konsentrasjonsgradienten, av rommet med mindre osmolaritet til rommet med større osmolaritet.
Elektrodialyse er derimot en strøm av ioner gjennom en ionutvekslingsmembran som lar eller ikke passere til ioner, avhengig av den elektriske ladningen. Drivkraften til ionebevegelsen er en forskjell i elektrisk potensial.
I motsetning til dialyse, i elektrodialyse er det ingen vannstrøm gjennom membraner, og det er bare ionestrømmen.
Elektrodialyseapplikasjoner
Vanndemineralisering
Det er elektrodialyseplanter som behandler vann med høye salter for å produsere drikkevann. Elektrodialyse brukes også til å behandle avløpsvann fra hjemlig og industriell bruk, med det formål å gjøre dem egnet for etterfølgende forbruk.
Det kan tjene deg: Erlenmeyer Flask: Egenskaper, bruksområder, bruksmetoderSpesifikt brukes elektrodialyse i utvinningen av verdifulle metaller som er til stede i avløpsvannene i næringer. Det brukes også i fjerning av salter og syreoppløsninger, og ved separasjon av ioniske forbindelser av nøytrale molekyler.
Mat industri
Selv om elektrodialyse brukes i legemiddelindustrien, innen kosmetikk, så vel som i andre bransjer, er den mest utbredte bruken i matindustrien. Blant noen av applikasjonene dine kan vi nevne følgende:
-Smineralisering av serum og melasse
-Vin tartarsyrestabilisering
-Reduksjon i surheten i fruktjuicer
-Produksjon av vegetabilsk protein isolert
-Svikt i serumproteiner
-Demineralisering av soya- og fiskeoljer
-Eliminering av rødbeter alkaliske ioner og stokkemolasser
-Sjømatavfallsbehandling
-Demineralisering av drue må og potetjuice
-Konsentrasjon og utvinning av organiske syrer
-Soyaproduksjon
-Anriking av antioksidant
Referanser
- Whitten, Davis, Peck & Stanley. (2008). Kjemi. (8. utg.). Cengage Learning.
- Wikipedia. (2020). Elektrodialyse. Hentet fra: i.Wikipedia.org
- Lentech b.V. (2020). Hva er Edi? Gjenopprettet fra: Lentech.com
- Mondor m., Ippersiel d., Lamarche f. (2012) Elektrodialyse i matbehandling. I: BOYE J., Arcand og. (Eds) Grønne teknologier i matproduksjon og prosessering. Food Engineering Series. Springer, Boston, MA. gjør jeg.org/10.1007/978-1-4614-1587-9_12
- Akhter M, Habib G, Qamar Hans (2018) anvendelse av elektrodiasis i behandling av avløpsvann og påvirkning av begroing på prosessytelse. J Memb Sci Technol 8: 182. Doi: 10.4172/2155-9589.1000182
- H. Strathmann. (6. desember 2006). Elektrodiasis og dens anvendelse i den kjemiske prosessindustrien. Taylor & Francis online. gjør jeg.org/10.1080/03602548508068411
- « Tredje person utarbeidelse av egenskaper og eksempler
- De 8 eksemplene på mest relevante grafiske ressurser »

