Kjemisk element
- 852
- 32
- Jonathan Moe
Vi forklarer hva et kjemisk element er, dets egenskaper, typene som finnes, og vi gir flere eksempler
 Et kjemisk element er en komponent som ikke kan deles og har unike egenskaper annet enn noe annet eksisterende materiale
Et kjemisk element er en komponent som ikke kan deles og har unike egenskaper annet enn noe annet eksisterende materiale Hva er et kjemisk element?
EN Kjemisk element Det kan defineres som en sak eller komponent som ikke kan deles, og som har unike egenskaper annet enn noe annet eksisterende materiale. I henhold til egenskapene til hvert element kan de være mer eller mindre knappe og verdifulle.
For at et kjemisk element skal defineres som sådan, må det oppfylle kjennetegn ved å være udelelig. Det vil si at det ikke kan deles opp i mindre porsjoner. Disse delene som ikke lenger kan deles, er det som kalles atomer.
Noen av de kjemiske elementene kan dele forbindelser til felles, noe som gjør det nært og forholdet mellom disse. Imidlertid har de mange andre deler som ikke deler med andre elementer som definerer seg selv så vel som unike.
Disse kjemiske materialene kan være i fast eller gassformig tilstand og finnes forskjellige steder og miljøer rundt planeten. Selv vitenskapelige studier har funnet denne typen stoffer i elementer utenfor Jorden, for eksempel asteroider eller andre fjerne planeter.
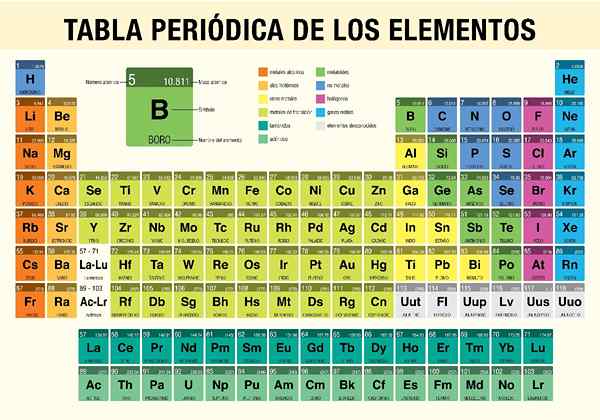
118 Kjemiske elementer er for tiden kjent og er organisert i henhold til antall atomer og egenskaper i det som er kjent som periodiske tabell.
Typer kjemiske elementer
I naturen kan de kjemiske elementene definert ovenfor bli funnet; Imidlertid kan mange av disse være rene eller bør bli med andre for å danne nye kjemiske materialer, og dermed gi opphav til klassifiseringen av disse forbindelsene.
Blant typene kjemiske elementer er det fire store grupper, som vil bli forklart nedenfor. Imidlertid er det andre mer spesifikke undergrupper av denne typen elementer som også vil bli utsatt.
Metaller
De er komponenter som stort sett er i solid tilstand, og på grunn av egenskapene deres er de veldig god varme- og strømledere. I tillegg er de elementer som har en karakteristisk lysstyrke, som varierer intensiteten i henhold til hvert individ.
Kan tjene deg: Hva er den mekaniske ekvivalenten til varme?Stoffer klassifisert som metaller er også preget av å være veldig håndterbare og duktile, og slik at de enkelt kan transformere eller bli med i andre kjemiske elementer.
Innenfor metallelementene er det seks undergrupper som er:
- Actinider
- Lantanider
- Overgangsmetaller
- Alkalisk
- Alkalisk-terreos
- Andre metaller.
Ingen metaller
Disse komponentene er stort sett i fast tilstand; Til tross for dette skiller de seg fra metaller, siden de ikke er god varme- eller strømledere og ikke har den karakteristiske lysstyrken til sistnevnte.
I tillegg er de komponenter som ikke har duktilitet og enkel håndtering av metaller, så det å transformere dem er en mye mer kompleks prosess.
Metalloider
Det kan sies at disse komponentene er en kombinasjon mellom metall og ikke -metallelementer, og deler egenskaper for begge gruppene. Noen av disse tillater delvis ledning av strøm og varme, og deres duktilitet kan være større eller mindre, avhengig av det kjemiske elementet.
Edle gasser
De er kjemiske materialer som finnes i naturen i gassformig tilstand og er komponenter med veldig spesielle egenskaper og forskjellige fra noe annet eksisterende gassform.
Disse elementene anses som ganske stabile og gjør ikke kjemiske modifikasjoner eller reaksjoner med andre elementer for å lage nye stoffer.
Periodiske egenskaper
Som nevnt ovenfor, er alle eksisterende kjemiske elementer klassifisert som det som er kjent som en periodisk tabell. Denne tabellen er ikke annet enn et organisert opplegg som plasserer av grupper (vertikalt) og perioder (horisontalt) hvert av de kjemiske forsøkspersonene i henhold til deres egenskaper.
Å være tydelig på det periodiske tabellen, periodiske egenskaper kan deretter defineres. De sistnevnte er de egenskapene eller særegenheter som definerer hvert kjemisk element og på sin side etablere sin beliggenhet i det periodiske tabellen.
Kan tjene deg: amorf karbon: hva er, typer, egenskaper, bruksområderDet er fire viktigste periodiske egenskaper:
Elektronegativitet
Denne egenskapen kan defineres som kapasiteten til en bestemt kjemisk komponent for å tiltrekke eller koble til andre kjemiske elementer. Med andre ord, elektronegativitet er kraften som atomene til en spesifikk komponent har, for å tiltrekke seg atomer av et annet element.
Innen den periodiske tabellen er elementene som øker elektronegativiteten plassert fra venstre til høyre i periodene og i de oppadgående gruppene.
Atomisk radio
Atomisk radioegenskap er ikke annet enn referansen til størrelsen på atomene som utgjør hvert kjemisk element. Det vil si at hvert individ har et visst antall atomer med forskjellige størrelser.
I den periodiske tabellen er de plassert fra topp til bunn når størrelsen på atomradius øker i gruppene og i periodene synker.
Affinitet eller elektronisk struktur
Denne egenskapen kan defineres som energiendring som et element oppnår i sin atomstruktur ved å ha noen endringer innenfor det samme.
Innen den periodiske tabellen er de lokalisert i samme gruppe, siden de har til felles denne atomstrukturen.
Ioniseringspotensial
Dette refererer til energien som kreves av atomstrukturen til et bestemt element for å endre sin status.
I den periodiske tabellen er klassifiseringen gitt i en gruppe ved å avta fra topp til bunn og i periodene øker fra venstre til høyre.
Det er andre sekundære periodiske egenskaper som elektropositivitet, atomtetthet, atomvolum, fusjonstemperatur og koketemperatur.
Kan tjene deg: kjemisk konsentrasjonEksempler på kjemiske elementer
Som nevnt er det for øyeblikket 118 kjemiske elementer identifisert. Disse elementene har et unikt navn og symbol som identifiserer dem ikke bare innen den periodiske tabellen, men også i det vitenskapelige feltet for kjemi.
Deretter vil 50 av disse elementene bli presentert med navn og identifikasjonssymboler, som er en del av de fire typene elementer som er nevnt ovenfor.
- Oksygen (o)
- Fluor (f)
- Neon (ne)
- Natrium (na)
- Magnesium (Mg)
- Aluminium (Al)
- Silisium (ja)
- Fosfor (P)
- Svovel (er)
- Klor (CL)
- Xenón (xe)
- Cesio (CS)
- Barium (BA)
- Lantano (LA)
- Cerio (CE)
- Prasodimio (PR)
- Neodimium (ND)
- Prometio (PM)
- Samario (SM)
- Europio (EU)
- Renio (re)
- Osmio (OS)
- Ididio (IR)
- Platinum (PT)
- Gull (AU)
- Kvikksølv (HG)
- Talio (TL)
- Bly (PB)
- Vismut (bi)
- Polonio (PO)
- Astato (at)
- Radon (RN)
- Francio (FR)
- Radio (RA)
- Actinio (AC)
- Torio (TH)
- Protacinium (PA)
- Uran (u)
- Neptunio (NP)
- Plutonium (PU)
- Dubnium (DB)
- Seaborgio (SG)
- Bohrio (BH)
- Hassio (HS)
- Meitnerio (MT)
- Darmstatio (DS)
- Roentgenio (RG)
- Copernicio (CN)
- Flerovio (FL)
- Livermoorio (LV)
Referanser
- Ball, s. (2019). Hva er et element? Hentet fra kjemiworld.com
- Periodic Table (2018). Oppnådd fra RSC.org
- Periodic Table of Elements (2019). Hentet fra Pubchem.NCBI.NLM.NIH.Gov
- Periodic Table of the Elements (2018). Hentet fra Sigmaaldrich.com
- Hvilke arementer? (2020). Hentet fra BBC.co.Storbritannia

