Metabolsk energi
- 897
- 82
- Markus Fredriksen
Hva er metabolsk energi?
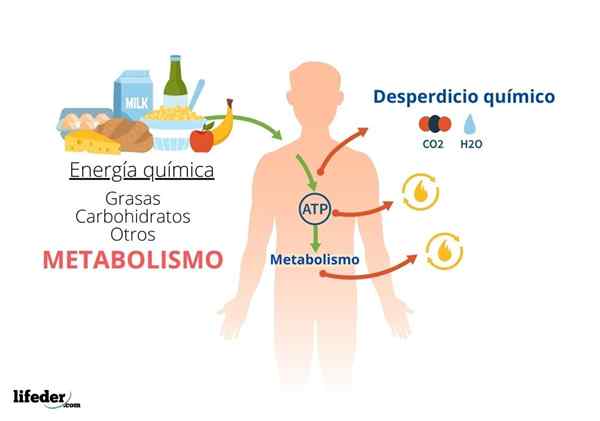
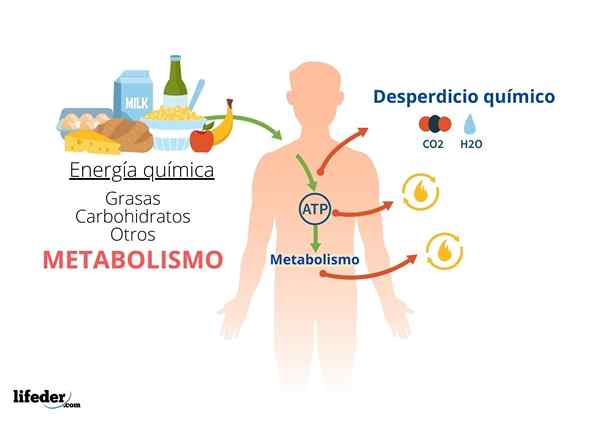
De Metabolsk energi Det er energien som er oppnådd av alle levende vesener fra den kjemiske energien i mat (eller næringsstoffer). Denne energien er i utgangspunktet den samme for alle celler; Måten å få er imidlertid veldig mangfoldig.
Mat blir dannet av en serie biomolekyler av forskjellige typer, som har kjemisk energi lagret i sine koblinger. På denne måten kan organismer dra nytte av mat som er lagret i mat og deretter bruke denne energien i andre metabolske prosesser.
Alle levende organismer trenger energi for å vokse og reprodusere, opprettholde sine strukturer og svare på miljøet. Metabolisme omfatter de kjemiske prosessene som støtter livet og som lar organismer transformere kjemisk energi til nyttig energi for celler.
Hos dyr bryter metabolismen ned karbohydrater, lipider, proteiner og nukleinsyrer for å gi kjemisk energi. For deres del omdanner planter solens belysning til kjemisk energi for å syntetisere andre molekyler; Dette gjøres under fotosynteseprosessen.
Typer metabolske reaksjoner
Metabolisme inkluderer flere typer reaksjoner som kan grupperes i to store kategorier: nedbrytningsreaksjonene til organiske molekyler og synteseaksjonene til andre biomolekyler.
Katabolisme
Metabolske nedbrytningsreaksjoner utgjør cellekatabolisme (eller katabolske reaksjoner)). Disse involverer oksidasjon av energi -rike molekyler, for eksempel glukose og annet sukker (karbohydrater). Når disse reaksjonene frigjør energi, kalles de eksergonisk.
Anabolisme
I motsetning til dette utgjør synteseaksjoner celleanabolisme (eller anabole reaksjoner))). Disse utfører molekyler reduksjonsprosesser for å danne andre rike på lagret energi, for eksempel glykogen. Fordi disse reaksjonene konsumerer energi, kalles de ender som gir.
Metabolske energikilder
De viktigste kildene til metabolsk energi er:
- Glukosemolekyler.
- Fettsyrer.
Disse utgjør en gruppe biomolekyler som raskt kan oksideres for å oppnå energi.
Glukosemolekyler kommer stort sett fra karbohydrater inntatt i kostholdet, som ris, brød, pasta, blant andre derivater av rike grønnsaker i stivelse. Når det er lite blodsukker, kan det også fås fra glykogenmolekylene som er lagret i leveren.
Under langvarig faste, eller i prosesser som krever ytterligere energiforbruk, kreves denne energien fra fettsyrer som mobiliseres fra fettvev.
Disse fettsyrene lider av en serie metabolske reaksjoner som aktiverer dem, og lar transport til det indre av mitokondriene der de blir oksidert. Denne prosessen kalles ß-oksidasjon av fettsyrer og gir opptil 80 % ekstra energi under disse forholdene.
Proteiner og fett er den siste reserven som syntetiserer nye glukosemolekyler, spesielt i ekstreme faste tilfeller. Denne reaksjonen er av den anabole typen og er kjent som glukoneogenese.
Kjemisk energitransformasjonsprosess til metabolsk energi
De komplekse matmolekylene som sukker, fett og proteiner er rike energikilder for celler, fordi mye av energien som brukes til å danne disse molekylene er bokstavelig talt lagret i de kjemiske bindingene som holder dem sammen.
Forskere kan måle mengden energi som er lagret i mat ved hjelp av en enhet som kalles kalorimetrisk pumpe. Med denne teknikken plasseres maten inne i kalorimeteret og varmes opp til den brenner. Overflødig varme frigitt ved reaksjon er direkte proporsjonal med mengden energi som er i mat.
Realiteten er at celler ikke fungerer som kalorimeter. I stedet for å brenne energi i en stor reaksjon, frigjør celler energien som er lagret i matmolekyler sakte gjennom en serie oksidasjonsreaksjoner.
Kan tjene deg: Nukleinsyrer: Kjennetegn, funksjoner, strukturOksidasjon
Oksidasjon beskriver en type kjemisk reaksjon der elektroner overføres fra ett molekyl til et annet, og endrer sammensetningen og energiinnholdet i giver- og akseptormolekylene. Matmolekyler fungerer som elektroners givere.
Under hver oksidasjonsreaksjon involvert i nedbrytning av mat, har reaksjonsproduktet et lavere energiinnhold enn givermolekylet som gikk foran det på ruten.
Samtidig fanger elektron som aksepterer molekyler en del av energien som er tapt fra matmolekylet under hver oksidasjonsreaksjon og lagrer den for senere bruk.
Etter hvert, når karbonatomer i et komplekst organisk molekyl blir fullstendig oksidert (på slutten av reaksjonskjeden) frigjøres de i form av karbondioksid.
Cellene bruker ikke energien til oksidasjonsreaksjoner så snart den frigjøres. Det som skjer er at de gjør det til små og rike molekyler i energi, for eksempel ATP og NADH, som kan brukes i hele cellen for å øke metabolismen og bygge nye cellulære komponenter.
Reserve energi
Når energi er rikelig, skaper eukaryote celler større og energirike molekyler for å lagre denne overflødige energien.
De resulterende sukker og fett holdes i avsetninger inne i cellene, hvorav noen er store nok til å være synlige i elektroniske mikrografer.
Dyreceller kan også syntetisere forgrenede glukose (glykogen) polymerer, som igjen tilsettes i partikler som kan observeres ved elektronisk mikroskopi. En celle kan raskt mobilisere disse partiklene når du trenger rask energi.
Kan tjene deg: Biologisk evolusjon: Teorier, prosess, tester og eksemplerUnder normale omstendigheter lagrer mennesker imidlertid tilstrekkelig glykogen til å gi en energidag. Planteceller produserer ikke glykogen, men produserer forskjellige glukosepolymerer kjent som stivelse, som er lagret i granuler.
I tillegg holder både planteceller og dyr energi ved å utlede glukose på fettsynteseveier. Et gram fett inneholder nesten seks ganger energien med samme mengde glykogen, men fettenergi er mindre tilgjengelig enn glykogen.
Likevel er hver lagringsmekanisme viktig fordi celler trenger energiavsetninger både på kort og lang sikt.
Fett er lagret i dråper i cellcytoplasma. Mennesker lagrer generelt nok fett til å levere cellene sine i flere uker.
Referanser
- Alberts, f., Johnson, a., Lewis, J., Morgan, d., Raff, m., Roberts, k. & Walter, P. (2014). Biologi av cellemolekylæren (6. utg.). Garland Science.
- Berg, J., Tymoczko, J., Gatto, g. & Strayer, l. (2015). Biokjemi (8. utg.). W. H. Freeman og selskap
- Campbell, n. & Reece, J. (2005). Biologi (2. utg.) Pearson Education.
- Lodish, h., Berk, a., Kaiser, ca., Krieger, m., Bretscher, a. , Ploegh, h., Amon, a. & Martin, K. (2016). Molekylær cellebiologi (8. utg.). W. H. Freeman og selskap.
- Purves, w., Sadava, d., Oruser, g. & Heller, h. (2004). Livet: Biologiens vitenskap (7. utg.). Sinaauer Associates og W. H. Freeman.
- Solomon, e., Berg, l. & Martin, D. (2004). Biologi (7. utg.) Cengage Learning.
- Voet, d., Voet, J. & Pratt, C. (2016). Grunnleggende om biokjemi: Livet på molekylært nivå (5. utg.). Wiley.