Fenoler eller fenolforbindelser egenskaper, typer, applikasjoner

- 1742
- 426
- Theodor Anders Hopland
De Fenoler De er en familie av organiske forbindelser (alkoholer) som er preget av å ha en aromatisk ring der ett eller flere av hydrogenatomer assosiert med karbonatomene i ringen erstattes av en eller flere hydroksylgrupper (-OH).
Fenolene og deres derivater er normalt til stede i naturen, fordi de som organiske molekyler produseres praktisk talt av alle levende vesener.
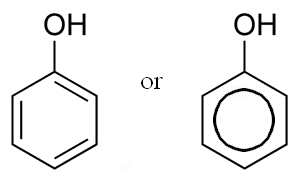 Kjemisk struktur av fenol, den enkleste fenolforbindelsen (Kilde: Dbenbenn, via Wikimedia Common)
Kjemisk struktur av fenol, den enkleste fenolforbindelsen (Kilde: Dbenbenn, via Wikimedia Common) Blant de vanligste eksemplene på fenoler kan vi nevne aminosyren tyrosin, en av de 20 proteinaminosyrene, som har den substituentgruppen en fenolisk ring; De har også fenolgrupper adrenalin og serotonin, to veldig viktige hormoner for pattedyrdyr.
Planter er "lærerne" i produksjonen av fenolforbindelser, siden mange av deres sekundære metabolitter (grunnleggende for deres vekst, reproduksjon, beskyttelse osv.) De har en eller flere av disse kjemiske gruppene i sine strukturer, som vanligvis stammer fra metabolske ruter som pentosefosfat, den fra Shiquimato og fenylpropanoider.
 Tyrosine aminosyrestruktur, hvis gruppe R er en fenolring (benzen + OH) (kilde: Neurotokeker, via Wikimedia Commons)
Tyrosine aminosyrestruktur, hvis gruppe R er en fenolring (benzen + OH) (kilde: Neurotokeker, via Wikimedia Commons) Fenolene har blitt studert mye på grunn av egenskapene de viser i møte med oksidativt stress (som antioksidanter) hos mennesker, spesielt hos de som lider av metabolske patologier som overvekt, diabetes eller noe kardiovaskulær tilstand.
Med disse antioksidantegenskapene skiller α-tokoferol seg ut, en fenolsderivatkomponent av vitamin E, som er til stede i blodplasma og er i stand til å "fange" gratis peroksydradikaler som er potensielt skadelige for celler for celler.
I tillegg har mennesket i den menneskeskapte sammenheng "lært" å utnytte egenskapene til fenolforbindelser fra det industrielle synspunktet for produksjon av fargestoffer, polymerer, medisiner og andre organiske stoffer med et bredt utvalg av forskjellige bruksområder og egenskaper , selv om mange av disse dessverre representerer viktige kilder til miljøforurensning.
[TOC]
Egenskaper til fenoler
Fenolforbindelser har stort mangfold av fysisk -kjemiske egenskaper, som er direkte relatert til deres gunstige egenskaper for dyre- og planteceller.
Hydroksylgruppene til fenolene bestemmer deres surhet, mens deres benterniske ring (den aromatiske ringen) bestemmer dens grunnleggende. Fra det fysisk -kjemiske synspunktet kan vi si at fenoler:
- De er forbindelser med et lavt smeltepunkt.
- I tillegg til all annen alkohol, har fenoler hydroksylgrupper som er i stand til å delta i intermolekylære hydrogenbindinger (hydrogenbroer), enda sterkere enn de som kan danne andre alkoholer.
- Når de krystalliserer, danner disse forbindelsene en slags krystaller som fargeløse "prismer" som har en karakteristisk gjennomtrengende lukt.
Kan tjene deg: ovalbumin: struktur, funksjoner, denaturering- Når du smelter, danner fenoler krystallinske "mobile" væsker (fargeløs).
- Takket være det faktum at de kan danne hydrogenbroer, kan disse forbindelsene være veldig oppløselige i vann, noe som avhenger av temperaturen og generelle egenskaper til de andre gruppene de er assosiert.
- De blir raskt oppløst i de fleste organiske løsningsmidler, spesielt hos de hvis sammensetning består av aromatiske hydrokarboner, alkoholer, ketoner, etere, syrer, halogenerte hydrokarboner, etc. (som også avhenger av den generelle strukturen til molekylet som huser fenolgruppene).
- De har et frysepunkt på omtrent 40 ° C.
- Dens molekylvekt varierer mellom 94 og 100 g/mol.
Celler
Når det gjelder celler, er derimot fenolforbindelser preget av:
- Være antioksidantforbindelser, siden de har redusert egenskaper, og fungerer som "givere" agenter for hydrogen eller elektroner (de fungerer som "kidnappere" av frie radikaler).
- Være chelars av metallioner, spesielt jern og kobber, undertrykke dannelsen av frie radikaler katalysert av metaller.
- Ha antimikrobiell aktivitet, da de er i stand til å utsette invasjonen av mikrober og forhindre råte og vegetabilsk råte (slik at de også er industrielt utnyttet).
Klassifisering: Typer fenoler
Avhengig av konteksten, kan fenoler klassifiseres på forskjellige måter, men den mest brukte kjemiske klassifiseringen er basert på antall hydroksylgrupper (-OH) som binder seg til den samme aromatiske ringen (erstatter et hydrogenatom). I denne forstand er de blitt definert:
- Fenoler monohydric, Med en enkelt hydroksylgruppe
- Fenoler Dihydrier, Med to hydroksylgrupper
- Fenoler trihydrisk, Med tre hydroksylgrupper
- Fenoler Polyhydric, Med mer enn tre hydroksylgrupper
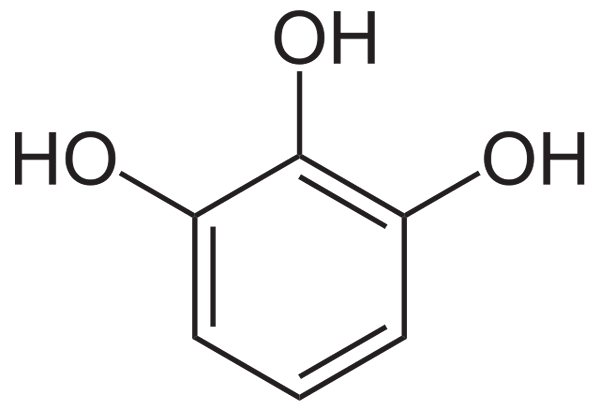 Pyrogalol (trihydroxyphenol), en fenolforbindelse som ofte brukes til produksjon av kapillære fargestoffer, som et antiseptisk og som et "utvikler" -midler i White-Negro Developers (kilde: Neurotoger / Public Domain, via Wikimedia Commons via Wikimedia)
Pyrogalol (trihydroxyphenol), en fenolforbindelse som ofte brukes til produksjon av kapillære fargestoffer, som et antiseptisk og som et "utvikler" -midler i White-Negro Developers (kilde: Neurotoger / Public Domain, via Wikimedia Commons via Wikimedia) Disse organiske forbindelsene kan være enkle fenolmolekyler eller polymeriserte forbindelser med stor kompleksitet, og det er vist at de fleste av fenolene som finnes i naturen forekommer som mono- og polysakkaridkonjugater, av estere og metylestere.
Det skal bemerkes at andre klassifiseringer også er relatert til den "ikke -fenoliske delen" av forbindelsene, men dette avhenger i stor grad av kilden til å oppnå (naturlig eller kunstig).
Ekstraksjonsmetoder
Fenolene ble oppdaget i 1834 av Friedlieb Runge, som isolerte fenol (Den enkleste fenolforbindelsen) fra mineral tjæreprøver og kalte den "karbolsyre" eller "kullolje" syre ". Imidlertid ble den rene fenol utarbeidet av Auguste Laurent noen år senere, i 1841.
Kan tjene deg: dyre- og planteorganogenese og dens egenskaperFor tiden er små mengder fenol fremdeles isolert fra Tarry og Coke Plants (planter sprekker). Imidlertid involverer mange syntetiske metoder både i fortiden og i dag syntese av fenol fra benzen som forløperring, til tross for at det er en ekstremt flyktig og kreftfremkallende forbindelse.
Syntesen av disse forbindelsene fra benzen kan være fin ved hydrolyse av klorbenzen eller oksidasjon av isopropylbenzen (cumeno).
- Utdrag
Et stort antall fenolforbindelser av naturlig opprinnelse blir trukket ut fra preparater fra forskjellige deler av anatomi av grønnsaker. Dessverre er det ingen standardiserte protokoller for dette formålet, fordi mye avhenger av formålet med ekstraksjon, typen vev, den spesielle klassen av fenol, blant andre faktorer.
Prøveforberedelse
Generelt er prøvene tidligere fremstilt gjennom teknikker som tørking eller dehydrering, knust, homogenisering eller filtrering.
Det må tas med i betraktningen at når man trekker ut fenoler av planteprøver, oppnås en kompleks blanding av fenolforbindelser av forskjellige klasser faktisk, spesielt de som har egenskaper som gjør dem mer løselige i løsningsmidlene som brukes til dette formålet.
Ekstraksjonsteknikker
Ekstraksjonen, når prøvene er oppnådd og er utarbeidet for dette formålet, blir vanligvis utført ved inkubering av prøvene oppnådd i organiske løsningsmidler, der den organiske fasen ofte blir renset gjennom metoder som faste faseekstraksjon, kolonnekromatografi og motstrøms dropperkromatografi.
I tillegg til løsningsmiddelekstraksjon, involverer andre teknikker bruk av ultralyd, mikrobølgeovn eller presurisert og superkritiske væsker.
Fenoler applikasjoner
Fenolene har flere applikasjoner, både de som er isolert fra levende organismer og de som er kunstig syntetisert.
I matproduksjon
Matindustrien bruker mange fenolforbindelser for å "styrke" produkter, øke halvdelen av noen matvarer og til og med være en del av de aktive ernæringsforbindelsene av dem.
Hovedårsaken til at de er så nyttige er fordi de har vist seg å være god "bi -trykker" for forgjengelige matvarer, og i tillegg tillater de matproduksjon uten behov for å bruke syntetiske tilsetningsstoffer som kan ha negative innvirkninger på forbrukerhelse.
Industrielle anvendelser av noen syntetiske fenoler
Fenolen, som er en av de enkleste fenolforbindelsene og mest forurensende, oppnås fra mineraltjære og noen syntetiske metoder, og brukes ofte til produksjon av:
Kan servere deg: primær buljong eller primitiv suppe- Utleie (for ugressmidler og plast)
- Cresoles (for løsningsmidler)
- Xilenoles (for fremstilling av antioksidanter og redoksindikatorer)
- fenolharpikser
- Aniliner (for fremstilling av polyuretan, malerier, ugressmidler, lakk osv.)
- Tekstilfargestoffer
- Eksplosiver
- plantevernmidler, etc.
Klorfenoler, som er den største gruppen av fenoler, brukes til syntese av desinfeksjonsmidler, ugressmidler og plantevernmidler. Disse leder listen over miljøforurensninger, vann- og landbruksprodukter.
Bruk av noen naturfenoler
Mange fenolforbindelser av naturlig opprinnelse er daglige ansatte i legemiddel- og medisinsk industri for behandling og forebygging av patologier som kreft. Disse forbindelsene er isolert fra urter og medisinplanter og omfatter en serie fenolsyrer, flavonoider, tanniner, curcuminoider, lignaner, kinoner, etc.
Mange av disse forbindelsene er aktive, så som antioksidanter, anti -karsinogene, antimutagene og til og med anti -inflammatorier.
Det er vist at noen av disse kan indusere programmert celledød eller "arrestasjonen" av cellesyklusen, samt regulere metabolisme, celleadhesjon, migrasjon og spredning, så de er potensielt gunstige for behandling av svulster.
 2,3-hydroksykinaminsyre, en fenol til stede som en metabolitt i humant urin (kilde: ED (Edgar181) / Public Domain, via Wikimedia Commons)
2,3-hydroksykinaminsyre, en fenol til stede som en metabolitt i humant urin (kilde: ED (Edgar181) / Public Domain, via Wikimedia Commons) Mat med fenolforbindelser
Siden mange sekundære metabolitter produsert av planter har et stort antall fenolforbindelser, er de fleste grønnsakene vi bruker daglig rike på disse.
På samme måte har alle celleproteiner (av dyr, grønnsaker og sopp) forskjellige andeler av tyrosin, aminosyreproteinet med en fenolisk ring.
 Free-the Image in www.Pixabay.com
Free-the Image in www.Pixabay.com Blant de viktigste rike matfenolene og/eller dens derivater skiller seg ut:
- oliven
- Druer
- Et stort antall frukt og grønnsaker
- ris
- De aromatiske krydderne (oregano, pepper, koriander, kino, kanel, lukt negler, sennep, ingefær, anis, gurkemeie, mynte, etc.)
- urtene
- Te og kaffe
- tang
- nøtter og andre nøtter
- vinen
- sjokoladen
- Belgfrukter og andre frø
Referanser
- Bento, c. & Gonçalves, Ana Carolina & Jesus, Fábio & Simões, Manuel & Silva, Luis. (2017). Fenolforbindelser: Kilder, egenskaper og applikasjoner.
- Michałowicz, J., & Tvil, w. (2007). Fenoler-kilder og toksisitet. Polish Journal of Environmental Studies, 16 (3).
- Minatel, i. ENTEN., Borges, c. V., Ferreira, m. Yo., Gomez, h. TIL. G., Chen, c. OG. ENTEN., & Lima, g. P. P. (2017). Fenolforbindelser: Funksjonsegenskaper, virkning av prosessering og biotilgjengelighet. Fenolforbindelser biologisk aktivitet. Ed. Intech. Rijaka, Kroatia, 1-24.
- Santos-Buelga, ca., Gonzalez-Manzano, s., Dueñas, m., & Gonzalez-paramas, a. M. (2012). Ekstraksjon og isolasjon av fenolske kompundasjoner. I naturlige produkter isolering (pp. 427-464). Menneskelig presse.
- Serie, s. (2003). Kjemien til funksjonell gruppe. Kjemien til fenoler, Ed. Z. Rappoport.
- Tyman, J. H. (nitten nittiseks). Syntetiske og naturfenoler. Elsevier.
- Vuolo, m. M., Lima, v. S., & Junior, m. R. M. (2019). Fenolforbindelser: Struktur, klassifisering og antioksidantkraft. I bioaktive forbindelser (pp. 33-50). Woodhead Publishing.
- Wade, l. (2018). Britannica Encyclopaedia. Hentet 6. mai 2020 fra Britannica.com
- « Sosiale institusjoner dukker opp, egenskaper, funksjoner, eksempler
- Bly nitratkonstruksjon, egenskaper, innhenting, bruker »

