Kaliumfosfat (K3PO4) struktur, egenskaper, bruk

- 1961
- 155
- Markus Fredriksen
Han Kaliumfosfat Det er en uorganisk forbindelse dannet av tre ioner kalium k+ og et fosfation po43-. Den kjemiske formelen er k3Po4. Det er et fargeløst fast eller krystallinsk hvitt. Det er veldig løselig i vann, og danner alkaliske løsninger, det vil si med mange OH -ioner-, Derfor, grunnleggende pH.
Fosfation har en viktig funksjon i celler som har med energilagring å gjøre. Kaliumfosfat er mye brukt i organiske kjemiske reaksjoner der det kan fungere som en base, det vil si å ta protoner h+. Det kan også fungere som en katalysator eller akselerator for noen reaksjoner.
 Kaliumfosfat k3Po4 fast. Xavier13540 på Chinese Wikipedia [Public Domain]. Kilde: Wikimedia Commons.
Kaliumfosfat k3Po4 fast. Xavier13540 på Chinese Wikipedia [Public Domain]. Kilde: Wikimedia Commons. Det har blitt brukt til å redusere angrepet av visse insekter i hveteplanter fordi det gjør dem mer motstandsdyktige mot disse. Imidlertid har det blitt observert at det favoriserer løsgjøringen av metan (CH4), En klimagass, rismikrokulturer.
Det har blitt brukt som avføringsmiddel, for å øke varigheten av lokalbedøvelse, for å stoppe karies og for å hjelpe til med å dekke overflater, blant andre applikasjoner.
[TOC]
Struktur
Kaliumfosfat består av tre kationer kalium k+ og en fosfatanion po43-.
Fosfation Po43- Det dannes av et fosfor (P) atom og fire oksygen (O) atomer, hvor fosfor har en oksidasjonstilstand på +5 og oksygen en valens på -2 -2.
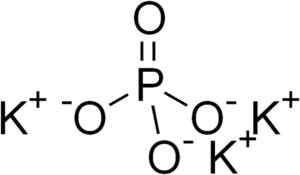 Kaliumfosfatstruktur k3Po4. Edgar181 [offentlig domene]. Kilde: Wikimedia Commons.
Kaliumfosfatstruktur k3Po4. Edgar181 [offentlig domene]. Kilde: Wikimedia Commons. Nomenklatur
- Kaliumfosfat
- Tripotasiumfosfat
- Kaliumtribasisk fosfat
- Tripotasium -ortofosfat
Egenskaper
Fysisk tilstand
Fargeløs fast eller krystallinsk hvit.
Molekylær vekt
212,27 g/mol
Smeltepunkt
1340 ºC
Tetthet
2.564 g/cm3
Løselighet
Veldig løselig i vann: 106 g/100 g vann ved 25 ° C. Uoppløselig i etanol.
Ph
En løsning med 1% k3Po4 Den har en pH på 11,5-12,3.
Kjemiske egenskaper
Ved å løse opp i vann, blir kaliumfosfat separert i de tre kationene kalium k+ og fosfatanionen PO43-. Fosfatanionen tar et proton av vann og HPO -hydrogenofosfatanionen dannes42-. Sistnevnte tar på sin side en annen proton av vann og blir dihydrogenofosfat H -anion2Po4-.
Kan tjene deg: Hvordan syntetiseres et elastisk materiale?Po43- + H2Eller ⇔ HPO42- + Åh-
Hpo42- + H2Eller ⇔ h2Po4- + Åh-
Når formioner oh- Den vandige oppløsningen blir alkalisk.
Andre egenskaper
I tillegg til den vannfrie formen (uten vann), har den flere hydratiserte former; Dette betyr at K -molekylet3Po4 Det kan ledsages av ett eller flere vannmolekyler i den krystallinske strukturen.
Av denne grunn kan du danne for eksempel k monohydrat3Po4.H2Eller3Po4.3H2Eller, hepthydrat og ikke -dehydrat.
Fosfatfunksjon i den menneskelige organismen
Fosfation Po43- Det er den mest tallrike anionen inne i cellene og utøver en viktig funksjon innen energilagring.
Fosfationet deltar også i dannelse og ernæringsaktiviteter av bein og tenner, da det regulerer konsentrasjonen av kalsium på blodserum og i en rekke energioverføringsreaksjoner i cellen.
Å skaffe
Kaliumfosfat kan oppnås fra reaksjonen mellom KCl kaliumklorid og ammoniumfosfat (NH4)3Po4.
Kaliumklorid + ammoniumfosfat → Kaliumfosfat + ammoniumklorid
3 KCl + (NH4)3Po4 → K3Po4 + 3 nh4Cl
applikasjoner
Som grunnlag i organiske kjemiske reaksjoner
Kaliumfosfat k3Po4 Det har blitt brukt i flere organiske kjemiske reaksjoner. For eksempel tjener det i syntesen av acetylener basert på dibromede forbindelser.
I denne syntesen oppstår det en dehydrobromasjon (eliminering av hydrogen og brom), hvor k3Po4 Ashidro fast (uten vann) fungerer som en myk base og tar to protoner fra molekylet, de to bromatomene elimineres og den tilsvarende acetylen oppnås.
C6H5-Chbr-ch2Br + 2 K3Po4 → c6H5-C≡CH + 2 KBr + 2 K2Hpo4
 Forfatter: Clker-Free-Vector-Image. Kilde: Pixabay.
Forfatter: Clker-Free-Vector-Image. Kilde: Pixabay. Som katalysator
K3Po4 Det fungerer som en katalysator i forskjellige organiske kjemiske reaksjoner. For eksempel har det blitt brukt som et fast stoff for å oppnå biodiesel fra brukt stekeolje.
Biodiesel er et drivstoff som ligner på diesel, men hentet fra fett eller naturlige oljer som brukes eller ikke.
Kan tjene deg: Coulombimetry: grunnleggende, typer, applikasjonerKaliumfosfat var mer effektiv som en katalysator eller akselerator av nevnte reaksjon enn natriumfosfat3Po4 og Cao kalsiumoksid.
I landbruket
K3Po4 Det har blitt brukt til å behandle hveteplanter og gjøre dem motstandsdyktige mot visse skadedyr.
 Hveteplanter kan behandles med k3Po4 å være motstandsdyktig mot noen typer insekter. Forfatter: Hans Braxmeier. Kilde: Pixabay.
Hveteplanter kan behandles med k3Po4 å være motstandsdyktig mot noen typer insekter. Forfatter: Hans Braxmeier. Kilde: Pixabay. Noen forskere prøvde hveteplanter med kaliumfosfat og viste seg at denne motstanden mot bladlus Duraphis Noxia, Et insekt som angriper disse plantene.
Etter påføring av en utvannet løsning av K3Po4 På frøplantene var det mindre alvorlighetsgrad av symptomene forårsaket av disse insektene og redusert antall bladlus som fôret på disse.
 Forfatter: Hans Braxmeier. Kilde: Pixabay.
Forfatter: Hans Braxmeier. Kilde: Pixabay. I medisinske applikasjoner
Kaliumfosfat har blitt brukt for å modifisere den bedøvelseseffekten av lidokain, en lokalbedøvelse. Et lokalbedøvelse er et medikament som når det brukes i et område av kroppen gir tap av smertefølsomhet i det området.
Det ble funnet at K3Po4 Det gjør det mulig å forlenge lokalbedøvelsen av lidokain.
Som avføringsmiddel
Kaliumfosfat øker flytningen av tarminnholdet fordi det hjelper til med å beholde vann i tarmen, noe som indirekte induserer tarmmuskelkontraksjon.
I veterinærmedisin
K3Po4 Det brukes i dyr med diabetisk ketoacidose (en komplikasjon av diabetes) for å behandle hypofospathia (liten mengde fosfat i blodet).
Imidlertid, når det tilføres i overkant, kan det forårsake hypokalsemi (lite kalsium i blodet), hyperfospati (overflødig fosfat i blodet), ufrivillig sammentrekning av musklene, mineralisering av mykt vev og nyresvikt.
 Hunder med diabetisk acidose kan behandles med kaliumfosfat. Forfatter: David Mark. Kilde: Pixabay.
Hunder med diabetisk acidose kan behandles med kaliumfosfat. Forfatter: David Mark. Kilde: Pixabay. Ved å få DNA
Kaliumfosfat har blitt brukt som en buffer for å rense DNA i genetiske laboratorier.
DNA er et protein som finnes i celler og inneholder all genetisk informasjon som er nødvendig for utvikling og funksjon av levende vesener.
Det kan tjene deg: brøkdestillasjon: prosess, utstyr, applikasjoner, eksemplerVed å isolere DNA går forskere inn i studiet av hvordan arvelige karakterer overføres, så kaliumfosfat er veldig nyttig.
 Tegne DNA -molekyl. Forfatter: Public Domain fartures. Kilde: Pixabay.
Tegne DNA -molekyl. Forfatter: Public Domain fartures. Kilde: Pixabay. I flere applikasjoner
Kaliumfosfat k3Po4 det tjener:
- som et kostholdstilskudd,
- for erstatning for elektrolytt,
- Som buffer, det vil si som et kjemisk system som gjør at OH -ionnivåer kan kontrolleres- eller hydrogen H+ I vandig løsning,
- Å stoppe eller hemme dannelsen av tann karies,
- Som korrosjonsinhibitor og anti -Sniff -middel,
- som et middel til å behandle overflater og beleggsmiddel,
- som frostvæske,
- i rengjøringsprodukter.
 Korroderte rør. K3Po4 gjør det mulig å unngå korrosjon i rørene i noen bransjer eller prosesser. Forfatter: Michael Gaida. Kilde: Pixabay.
Korroderte rør. K3Po4 gjør det mulig å unngå korrosjon i rørene i noen bransjer eller prosesser. Forfatter: Michael Gaida. Kilde: Pixabay. Negativt aspekt for bruk i landbruket
Visse forskere fant det ved å legge til k3Po4 En metanutslipp økes til en rismikrokultur (velg4) til atmosfæren. Metan er en gass som bidrar til drivhuseffekten og økningen i temperaturen på planeten vår.
Referanser
- ELLER.S. National Library of Medicine. (2019). Kaliumfosfat. Gjenopprettet fra Pubchem.NCBI.NLM.NIH.Gov.
- Panciera, d.L. (2012). Væsketerapi ved endokrine og metabolske lidelser. Fosfortilskudd. I væske, elektrolytt og syre-baseforstyrrelser i små dyrepraksis (fjerde utgave). Gjenopprettet fra Scientedirect.com.
- Shenawi-Khalil, s. et al. (2012). Syntese av acetylener via dehydrobromasjon ved bruk av fast vannfritt kaliumfosfat som base under faseoverføringstilstand. Tetrahedron Letters, bind 53, utgave 18, 2012, side 2295-2297. Gjenopprettet fra Scientedirect.com.
- Guan, g. et al. (2009). Tri-passiumfosfat som en solid katalysator for biodieselproduksjon fra avfallskokingsolje. Drivstoffbehandlingsteknologi, bind 90, utgave 4, 2009, side 520-524. Gjenopprettet fra Scientedirect.com.
- Kulkami, m.TIL. (2012). Mekanistisk tilnærming for ekspansjon og løsningsmiddelfri syntese av a-hydroksyfosfonater ved bruk av kaliumfosfat som katalysator. Comperes Rendus Chimie, vol 16, utgave 2, 2013, side 148-152. Gjenopprettet fra Scientedirect.com.
- Venter, e. et al. (2014). Kaliumfhosfat induserer toleranse anti -install den russiske hvete bladlus (Duraphis Noxia, Homoptera: Aphididae) i hvete. Crop Protection Vol 61, juli 2014, side 43-50. Gjenopprettet fra Scientedirect.com.
- Bonturi, n. et al. (2013). Natriumcitrat og kaliumfosfat som alternative adsorpsjonsbuffere i hydrofob og aromatisk tiofil kromatografisk rensing av plasmid -DNA fra nøytralisert lysat. Journal of Chromatography B, bind 919-920, 2013, side 67-74. Gjenopprettet fra Scientedirect.com.
- Conrad, r. og Klose, m. (2005). Effekt av kaliumfosfat befruktning på produksjon og utslipp av metan og dets 1. 3C-stabil isotopsammensetning i rismikrokosmos. Jordbiologi og biokjemi, vol 37, utgave 11, 2005, side 2099-2108. Gjenopprettet fra Scientedirect.com.
- Bly, d.R. (Editor) (2003). CRC Handbook of Chemistry and Physics. 85th CRC Press.
- Røykfot. (2019). Tipotassiumfosfat. Innhentet fra.Wikipedia.org
- « Karakteristikk inndataenheter, hva er bruk, typer, eksempler
- Tumor nekrose faktor (TNF) struktur, virkningsmekanisme, funksjon »

