Hafnium

- 3882
- 326
- Prof. Theodor Gran
 Metallisk hafnio prøve. Kilde: Hi-res Images ofchemical Elements [CC av (https: // creativeCommons.Org/lisenser/av/3.0)]
Metallisk hafnio prøve. Kilde: Hi-res Images ofchemical Elements [CC av (https: // creativeCommons.Org/lisenser/av/3.0)] Hva er Hafnio?
Han Hafnium Det er et overgangsmetall hvis kjemikalie er HF og har et atomnummer på 72. Det er det tredje elementet i gruppe 4 i det periodiske tabellen, og er congene i titanen og circum. Med sistnevnte deler den mange kjemiske egenskaper, og er lokalisert sammen i mineraler av jordskorpen.
Ser du etter Hafnio ser hvor zirkoniumet, fordi det er et biprodukt av dets ekstraksjon. Navnet på dette metall.
Dette metallet tar skillet om å være det siste av de mest stabile elementene som er oppdaget her på jorden; Det vil si at de andre funnene har utgjort en serie med ultrapesados, radioaktive og/eller kunstige isotoper.
HAFNIO -forbindelser er analoge med titan og sirkonium, hovedsakelig +4 oksidasjonsnummer, for eksempel HFCL4, HFO2, HFI4 og HFBR4. Noen av dem leder listen over de mest ildfaste materialene som noen gang er opprettet, så vel som legeringer av stor termisk motstand og fungerer også som utmerkede nøytronabsorbenter.
Av denne grunn har Hafnio mye deltakelse i kjernekjemi, spesielt for trykkvannsreaktorene.
Oppdagelse
Overgangsmetall eller sjeldne jordarter
Oppdagelsen av Hafnio var omgitt av kontroverser, selv om dens eksistens allerede var spådd siden 1869 takket være Mendeleev periodiske tabell.
Problemet var at det var plassert under zirkoniet, men falt sammen i samme periode av elementene i de sjeldne jordene: Lantanoides. Kjemikere på den tiden visste ikke om det var et overgangsmetall eller et metall fra sjeldne jordarter.
 99,9% Hafnium bar. Source-Alchemist-HP (www.PSE-MENDELEJEW.av), CC By-SA 2.0, via Wikimedia Commons
99,9% Hafnium bar. Source-Alchemist-HP (www.PSE-MENDELEJEW.av), CC By-SA 2.0, via Wikimedia Commons Den franske kjemikeren Georges Urbain, Discoverer of Luthacio, nabolandet metall av Hafnio, sa i 1911 at han hadde oppdaget element 72, som Celtio kalte og proklamerte at det var et metall av de sjeldne jordene. Men tre år senere ble det konkludert med at resultatene var feil, og at det bare hadde isolert en blanding av Lantanoides.
Det var ikke før elementene ble bestilt av atomnumrene deres, takket være arbeidet til Henry Moseley i 1914, som nabolaget mellom Luthate og Element 72 var bevis på at den samme gruppen som titan og omkretsmetaller.
Kan tjene deg: flokkulering: reaksjon, typer, applikasjoner, eksemplerDeteksjon i København
I 1921, etter studiene av atomstrukturen til Niels Bohr og dens prediksjon av røntgenutslippsspekteret for element 72, ble dette metallet stoppet i mineralene til de sjeldne jordene; Og i stedet, søket hans på sirkoniummineraler fokuserte, siden begge elementene måtte dele flere kjemiske egenskaper.
Den danske kjemikeren Dirk Coster og ungarsk kjemiker Georg Von Hevesy i 1923 anerkjente endelig det forutsagte spekteret av Niels Bohr i zirkonprøver fra Norge og Grønland. Etter å ha gjort oppdagelsen i København, kalte de element 72 med det latinske navnet på denne byen: Hafnia, som senere avledet 'Hafnio'.
Isolasjon og produksjon
Imidlertid var det ikke en lett oppgave. Selv om en metode i 1924 ble utviklet ved fraksjonell rekrystallisering for å oppnå HAFNIO -tetraklorid, HFCL4, Det var de nederlandske kjemikaliene Anton Eduard Van Arkel og Jan Hendrik de Boer som reduserte ham til det metalliske Hafnium.
For å gjøre dette, HFCL4 Det gjennomgikk en reduksjon ved bruk av metallisk magnesium (Kroll -prosess):
HFCL4 + 2 mg (1100 ° C) → 2 mgcl2 + Hf
På den annen side, fra Hafnio Tetrayoduro, HFI4, Dette ble fordampet for å få en termisk nedbrytning på et glødende wolframfilament, hvor det metalliske hafnium ble avsatt for å forårsake en polykrystallinsk utseendestang (krystallinsk stangprosess eller Arkel-BERER-prosess):
HFI4 (1700 ° C) → HF + 2 I2
Hafnio struktur
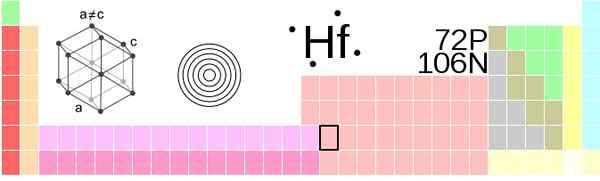 HAFNIO -plasseringen i det periodiske bordet. Fontene: !Original: AhoteseierVector: Sushant Savla, CC BY-SA 3.0, via Wikimedia Commons
HAFNIO -plasseringen i det periodiske bordet. Fontene: !Original: AhoteseierVector: Sushant Savla, CC BY-SA 3.0, via Wikimedia Commons Hafnio, HF -atomer, er gruppert i omgivelsestrykk på en kompakt sekskantet struktur krystall, HCP, akkurat som titan og zirkoniummetaller gjør. Denne Hafnio HCP -krystallen blir dens α -fase, som forblir konstant opp til en temperatur på 2030 K, når den lider en overgang til β -fasen, med en kubikkstruktur sentrert i kroppen, BCC.
Dette forstås hvis varmen "slapper av" glasset blir vurdert, og derfor søker HF -atomer å plassere seg på en slik måte at komprimeringen deres avtar. Disse to fasene er nok til å vurdere polymorfismen i hafnium.
Den presenterer også en polymorfisme som avhenger av høyt trykk. Α- og β -fasene eksisterer ved et trykk på 1 atm; Mens ω, sekskantet, men enda mer komprimert fase enn den vanlige HCP, vises når trykket overstiger 40 GPA. Interessant nok, når presset fortsetter å øke, dukker β -fasen opp igjen, den minst tette.
Kan tjene deg: seleenhydronsyre (H2SE): Hva er, struktur, egenskaper, brukHafnio egenskaper
Fysisk utseende
Sølvhvit faststoff, som viser mørke toner hvis det har et lag med oksid og nitrid.
Molmasse
178,49 g/mol
Smeltepunkt
2233 ºC
Kokepunkt
4603 ºC
Tetthet
Ved romtemperatur: 13,31 g/cm3, å være to ganger tettere enn circum
Rett ved smeltepunktet: 12 g/cm3
Fusjonsvarme
27,2 kJ/mol
Fordampningsvarme
648 kJ/mol
Elektronegativitet
1.3 på Pauling -skalaen
Ioniseringsenergier
Først: 658,5 kJ/mol (HF+ gassform)
For det andre: 1440 kJ/mol (HF2+ gassform)
Tredje: 2250 kJ/mol (HF3+ gassform)
Termisk ledningsevne
23,0 w/(m · k)
Elektrisk resistivitet
331 nΩ · m
Mohs hardhet
5.5
Reaktivitet
Med mindre metallet er Pula og forbrenner, skyter gnister ved en temperatur på 2000 ºC, har det ingen mottakelighet for å oksidere eller løpe, siden et tynt lag med oksyd beskytter det. I denne forstand er det en av de mest stabile metaller. Syrer eller sterke baser kan faktisk oppløse det; Med unntak av fluorhorinsyre og halogener som er i stand til å oksidere den.
Elektronisk konfigurasjon
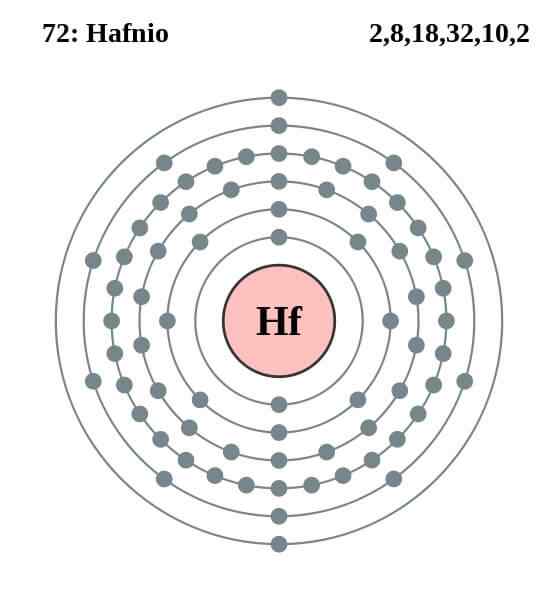 HAFNIO elektronisk konfigurasjon
HAFNIO elektronisk konfigurasjon Hafnios atom har følgende elektroniske konfigurasjon:
[Xe] 4f14 5 d2 6s2
Dette sammenfaller med at tilhørende gruppe 4 i det periodiske bordet, sammen med titan og sirkonium, fordi det har fire Valencia -elektroner i 5D og 6S orbitals. Legg merke til at Hafnio ikke kunne være et lantanoid, siden den har sine helt fulle 4F -orbitaler.
Oksidasjonstall
Den samme elektroniske konfigurasjonen avslører hvor mange elektroner som er i stand til å miste et Hafnio -atom når du er en del av en forbindelse. Forutsatt at han mister sine fire elektroner i Valencia, ville han være en tetravalent kation HF4+ (I analogi med deg4+ og Zr4+), Og vil derfor ha et oksidasjonsnummer på +4.
Dette er faktisk det mest stabile og vanlige av oksidasjonstallene. Andre mindre relevante er: -2 (HF2-), +1 (HF+), +2 (HF2+) og +3 (HF3+).
Isotoper
Hafnio presenteres på jorden som fem stabile isotoper og en radioaktiv med en veldig stor tid i livet:
-174HF (0,16%, med en halvliv på 2 · 10femten år, så det anses som praktisk talt stabilt)
-176HF (5,26%)
-177HF (18,60%)
Kan tjene deg: svake baser-178HF (27,28%)
-179HF (13,62%)
-180HF (35,08%)
Legg merke til at det ikke er noen slik isotop som sådan som skiller seg ut i overflod, og dette gjenspeiles i den gjennomsnittlige atommassen til Hafnio, 178.49 Uma.
Av alle radioaktive isotoper av Hafnio, som sammen med de innfødte totalt totalt 34, 178M2HF er den mest kontroversielle fordi i sitt radioaktive forfall frigjør gammastråling, slik at disse atomene kan brukes som krigsgrum.
Bruk/applikasjoner
 Hafnio dekket med et tynt lag oksid. Kilde: Alchemist-HP (snakk) (www.PSE-MENDELEJEW.De), Fal, via Wikimedia Commons
Hafnio dekket med et tynt lag oksid. Kilde: Alchemist-HP (snakk) (www.PSE-MENDELEJEW.De), Fal, via Wikimedia Commons Atomreaksjoner
Hafnio er et fuktighetsresistent metall og høye temperaturer, i tillegg til å være et utmerket nøytronabsorberende. Av denne grunn brukes det i trykkvannsreaktorer, så vel som i fremstilling av kontrollerende barer for kjernefysiske reaktorer, i hvis belegg de er laget av Ultrapuro Circu.
Legeringer
Hafnio -atomer kan integrere andre metallkrystaller for å gi opphav til forskjellige legeringer. Disse er preget av å være iherdige og termisk resistente, så de er bestemt for romlige anvendelser, som i konstruksjonen av motoriske dyser for raketter.
På den annen side har noen legeringer og faste forbindelser av Hafnio spesielle egenskaper; som henholdsvis karbider og nituros, HFC og HFN, som er veldig ildfaste materialer. Tantalo og Hafnio Carbide, TA4HFC5, Med et fusjonspunkt på 4215 ºC er det et av de mest ildfaste materialene som noen gang er kjent.
Katalyse
Hafnios metalocenes brukes som organiske katalysatorer for polymelensyntese som polyetylen og polystyren.
Risiko
Det er hittil ukjent hvilken innvirkning HF -ionene kan ha i kroppen vår4+. På den annen side, fordi de finnes i naturen i zirkoniummineraler, antas det ikke at de får endre økosystemet for å frigjøre saltene sine til miljøet.
Nå anbefales det å manipulere Hafnio -forbindelser nøye, som om de var giftige, selv om det ikke er noen medisinske studier som beviser at de er helseskadelige.
Den virkelige faren for hafnio ligger i partiklene i dets fine bakke faststoff, som kan brenne akkurat når de kommer i kontakt med oksygenet i luften.
Dette forklarer hvorfor når den er polert, handling som skraper overflaten og gir fra seg rene metallpartikler, frigjør gnister med en temperatur på 2000 ºC; Det vil si at Hafnio presenterer pyroporisitet, den eneste eiendommen som innebærer brann eller alvorlig forbrenningsrisiko.

