Hydrofil bruk av begrepet, egenskaper, eksempler

- 1587
- 474
- Markus Fredriksen
EN hydrofyl eller hydrofil Det er et molekylært segment eller en forbindelse som er preget av å ha en sterk affinitet for vann og polare løsningsmidler. Etymologisk betyr det 'vannelskere', noe som innebærer at en hydrofil vil kunne oppløse eller samhandle effektivt med vannmolekyler.
Derfor har hydrofile stoffer en tendens til å være oppløselige eller blandbare med vann. Imidlertid hydrofilisitet, det vil si dens affinitet for vann og annet polært løsningsmiddel.
 Glass er et hydrofilt materiale fordi det blir vått lett og dråpene som blir avsatt på det blir flatet ut eller glir ned. Kilde: Pexels.
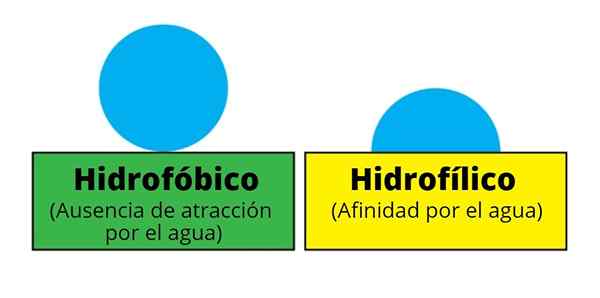
Glass er et hydrofilt materiale fordi det blir vått lett og dråpene som blir avsatt på det blir flatet ut eller glir ned. Kilde: Pexels. Dermed er hydrofile overflater lettere å våte eller fuktige enn hydrofobe, de som hater vann eller frastøter det. Det første flatere vannet synker i rader, mens sistnevnte snur dem rundt og fremtredende. Visualiseringen av disse dråpene er en av hovedfaktorene for å skille et hydrofilt materiale fra et hydrofobisk.
Konseptet med hydrofilisitet er essensielt for forståelsen av overflatekjemi, løsninger, grensesnitt og den amfifylliske karakteren til stoffer som proteiner og fettsyrer.
[TOC]
Bruk av det hydrofile eller hydrofile begrepet
De 'hydrofile' og 'hydrofile' begrepene er betegnet både molekyler og strukturelle deler av det samme. Imidlertid brukes 'hydrofil' hovedsakelig for å referere til ethvert molekyl eller forbindelse som har mye affinitet for vann.
Derfor er det et hydrofilt eller hydrofilt molekyl, hvis dens affinitet til vann er veldig høy i henhold til visse hensyn. For eksempel er sukrose en hydrofil forbindelse, som er den samme som å si at det er en hydrofil, siden krystaller lett oppløses i ethvert volum av vann.
Kan tjene deg: TritioDet aktuelle molekylet kan presentere hydrofile segmenter eller deler, som kan være konstituert av et kullsyreholdig skjelett, eller ganske enkelt av en polar gruppe. Når det gjelder en gruppe, sier vi vanligvis at det er en hydrofil gruppe, som bidrar til hydrofilisiteten til molekylet eller overflaten det tilhører.
Vanligvis brukes 'hydrofil' oftere enn 'hydrofil', siden sistnevnte vanligvis forbeholder seg mer enn noe annet for molekyler eller forbindelser som er helt hydrofile; det vil si at de ikke har hydrofobe regioner i sine molekylære strukturer. Dette gjelder spesielt når makromolekyler eller polymere faste stoffer er beskrevet.
Kjennetegn på hydrofile stoffer
Kovalens
Hydrofile stoffer er kovalente forbindelser, noe som betyr at enhetene deres består av molekyler og ikke av ioniske nettverk. Selv om salter har en tendens til å være veldig løselig i vann, enda mer enn mange hydrofile.
På den annen side er ikke alle salter oppløselige i vann, for eksempel sølvklorid, AGCL, og det er derfor de ikke kan klassifiseres som hydrofil.
Polaritet
For at et molekyl skal være hydrofilt, må det ha en viss polaritet. Dette er bare mulig hvis polargrupper som -oh, -sh, -nh har i sin struktur2, -COOH, etc., slik at de bidrar til sitt permanente dipolmoment og derfor til deres hydrofilisitet.
Interaksjoner
Hydrofiler gjenkjennes over andre forbindelser på grunn av deres evne til å danne hydrogenbroer med vannmolekyler. Merk at polargruppene nevnt ovenfor har muligheten til å donere hydrogener eller akseptere dem for å danne slike broer, som er en spesiell type dipol-dipolo-interaksjoner.
Solide stater
Hydrofiler kan være gassformige, flytende eller faste stoffer, den vanligste er disse to siste.
Kan tjene deg: DifferensialelektronHydrofile væsker er blandbar med vann, så når det er blandet, vil ikke to faser bli sett.
I mellomtiden oppløses hydrofile faste stoffer i vann eller absorberer det veldig enkelt; Men i tillegg har noen evnen til å bli våte eller bli våte uten å løse opp i det hele tatt, siden selv om overflaten er hydrofil, er det ikke helt dens indre masse. Dette er tilfellet med mange polymermaterialer, for eksempel kjemisk modifiserte silikoner.
Hydrofile overflater
Hydrofile overflater er utsatt for overflatekjemi -studier. De er ikke oppløselige i vann, men de kan fukte og flate ut dråpene av vann som blir avsatt på det. Dette er fordi de har eksterne hydrofile grupper som samhandler effektivt med vannmolekyler.
Dråpen av vann dannes med den hydrofile overflaten en kontaktvinkel mindre enn 90 º, som er lik for å si at den vil presentere en flatet, liten sfærisk eller rund form.
Slik er det slik at den slipper ende og utvides og går som væsketrekker. For eksempel brukes denne egenskapen for å forhindre at tåke som setter overflaten, siden den knapt berøres av vannet kondenserer og glir ned.
Huden vår er hydrofil, siden dråpene på den har en tendens til å flate og gli; Bortsett fra når det er porestyrer med olje eller en krem. Da vil vanndråpene være rundt og definert, fordi overflaten har blitt midlertidig hydrofob.
Eksempler på hydrofile stoffer
Ammoniakk
Ammoniakk, NH3, Det er hydrofilt fordi molekylet kan danne flere hydrogenbroer med vann. Dette gjør både i en gass og flytende tilstand veldig løselig i vannet.
Oksalsyre
Oksalsyre, h2C2ENTEN4, Det er en hydrofil.
Kan tjene deg: Petri Box: Karakteristikk, funksjoner, bruk eksemplerMetanol
Metanolen, CH3Å, det er en hydrofil takk til gruppen Oh.
Alkoholer
Alkohol er vanligvis hydrofile stoffer, så lenge karbonskjelettet ikke er veldig stort. For eksempel er 1-propanol og 2-propanol blandbar med vann, men dette skjer ikke med 1-butanol, hvis blandbarhet blir lavere på grunn av karbonkjeden med større lengde.
Stivelse
Stivelse er et eksempel på en hydrofil polymer, siden glukoseenhetene har flere OH -grupper som hydrogenbroer dannes med vannmolekyler.
Tre
Treverket er hydrofilt, og selv om det ikke oppløses i vannet, fuktes det raskt hvis det ikke blir behandlet med hydrofobe belegg.
Proteiner
Proteiner har polare grupper veldig relatert til vann. Derfor er interaksjonene med vannmolekyler effektive. Dette innebærer imidlertid ikke at alle proteiner er oppløselige i vann, siden deres strukturer (tertiær og kvartær) spiller en grunnleggende rolle i nevnte oppløsningsprosess.
Glass
Glass er et hydrofylmateriale fordi det ikke består av molekyler, men SIO -nettverk2 tre -dimensjonale, oksygenatomer kan akseptere vannhydrogenbroer. Dette er grunnen til at glassfartøy svetter i fuktige miljøer.
Referanser
- Graham Solomons t.W., Craig f. Yngel. (2011). Organisk kjemi. (10th Utgave.). Wiley Plus.
- Carey f. (2008). Organisk kjemi. (Sjette utgave). Mc Graw Hill.
- Morrison og Boyd. (1987). Organisk kjemi. (Femte utgave). Addison-Wesley Iberoamericana.
- Wikipedia. (2020). Hydrofil. Hentet fra: i.Wikipedia.org
- David L. Chandler. (16. juli 2013). Forklart: hydrofob og hydrofil. Gjenopprettet fra: Nyheter.mit.Edu
- Gelest. (2020). Hydrofile materialer. Gjenopprettet fra: gelest.com
- Ahmad Darem et al. (5. september 2018). Hydrofile og hydrofobe materialer og applikasjoner. Taylor & Francis online. gjør jeg.org/10.1080/15567036.2018.1511642
- « Chaco -krigsbakgrunn, årsaker, utvikling, konsekvenser
- Levende belastning konsept, egenskaper, eksempler »

