Kalsiumoksalat (CAC2O4) egenskaper, struktur, bruk, risiko
- 2734
- 5
- Jonathan Moe
Han Kalsiumoksalat Det er en organisk forbindelse dannet av karbon (C), oksygen (O) og kalsium (CA) elementer (CA) (CA). Den kjemiske formelen er CAC2ENTEN4. Det finnes vanligvis i sine tre hydratiserte former: mono-, di- og trihydrat. Dette er henholdsvis med en, to eller tre vannmolekyler i sin krystallinske struktur.
Kalsiumoksalat finnes i mineraler, planter, sopp og andre levende vesener som pattedyr og til og med i mennesker som et resultat av metabolismen til noen proteiner. Det kan finnes i urinen til mennesker og noen dyr.
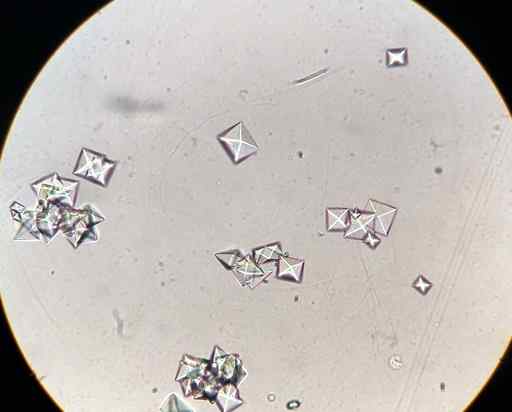 CAC kalsiumoksalatkrystaller2ENTEN4 I en urinprøve observert med et mikroskop. J3D3/CC BY-SA (https: // CreativeCommons.Org/lisenser/by-SA/4.0). Kilde: Wikimedia Commons.
CAC kalsiumoksalatkrystaller2ENTEN4 I en urinprøve observert med et mikroskop. J3D3/CC BY-SA (https: // CreativeCommons.Org/lisenser/by-SA/4.0). Kilde: Wikimedia Commons. Noen matvarer som spinat, ruibarbos, soya.
Du kan unngå utseendet til CAC -steiner2ENTEN4 I nyrene hvis mange væsker blir inntatt, spesielt vann, unngår mat med høyt oksalatinnhold og bruker de rike på kalsium og magnesium.
Kalsiumoksalat danner uønskede inlays i rør og prosesstanker som masse- og papirproduksjon, og også i ølfabrikker.
[TOC]
Struktur
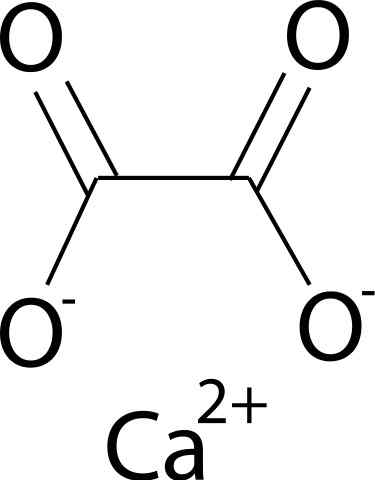
Kalsiumoksalat dannes ved kalsiumka ion2+ og oksalationet C2ENTEN42-. Oksalatanion består av to karbonatomer og fire oksygenatomer. De negative belastningene med oksalatanion finnes i oksygenatomer.
 Kjemisk struktur av kalsiumoksalat. Vsimonian/CC By-SA (https: // CreativeCommons.Org/lisenser/by-SA/2.5). Kilde: Wikimedia Commons.
Kjemisk struktur av kalsiumoksalat. Vsimonian/CC By-SA (https: // CreativeCommons.Org/lisenser/by-SA/2.5). Kilde: Wikimedia Commons. Nomenklatur
- Kalsiumoksalat
- Oksalsyre kalsiumsalt
- Etanodiosyre kalsiumsalt
Egenskaper
Fysisk tilstand
Fargeløs krystallinsk, hvit, gul eller brun som kan være i tre forskjellige hydratiserte former.
Molekylær vekt
128,1 g/mol
Smeltepunkt
Kalsiumoksalatmonohydrat dekomponerer til 200 ° C.
Spesifikk vekt
CAC monohydrat2ENTEN4 •H2O = 2,22 g/cm3
CAC dihydrat2ENTEN4 •2H2O = 1,94 g/cm3
CAC trihydrat2ENTEN4 •3H2O = 1,87 g/cm3
Løselighet
Nesten uoppløselig i vann: 0,00061 g/100 g vann ved 20 ° C. Monohydrat oppløses i fortynnet syre.
Ph
Vandige kalsiumoksalatløsninger er svakt grunnleggende.
Kjemiske egenskaper
Kalsiumoksalat er kalsiumsaltet av oksalsyre. Dette er et naturlig sekundært produkt av metabolisme, så det er veldig rik i menneskekroppen, og er en del av mange matvarer.
Oksalsyre og dens konjugerte base, oksalat, er veldig oksiderte organiske forbindelser, med en kraftig chelateringsaktivitet, det vil si at de lett kan kombineres med positive ioner med +2 eller +3 belastninger.
Kan tjene deg: metyl- eller metilogruppeDens vandige oppløsninger er svakt grunnleggende fordi oksalationet har en tendens til å ta protoner h+ vann, som frigjør OH -ioner-. Etter å ha tatt to protoner h+ Oksalationet blir oksalsyre H2C2ENTEN4:
C2ENTEN42- + H2O → HC2ENTEN4- + Åh-
HC2ENTEN4- + H2O → h2C2ENTEN4 + Åh-
Tilstedeværelse i naturen
I mineraler
Kalsiumoksalat er det vanligste oksalatet og presenteres i form av mineraler kalt Whewellita, Weddellita og Caoxite.
Whewellita er CAC -monohydrat2ENTEN4 •H2Eller og er den mest stabile av formene for denne forbindelsen.
 Whewellita Mineral Rock. Rob Lavinsky, Irocks.COM-CC-BY-SA-3.0/CC By-SA (https: // CreativeCommons.Org/lisenser/by-SA/3.0). Kilde: Wikimedia Commons.
Whewellita Mineral Rock. Rob Lavinsky, Irocks.COM-CC-BY-SA-3.0/CC By-SA (https: // CreativeCommons.Org/lisenser/by-SA/3.0). Kilde: Wikimedia Commons. Weddellita er CAC -dihydratet2ENTEN4 •2H2O og er mindre stabil enn monohydrat.
 Weddelite mineralkrystaller. Leon Hupperichs/CC av (https: // creativecommons.Org/lisenser/av/3.0). Kilde: Wikimedia Commons.
Weddelite mineralkrystaller. Leon Hupperichs/CC av (https: // creativecommons.Org/lisenser/av/3.0). Kilde: Wikimedia Commons. Caxita er kalsiumoksalat trihydrado cac2ENTEN4 •3H2ENTEN.
I planter og sopp
Kalsiumoksalat er assosiert med tørr jord og blader, også med patogener, frie, symbiose eller planter assosiert med planter. I sistnevnte dannes krystaller ved utfelling av kalsium i form av dets oksalat.
CAC -formasjon2ENTEN4 For sopp har det en viktig innflytelse på de biologiske og geokjemiske jordprosessene, ettersom det utgjør et kalsiumreserve for økosystemet.
Tilstedeværelse i menneskekroppen og i pattedyr
Oksalat har sin opprinnelse i leveren, i de røde eller erytrocyttblodcellene og i mindre mengde i nyren. Det er dannet av metabolismen av aminosyrer (som fenylalanin og tryptofan) og ved oksidasjon av glioxal dialdehyd,.
C -vitamin kan også bli oksalat når du utfører sin antioksidantfunksjon.
Kalsiumoksalat finnes i steinene som er dannet i nyrene til mennesker eller dyr med nyresykdom.
De så -kallede kalsiumoksalatberegningene eller steinene dannes ved krystallisering eller aggregering av CAC2ENTEN4 I generell urin med kalsium og oksalat. Dette betyr at urin inneholder både kalsium og oksalat at det ikke er mulig at nevnte forbindelse forblir oppløst, men utfeller eller passerer til fast tilstand i form av krystaller.
Hos mennesker
Dannelsen av sand eller steiner i nyrene er en sykdom som kalles nefrolithiasis; Den angriper omtrent 10% av befolkningen og omtrent 75% av disse steinene er sammensatt av kalsiumoksalat -CAC2ENTEN4.
 Kalsiumoksalat kan danne steiner i nyrene. Forfatter: vsrao. Kilde: Pixabay.
Kalsiumoksalat kan danne steiner i nyrene. Forfatter: vsrao. Kilde: Pixabay. Dannelsen og veksten av kalsiumoksalatkrystaller i nyren oppstår fordi urinen hos noen mennesker er overmettet med nevnte salt. Kalsiumoksalat utvikler seg i syre urin i pH mindre enn 6,0.
Kan tjene deg: IsóbarosSupeurasjon oppstår når utskillelsen eller eliminering av dette saltet (som er veldig lite oppløselig i vann) gjennom urinen oppstår i et lite vannvolum.
Faktorer som påvirker utseendet til nyrestein
Blant faktorene som favoriserer dannelse av kalsiumoksalat sand er overflødig kalsium i urin eller hyperkalciuria, overflødig oksalat i urin eller hyperoxaluria, elementer avledet fra fôring og fravær av hemmere.
Overskytende oksalat kan oppstå når høye mengder spinat, grov, soya, nøtter og sjokolade blir inntatt, blant annet mat.
 Sjokolade kan være en kilde til kalsiumoksalat og favorisere utseendet til steiner i nyrene. Forfatter: Alexander Stein. Kilde: Pixabay.
Sjokolade kan være en kilde til kalsiumoksalat og favorisere utseendet til steiner i nyrene. Forfatter: Alexander Stein. Kilde: Pixabay. Imidlertid er det stoffer som hemmer eller forhindrer dannelse av steiner. Blant forbindelsene som unngår beregninger er små molekyler som sitrat og pyrofosfat, og store molekyler som glykoproteiner og proteoglykaner.
Måter å unngå dannelse av kalsiumoksalatsteiner
En god strategi for å forhindre tilbakefall av sand eller kalsiumoksalatberegninger inkludert økningen i inntak av væske, økning i kalsiumrike matvarer (for eksempel meieriprodukter) og begrense bordsalt (NaCl), animalsk protein, animalsk protein og rike måltider i oksalat.
Hos dyr
Siden begynnelsen av år 2000. Det ser ut til at dette avhenger av hvilken type mat som disse dyrene inntar og har å gjøre med surheten i urin og magnesiummangel (MG).
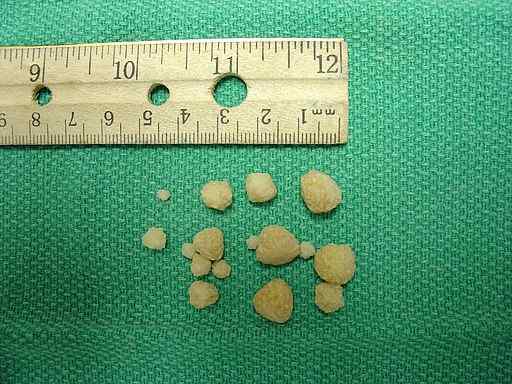 Kalsiumoksalatsteiner funnet i urinblæren til en hund. Joel Mills/CC By-SA (http: // CreativeCommons.Org/lisenser/by-SA/3.0/). Kilde: Wikimedia Commons.
Kalsiumoksalatsteiner funnet i urinblæren til en hund. Joel Mills/CC By-SA (http: // CreativeCommons.Org/lisenser/by-SA/3.0/). Kilde: Wikimedia Commons. Kroppsrespons på overflødig oksalat
Det er bevis på at både mennesker og dyr reagerer på overflødig oksalat ved å øke antallet bakterier som kan nedbryte oksalat.
Noen av disse bakteriene er Oxalobacter formigenes, Bifidobacterium sp., Porphyromonas gingivalis og Bacillus sp., blant andre, og er til stede naturlig i tarmen.
applikasjoner
I følge kilder som er konsultert, brukes kalsiumoksalat i keramisk belegg.
Det har blitt brukt til å dekke skulpturer og andre kunstneriske elementer av kalkstein, og det har blitt funnet at det forbedrer hardheten i materialet, reduserer porøsiteten og øker dens motstand mot syrer og alkalier.
 I Italia har det vært opplevd å dekke objekter kalkstein av museer med kalsiumoksalat for å bevare dem. Forfatter: Kilde: Moni Quayle. Pixabay.
I Italia har det vært opplevd å dekke objekter kalkstein av museer med kalsiumoksalat for å bevare dem. Forfatter: Kilde: Moni Quayle. Pixabay. Problemer i noen prosesser
I masse- og papirindustrien kan kalsiumoksalat danne inlays som forårsaker mange problemer i prosessen.
For å unngå dannelsen i industrielle prosesskanaler eller rør.
Det kan tjene deg: koboltklorid (COCL2 (: Struktur, nomenklatur, egenskaperDet har også en tendens til å samle seg som stein i beholderne der øl produseres, hvor det må elimineres for å unngå dannelse av mikroorganismer som kan gi en ubehagelig smak til å drikke.
Risiko
I høye konsentrasjoner kan oksalat forårsake død hos dyr og noen ganger hos mennesker hovedsakelig på grunn av dens korrosive effekter.
Akkumulering av oksalat og dens konjugerte syre, oksalsyre, kan forårsake lidelser som funksjonsfeil i hjertet, kalsiumoksalatsteiner, nyresvikt og til og med død av toksisitet.
Referanser
- Glasauer, s.M. et al. (2013). Metaller og metalloider, transformasjon av mikroorganismer. Oksalater. I referansemodulasjon i jordsystemer og miljøvitenskap. Gjenopprettet fra Scientedirect.com.
- Baumann, J. M. og Casella, r. (2019). Forebygging av kalsium nefrolithiasis: påvirkning av diurese på kalsiumoksalatkrystallisering i urin. Adv Previum, 2019; 2019: 3234867. NCBI kom seg.NLM.NIH.Gov.
- Breshears, m.TIL. og konferere, til.W. (2017). Urinsystemet. Kalsiumoksalatberegning. På patologisk grunnlag av veterinærsykdom (sjette utgave). Gjenopprettet fra Scientedirect.com.
- Huang, og. er al. (2019). TGE -håndtering av oksalat i TGE -kropp og TGE opprinnelse av oksalat i kalsiumoksalatstoner. Urol Int, 2019 5. desember: 1-10. NCBI kom seg.NLM.NIH.Gov.
- Nilvebrant, n.-ENTEN. et al. (2002). Bioteknologi i masse- og papirindustrien. Pågår i bioteknologi. Gjenopprettet fra Scientedirect.com.
- Pahira, J.J. Og Pevzner, m. (2007). Nefrolithiasis. Kalsiumsteiner. I Penn Clinical Manual of Urology. Gjenopprettet fra Scientedirect.com.
- Worcester, e. M. (1994). Urin kalsiumoksalatkrystallveksthemmere. J Am Soc Nephrol 1994 nov; 5 (5 Suppl 1): S46-53). Gjenopprettet fra Jasn.Asnjournals.org.
- Finkielstein, v.TIL. og gullfarb, d.S. (2006). Strategier for å forhindre kalsiumoksalatsteiner. NCBI kom seg.NLM.NIH.Gov.
- ELLER.S. National Library of Medicine. (2019). Kalsiumoksalat. Gjenopprettet fra Pubchem.NCBI.NLM.NIH.Gov.
- Peck, a.B. et al. (2015). Oksalat-nedbryting av mikroorganismer eller oksalat-nedbrytende enzymer: Wich er den fremtidige terapien for enzymatisk oppløsning av kalsiumokalat urolitter ved tilbakevendende steinsykdom? Urolithiasis, 2016 februar; 44 (1): 27-32. NCBI kom seg.NLM.NIH.Gov.
- Holames, r.P. et al. (2016). Senke urinoksalatutskillelse for å dekret kalsiumoksalat stein diepar. Urolithiasis. 2016 februar; 44 (1); 27-32. NCBI kom seg.NLM.NIH.Gov.
- Cyzar, t.M. (1998). Kalsiumoksalat: en overflatebehandling for kalkstein. Journal of Conservation and Museum Studies 4, PP.6-10. Hentet fra JCMS-Journal.com.
- Wikimedia (2019). Kalsiumoksalat. Innhentet fra.Wikipedia.org.
- « Kvalitative forskningsegenskaper, typer, teknikker, eksempler
- Funksjonalisme (psykologi) opprinnelse, egenskaper og representanter »

