Organiske salter
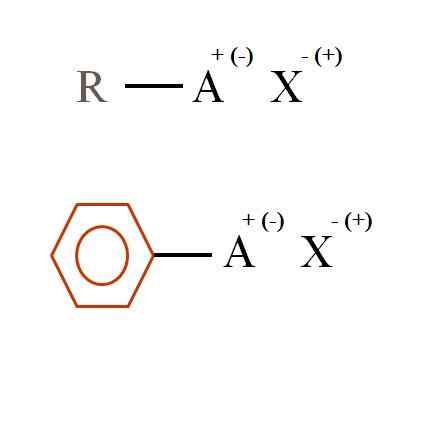
- 1239
- 271
- Thomas Karlsen
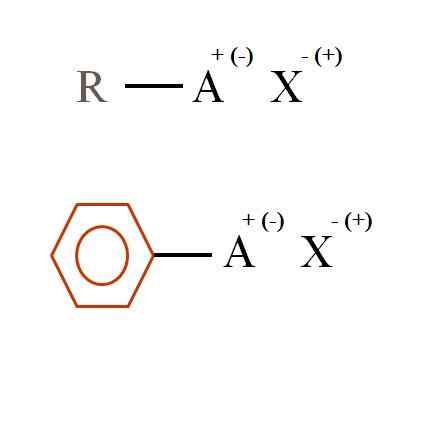 To generelle kjemiske formler for organiske salter. Kilde: Gabriel Bolívar
To generelle kjemiske formler for organiske salter. Kilde: Gabriel Bolívar Hva er organiske salter?
De Organiske salter De er et tett antall ioniske forbindelser med utallige funksjoner. Tidligere avledet fra en organisk forbindelse, som har gjennomgått en transformasjon som gjør at den kan være en last, og at dens kjemiske identitet avhenger av det tilhørende ionet.
I det overlegne bildet vises to veldig generelle kjemiske formler for organiske salter. Den første, R-AX, tolkes som en forbindelse i hvis karbonstruktur et atom, eller gruppe A, bærer en positiv + eller negativ belastning (-).
Som det kan sees, er det en kovalent binding mellom R og A, R-A, men på sin side har den en formell belastning som tiltrekker seg (eller frastøter) til ionen x. Lastskiltet vil avhenge av arten av a og det kjemiske miljøet.
Hvis det var positivt, hvor mange X kunne samhandle? Med en, gitt prinsippet om elektroneutralitet (+1-1 = 0). Hva er imidlertid identiteten til x? Anion X kan være CO32-, krever to kationer RA+; Et halogenid: f-, Cl-, Br-, etc.; eller til og med en annen forbindelse-. Alternativene er uberegnelige.
På samme måte kan et organisk salt være aromatisk, illustrert i den benzenbrune ringen. Kobberbenzoatsalt (II), (C6H5Coo)2Cu består for eksempel av to aromatiske ringer med negativt lastede karboksy -grupper, som samhandler med kation Cu2+.
Fysiske og kjemiske egenskaper ved organiske salter
Fra bildet kan det bekreftes at organiske salter består av tre komponenter: den organiske, r eller AR (den aromatiske ringen), en atom eller gruppebærer av den ioniske belastningen a, og en motion x.
Akkurat som kjemisk identitet og struktur er definert av slike komponenter, på samme måte som egenskapene deres er avhengige av dem.
Fra dette faktum kan visse generelle egenskaper som oppfyller de aller fleste av disse saltene oppsummeres.
Kan tjene deg: Oksidasjonsnummer: Konsept, hvordan få det ut og eksemplerHøye molekylære masser
Forutsatt at mono eller allsidige uorganiske anioner, har organiske salter vanligvis mye større molekylære masser enn uorganiske salter. Dette skyldes hovedsakelig kullsyreholdig skjelett, hvis enkle C-C-bindinger, og dets hydrogenatomer, gir mye masse til forbindelsen.
Derfor er de de ansvarlige for deres høye molekylære masser.
Amfifyliske og overflateaktive midler
Organiske salter er amfifile forbindelser, det vil si at strukturene deres har både hydrofile og hydrofobe ytterpunkter.
Hva er slike ytterpunkter? R eller AR representerer den hydrofobe enden, fordi atomene deres av C og H ikke har stor affinitet for vannmolekyler.
TIL+(-), Atom- eller lastebærergruppen er den hydrofile enden, siden det bidrar til dipolmomentet og samhandler med vanndannende dipol (RA+ Åh2).
Når hydrofile og hydrofobe regioner polariseres, blir amfifilt salt et overflateaktivt middel, et stoff som er mye brukt for utdyping av vaskemidler og Unullamping.
Høye kokepunkter eller fusjon
I likhet med uorganiske salter har organiske salter også høye smelte- og kokepunkter, på grunn av de elektrostatiske kreftene som styrer i flytende eller fast fase.
Å ha en organisk komponent R eller AR, andre typer van der Waals (London, Dipolo-Dipolo, Hydrogen Bridges) deltar på noen måte med elektrostatisk.
Av denne grunn er de faste eller flytende strukturer av organiske salter i første omgang mer komplekse og varierte. Noen av dem kan til og med oppføre seg som flytende krystaller.
Surhet og grunnleggende
Organiske salter er vanligvis sterkere syrer eller baser enn uorganiske salter. Dette er fordi for eksempel i aminsalter har en positiv belastning på grunn av koblingen med et ekstra hydrogen: a+-H. Så, i kontakt med en base, doner protonet til å være en nøytral forbindelse igjen:
Det kan tjene deg: Strontium: Historie, struktur, egenskaper, reaksjoner og brukRa+H + b => ra + hb
H tilhører en, men er skrevet, siden den griper inn i nøytraliseringsreaksjonen.
På den annen side, ra+ Det kan være et stort molekyl, ikke i stand til å danne faste stoffer med et krystallinsk nettverksstall med hydroksylanion eller okshydrilo oh-.
Når dette er slik, salt ram+Åh- Det oppfører seg som en sterk base; Selv så grunnleggende som Naoh eller Koh:
Ra+Åh- + Hcl => racl + h2ENTEN
Legg merke til i den kjemiske ligningen at anion CL- Erstatt åh-, danner salt Ra+Cl-.
Bruk av organiske salter
Bruken av organiske salter vil variere i henhold til identiteten til R, AR, A og X. Dessuten avhenger applikasjonen de blir tildelt også av hvilken type fast eller væske de dannes. Noen generaliteter i denne forbindelse er:
- De tjener som reagenser for syntese av andre organiske forbindelser. Rax kan fungere som en "giver" av R -kjeden for å legge til en annen forbindelse som erstatter en god utgående gruppe.
- De er overflateaktive midler, slik at de også kan brukes som smøremidler. Metallkarboksylalatsalter brukes til dette formålet.
- De tillater å syntetisere et bredt spekter av fargestoffer.
Eksempler på organiske salter
Karboksylater
Karboksylsyrer reagerer med et hydroksyd i en nøytraliseringsreaksjon, noe som forårsaker karboksylalatsalter: RCOO- M+; hvor m+ Det kan være hvilken som helst metallisk kation (Na+, Pb2+, K+, etc.) eller ammonium NH -kation4+.
Fettsyrer er lang -sjain karboksylsyrer, de kan være mettede og umettet. Palmitinsyre er blant mettet (velg3(Ch2)14COOH). Dette stammer fra palmitatsaltet, mens stearinsyren (Cho3(Ch2)16COOH danner Stear Salt. Såper utgjøres av disse saltene.
Kan tjene deg: Generell gasslovNår det gjelder benzosyre, C6H5COOH (hvor c6H5- Det er en benzenring), når den reagerer med en base danner saltene av benzoat. I alle karboksilater gruppen -co- Representerer en (RAX).
Litium diaquilcupratos
Litiumdag er nyttig i organisk syntese. Formelen er [r-cu-r]-Li+, der kobberatomet har en negativ belastning. Her representerer kobber atomet i bildet.
Sulfoniumsalter
De dannes fra reaksjonen av et organisk sulfid med et alkylhalogenid:
R2S + r'x => r2R+X
For disse saltene bærer svovelatom en positiv formell belastning (S+) med tre kovalente lenker.
Oxyio salter
På samme måte reagerer eterne (de oksygenerte analogene av sulfidene) med hydraceidene for å danne oksyrommene:
Ror ' + hbr ro+HR ' + BR-
HBR -syreprotonet er konsekvent knyttet til eterens oksygenatom (r2ENTEN+-H), lading det positivt.
Amina salter
Aminer kan være primær, sekundær, tertiær eller kvartær, akkurat som saltene sine. Alle av dem er preget av å ha et atom av H knyttet til nitrogenatom.
Dermed RNH3+X- Det er et primært aminsalt; R2NH2+X-, av sekundær amina; R3NH+X-, av tertiær amin; og r4N+X-, av kvartær amin (kvartær ammoniumsalt).
Diazoniumsalter
Endelig diazoniumsalter (RN2+X-eller arildiazonium (RNA2+X-), representerer de utgangspunktet for mange organiske forbindelser, spesielt de azoiske fargestoffene.
Referanser
- Francis a. Tortoiseshell. Organisk kjemi (sjette utgave, PP. 604-605, 697-698, 924). Mc Graw Hill.
- Graham Solomons t.W., Craig f. Yngel. Organisk kjemi. Aminer (10. utgave.). Wiley Plus.
- Wikipedia (2018). Salt (kjemi). Hentet fra: i.Wikipedia.org
- Steven a. Hardinger (2017). Illustrert ordliste over organisk kjemi: salter. Gjenopprettet fra: Chem.UCLA.Edu
- Chevron Oronite (2011). Karboksylater. [PDF]. Gjenopprettet fra: Oronite.com

