Kromoksyd (III) struktur, nomenklatur, egenskaper, bruk

- 751
- 149
- Marius Aasen
Han Kromoksid (III) U kromoksid er et uorganisk grønt fast stoff som dannes ved å brenne krommetall (CR) i oksygen (eller2), og etterlater krom med oksidasjonstilstand 3+. Den kjemiske formelen er CR2ENTEN3. I naturen finnes det i Eskolaíta -mineralet. Naturlige avsetninger av kromoksid (III) er ikke kjent.
Det kan utarbeides blant andre måter ved å varme opp CR2ENTEN3 hydrert (Cr2ENTEN3.NH2O) For å fjerne vann helt. Det oppnås også som et produkt av kromoksydkalsinering (VI) (CRO3).
 Kromoksidpigment (III). FK1954 [Public Domain]. Kilde: Wikipedia Commons
Kromoksidpigment (III). FK1954 [Public Domain]. Kilde: Wikipedia Commons Imidlertid er den beste måten å oppnå den ren ved nedbrytning av ammoniumdikromatet (NH4)2Cr2ENTEN7 ved 200 ºC. Industrielt er produsert ved reduksjon av natriumdikromat (NA2Cr2ENTEN7) fast med svovel.
Når den er fint delt, presenterer den en lysegrønn farge med gulaktig nyanse. Men hvis partiklene er større, viser den et blåaktig fargestoff. Kromoksid er det mest stabile grønne pigmentet som er kjent. Den termiske og kjemiske motstanden gjør det til et verdifullt keramisk fargestoff.
Det brukes i industrielle belegg, lakk, i byggebransjen, i smykker, som en fargelegging i kosmetikk eller i farmasøytiske produkter, blant andre applikasjoner.
[TOC]
Struktur
Α-Cr-oksid2ENTEN3 Den har Corindon -typen struktur. Det krystallinske systemet er rhomboonisk sekskantet. Er isomorf med a-aluminiumoksyd og α-FE2ENTEN3.
Eskolaíta, naturlig mineral av kromoksid (III), presenterer strukturen vist nedenfor:
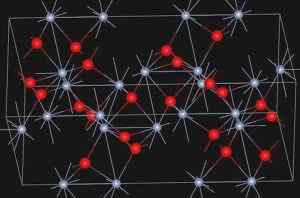 Krystallstruktur av Eskolaíta mineral. https: // last opp.Wikimedia.org/wikipedia/commons/e/ee/esskolaite_structure.Jpg. Kilde: Wikipedia Commons
Krystallstruktur av Eskolaíta mineral. https: // last opp.Wikimedia.org/wikipedia/commons/e/ee/esskolaite_structure.Jpg. Kilde: Wikipedia Commons Nomenklatur
- Kromoksid (III).
- Grønt kromoksid.
- Dichroma -trioksid.
- Krom Seasquioxide.
- Krom.
- Eskolaíta: Chrome Oxide Mineral (III).
- Hydrat: Cr2ENTEN3.NH2Eller (hvor n ≅ 2) kalles kromoksydhydrat (III) eller Guignet Green.
 Kromoksydhydrat (III). W. Oelen [CC BY-SA 3.0 (https: // creativecommons.Org/lisenser/by-SA/3.0)]. Kilde: Wikipedia Commons
Kromoksydhydrat (III). W. Oelen [CC BY-SA 3.0 (https: // creativecommons.Org/lisenser/by-SA/3.0)]. Kilde: Wikipedia Commons Egenskaper
Fysisk tilstand
Krystallinsk fast.
Mohs hardhet
9 (krystallene deres er ekstremt harde).
Molekylær vekt
151,99 g/mol.
Kan tjene deg: kvartære forbindelser: egenskaper, trening, eksemplerSmeltepunkt
Smelter ved 2435 ºC, men det begynner å fordampe til 2000 ºC som danner skyer av grønn røyk.
Tetthet
5.22 g/cm3
Løselighet
Når det er blitt oppvarmet ved høye temperaturer, er den praktisk talt uoppløselig i vann (3 mikrogram/l ved 20 ºC); uoppløselig i alkoholer og aceton; litt oppløselig i syrer og alkalier; Perklorsyre ssoluble (Hclo4) til 70%, der det går i stykker.
Ph
6.
Brytningsindeks
2.551.
Andre egenskaper
- Hvis den er sterkt kalsinert, blir den inert mot syrer og baser. Ellers Cr2ENTEN3 og den hydratiserte formen CR2ENTEN3.NH2O De er amfoterisk, løses lett opp i syre for å gi aqua -ions [CR (h2ENTEN)6]3+, og i konsentrert alkali for å danne "kromitos".
- Når det er blitt kalsinert, er den kjemisk motstandsdyktig mot syrer, alkalier og høye temperaturer. Er ekstremt stabil mot så2.
- Den har en enestående lysmotstand fordi krystallene har opacitet, høy UV -demping og åpenhet mot synlig lys.
- Det er et ekstremt hardt materiale, du kan skrape kvarts, Tapacio og Zirconio.
- Dets hydrat Cr2ENTEN3.NH2Eller (der n ≅ 2) ikke har termisk stabilitet, begrenser hydreringsvannet dens anvendbarhet til mindre enn 260 ºC. Den presenterer lav fargingskapasitet og begrenset nyanse av nyanser.
- Men dette hydratet har en veldig ren og lysgrønn blå fargetone. Det er semi -transparent, presenterer lav opacitet, utmerket motstand mot lys og motstand mot alkalier.
- Cr2ENTEN3 Det er ikke klassifisert som farlig materiale og regnes som et inert fint pulver. Det er ikke underlagt internasjonale transportforskrifter.
- Irriterer ikke huden eller slimhinnene.
applikasjoner
I keramikk- og glassindustrien
På grunn av sin høye motstand mot varme og kjemisk motstand, CR2ENTEN3 Kalsinert brukes som fargelegging eller forutsigbar pigment i keramisk produksjon, i porselensemaljer og blandinger for glass.
I industrielle belegg
Keramikk med kromoksid (III) gir utmerket motstand mot de fleste korrosive miljøer. Alt dette gjennom mekanismen for ekskludering av det omkringliggende underlaget.
Av denne grunn brukes det i belegg for å forhindre korrosjon av mange materialer, og brukes av termisk spray (forstøvning eller varm dugg).
Kan tjene deg: Kjemisk prosess: Prinsipper, typer, eksemplerDet brukes også som beskyttelse mot slitasje slitasje (når fjerning av materialet er forårsaket av partikler som beveger seg gjennom en overflate).
I disse tilfellene er bruken av et CR -belegg2ENTEN3 Ved avsetning med plasma genererer det høy slitemotstand.
De to foregående sakene har for eksempel nytteverdi i gassturospacial turbinmotorer.
I den ildfaste industrien
Det brukes i termisk og kjemisk resistente murstein, beleggmaterialer og aluminiumoksydbasert ildfast betong.
Under konstruksjon
Siden det er ekstremt motstandsdyktig mot atmosfæriske forhold, lys og varme, påføres det som et granulert fjellfargestoff for asfalttak, betongsement, industrielle belegg av høy kvalitet for utvendige, stålkonstruksjoner og fasader belegg (emulsjonsbare malinger).
Som pigment i varierte applikasjoner
Det kan støtte vulkaniseringsbetingelser og brytes ikke ned, så det brukes i gummi -pigmentering.
Fordi de er ikke-tekniske, brukes det som et pigment for leker, kosmetikk (spesielt dets hydrat), plast, utskriftsblekk, malerier som kommer i kontakt med mat og farmasøytiske produkter.
I pigmentindustrien brukes det som råstoff for å produsere gjennomtrengende fargestoffer som inneholder krom og pigmenter basert på faser av blandede metalloksider. Det brukes også som en fargelegging av malerier for spiralbelegging.
Hydratet har en åpenhet som tillater formulering av polykromatiske utførelser i bilindustrien (metallisk bilfinish).
På grunn av dets unike kjennetegn ved å reflektere infrarød stråling (IR) som lignende planter klorofyll, under infrarødt lys virker det løvverk. Av denne grunn er bruken i kamuflasjemalerier eller belegg for militære applikasjoner veldig utbredt.
I smykker
Det brukes som et fargestoff av syntetiske perler. Når CR blir introdusert2ENTEN3 som urenhet i det krystallinske nettverket av α-al2ENTEN3, Som i det semi-faste rubinmineralet er fargen rød i stedet for grønn.
Det brukes også som et slipemiddel og polert for høye hardhets- og slitende egenskaper.
På kjemiske reaksjoner
Støttet i aluminiumoksyd (til2ENTEN3) eller andre oksider, brukes i organisk kjemi som katalysator, for eksempel ved hydrogenering av estere eller aldehyder for å danne alkoholer og i hydrokarbon -syklisering. Katalyserer reaksjonen av nitrogen (n2) med hydrogen (h2) For å danne ammoniakk (NH3).
Det kan tjene deg: litium: historie, struktur, egenskaper, risikoer og bruksområderFor sin oksidreduksjonskapasitet som virker sammen med kromoksid (VI) spiller en viktig rolle i dehydrogenering av alkaner2 Å produsere Propeno og Isobuten, siden katalysatordeaktivering-reaktiveringssyklusen er lett kjørbar. Det brukes også som en katalysator i uorganisk kjemi.
I kromproduksjon
Det brukes i ren krom metall aluminternotermisk produksjon. For å gjøre dette, må det varmes opp til 1000 ºC for å øke kornstørrelsen.
 Krommetallforberedelse ved aluminaoterm reduksjon av kromoksid (III). Rando Tuikene [CC By-SA 4.0 (https: // creativecommons.Org/lisenser/by-SA/4.0)]. Kilde: Wikipedia Commons
Krommetallforberedelse ved aluminaoterm reduksjon av kromoksid (III). Rando Tuikene [CC By-SA 4.0 (https: // creativecommons.Org/lisenser/by-SA/4.0)]. Kilde: Wikipedia Commons I magnetiske materialer
Det er lagt til i små mengder til magnetiske materialer av lyd- og videobånd ved å lære en selv -imponerende effekt til lydhoder.
Nyere innovasjoner
Det er oppnådd pigmenter som har forbedret refleksjonen av nesten å gå til Dopar CR -nanopartikler2ENTEN3 med salter av elementer som tilhører den sjeldne jordgruppen, som Lantano og praseodimio.
Øk konsentrasjonen av disse elementene øker solens refleksjon av de nærmeste infrarøde øker uten å påvirke den grønne fargen på CR -grisen2ENTEN3.
Dette gjør det mulig å klassifisere CR2ENTEN3 Doping som "kaldt" pigment, fordi det er egnet for å kontrollere varmeopphopning.
Anvendt i tak, biler og møbeltrekk, oppnår blant annet høy refleksjon av IR -sollys, noe som gjør at vi kan redusere varmeøkningen betydelig i miljøer.
Referanser
- Bomull, f. Albert og Wilkinson, Geoffrey. (1980). Avansert uorganisk kjemi. Fjerde utgave. John Wiley & Sons.
- Kirk-Ohmer (1994). Encyclopedia of Chemical Technology. Volum 19. Fjerde utgave. John Wiley & Sons.
- Ullmanns Encyclopedia of Industrial Chemistry. (1990). Femte utgave. Volum A7 og A20. VCH Verlagsgellschaft MBH.
- Amerikanske elementer. (2019). Krom (iii) oksid. Gjenopprettet fra amerikanementer.com.
- National Library of Medicine. (2019). Krom (iii) oksid. Gjenopprettet fra: Pubchem.NCBI.NLM.NIH.Gov.
- Dorfman, Mitchell R. (2012). Termisk spraybelegg. I håndbok for miljøforringelse av materialer. Kapittel 19. Gjenopprettet fra Scientedirect.com.
- Takehira, k. et al. (2004). Co2 Dehydrogenering av propan over CR-MCM-41-katalysator. I studier i overflatevitenskap og katalyse 153. Gjenopprettet fra Scientedirect.com.
- Selvam Sangeetha et al. (2012). Funksjonelle pigmenter fra krom (iii) nanopartikkeloksid. Fargestoffer og pigmenter 94 (2012) 548-552. Gjenopprettet fra Scientedirect.com.

