Etylenoksidstruktur, egenskaper, risikoer og bruk
- 4874
- 1359
- Jonathan Carlsen
Han etylenoksid Det er en organisk forbindelse av epoksydfamilien. Ved romtemperatur er det gassform.
Det er en veldig allsidig kjemisk konstruksjonsblokk, siden den brukes i et bredt utvalg av industrielle anvendelser for fremstilling av andre kjemiske forbindelser med flere bruksområder. Dette skyldes den høye reaktiviteten, det vil si at det er lett å reagere med andre stoffer.
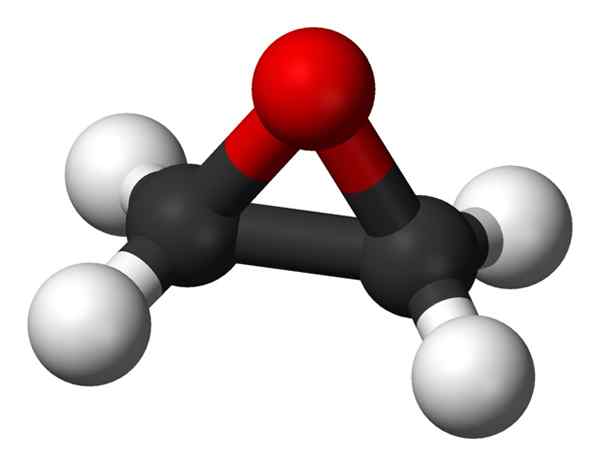
 Romlig struktur av etylenoksyd. Svarte baller: karbonatomer; Hvite baller: hydrogenatomer; Rød ball: oksygenatom. Benjah-BMM27 [Public Domain]. Kilde: Wikimedia Commons.
Romlig struktur av etylenoksyd. Svarte baller: karbonatomer; Hvite baller: hydrogenatomer; Rød ball: oksygenatom. Benjah-BMM27 [Public Domain]. Kilde: Wikimedia Commons. En av de viktigste applikasjonene er som råstoff i produksjonen av komponentene i frostvæske for kjøretøyradiatorer. Derivater er ansatt som ingredienser i industrielle eller hjemmene, kosmetiske produkter og sjampoer, plastisering, farmasøytiske preparater eller salver.
Det er et mye brukt desinfeksjonsmiddel, for eksempel ved sterilisering av medisinsk og tannhelseutstyr, siden det er i stand til å ødelegge virus, bakterier, sopp og sporer, spesielt under tørre forhold. I tillegg har den blitt brukt til å fumre matprodukter til pakket, selv om denne bruken blir stilt spørsmål ved.
Til tross for nytten, må den manipuleres med høy forsiktighet, da det kan forårsake irritasjon i øynene og huden. Innånding av etylenoksid i lange perioder kan påvirke nervesystemet. Derfor må personer som blir utsatt for damper eller løsninger bruke verneutstyr og klær.
[TOC]
Struktur
Den molekylære formelen er C2H4ENTEN. Det tilhører gruppen av epoksider, og er den enkleste og viktigste av disse. Den har formen som en tre -medlemsring.
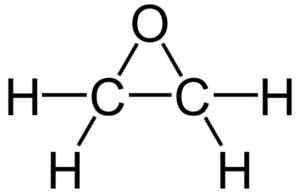 Etylenoksidstruktur. Kilde: Wikimedia Commons
Etylenoksidstruktur. Kilde: Wikimedia Commons På grunn av sin trekantede ringstruktur er etylenoksyd veldig reaktiv, noe som skyldes hvor enkelt ringen åpnes. I gjennomsnitt er koblingsvinklene 60º, noe som gjør koblingene deres svake. Molekylet er mindre stabilt enn for en lineær eter og har en tendens til å reagere lett med andre kjemiske forbindelser.
Kan tjene deg: natriumnitritt (nano2): struktur, egenskaper, bruksområder, risikoEgenskaper
Andre navn
- Oxyran.
- Epoxietano.
Fysisk tilstand
Ved romtemperatur og under atmosfæretrykk er det en gass. Under 10,6 ºC og under atmosfæretrykk er det en væske. Under -111 ºC er et faststoff.
Molekylær vekt
44,05 g/mol.
Flashpoint
Mindre enn 0 ºF (-17,8 ºC).
Tetthet
Dens tetthet er mindre enn vannet, og er 0,882 til 10 ºC. På sin side er deres damper tyngre enn luft.
Løselighet
Det er løselig i vann, benzen, aceton, etanol og eter. Det er blandbar med karbontetraklorid.
Selvordemperatur
428,9 ºC.
Andre egenskaper
- Hvis det gjennomgår oppvarming eller forurensning, kan det polymerisere eksotermisk (produsere en stor mengde varme). Hvis polymerisasjon oppstår i en beholder, kan den brytes voldsomt.
- Kan reagere med oksidasjonsmaterialer.
- Det er ekstremt giftig, kreftfremkallende og god mutasjonsgenerator i bakterier og pattedyrceller.
Produksjon
I industriell skala er det fremstilt ved oksidasjon av etylen med oksygen (eller2) fra luft. Hastigheten på denne reaksjonen økes med tilstedeværelsen av sølvmetall (Ag) og temperaturvirkning. Deretter vises reaksjonen:
AG, 250 ºC
2 c2H4 + ENTEN2 -> 2c2H4ENTEN
Etylenetylenoksid
Risiko
Til helse
- Det er rapportert at det produserer nevrologiske lidelser og at døden kan forårsake. Den lavere konsentrasjonen som kan generere toksiske effekter ved innånding er 12.500 ppm/10 sekunder (ppm betyr: deler per million).
- Det er en sterk irriterende hud, øyne og luftveier.
Kan tjene deg: samario: egenskaper, struktur, innhenting, bruk- Dampeksponering med høy konsentrasjon av etylenoksyd kan forårsake øyeirritasjon, betennelse i øyemembranen og hornhinneskaden.
- Utviklingen av grå stær har vært assosiert med eksponering for damper og sprut. Med konsentrerte løsninger er det alvorlig skade på øynene.
- Kontakten med vandige oppløsninger av etylenoksid med huden gir irritasjon og kan føre til alvorlig dermatitt med ampuller og forbrenninger.
- Innånding kan påvirke nervesystemet og forårsake hodepine og kvalme, blant andre symptomer.
Brann
- Når det blir utsatt for en flamme eller varme er det fare for eksplosjon. Når de oppvarmes, genererer de farlige damper.
- Damp danner eksplosive blandinger med luft i et bredt spekter av konsentrasjoner.
- Det bør unngås å manipulere det med utstyr som inneholder metaller som kobber, sølv, kvikksølv, magnesium, aluminium eller jernoksider, i tillegg til å unngå midler som ammoniakk, oksidasjonsmidler, syrer eller organiske baser, blant andre. Alle disse materialene kan akselerere polymerisasjonen og/eller eksplosjonen.
applikasjoner
Industrielle applikasjoner
Det brukes som en mellomledd i produksjon av andre kjemikalier, som igjen brukes i fremstilling av polyesterfibre for klær, møbeltrekk, tepper og puter.
Med etylenoksid brukes etylenglykol i frostvæske for kjøretøymotorer. Etylenglykol brukes også i glassfiberproduksjon og plastfilmer for emballasje.
Andre kjemikalier produsert fra etylenoksid inkluderer ikke -ioniske overflateaktive midler som brukes i vaskemidler og formler for å vaske oppvasken.
Kan tjene deg: Isobutil: Nomenklatur, trening, struktur og egenskaperMedisinske applikasjoner
Det brukes som et steriliseringsmiddel for medisinsk utstyr, for eksempel kirurgiske instrumenter, hypodermiske nåler og injektorer eller proteser.
Det brukes også til å sterilisere maskiner for hemodialyse, laboratorieutstyr, tanninstrumenter, veterinærinstrumenter, termometre, kirurgiske klær eller førstehjelpsutstyr, blant andre.
 Steriliseringsrom. Kilde: Pixabay.com
Steriliseringsrom. Kilde: Pixabay.com Selv om det er flere metoder tilgjengelig for sterilisering av medisinsk utstyr, kan ingen tilgjengelig behandling erstatte etylenoksyd.
Dette er tilfellet med sterilisering av visse varmefølsomme materialer og stråling, samt noen instrumenter og gjenstander som krever sterilisering på sykehusets sted selv.
Biblioteker og museer
På disse stedene brukes etylenoksid til å kontrollere skadedyr som sopp og insekter. Imidlertid er denne bruken ikke så vanlig og brukes når andre alternativer ikke er effektive.
Landbruk og mat
Det har blitt brukt som plantevernmiddel, soppdrepende, fumigant, ugressmiddel, insektmiddel, gnagermiddel, blant andre varianter. Reduserer populasjonen av bakterier og krydder sopp betydelig.
På grunn av sikkerhets- og miljøhensyn har imidlertid bruk av etylenoksid for matfumigering blitt forbudt i EU og i USA.
Referanser
- ELLER.S. National Library of Medicine. (2019). Ethylenoksid. Gjenopprettet fra Pubchem.NCBI.NLM.NIH.Gov
- Kjemiske sikkerhetsfakta. (2019). Ethylenoksid. Gjenopprettet fra kjemikalieresikkerhetsfakta.org
- Morrison, Robert Thornton; og Boyd, Robert Neilson. 1992. Organisk kjemi. Prentice-Hall.
- Moerman, f. og Mager, K. (2016). Rengjøring og dissinfeksjon i tørrmatforedlingsanlegg. I Handbook of Hygiene Control in the Food Industry (Second Edition). Gjenopprettet fra ScientIrect.com.
- Eastmond, David A. og Balakrishnan, Sharada. (2010). Genotoksy av plantevernmidler. I Hayes 'Handbook of Pesticide Toxicology (tredje utgave). Gjenopprettet fra Scientedirect.com
- Atungulu, g.G. og brød, z. (2012). Mikrobiell dekontaminering av nøtter og krydder. I mikrobiell dekontaminering i matindustrien. Gjenopprettet fra Scientedirect.com
- « Jernoksid (II) struktur, nomenklatur, egenskaper, bruk
- Enkle flate epitelegenskaper, funksjoner og typer »

