Blyacetatstruktur, egenskaper, innhenting, bruk

- 1890
- 305
- Prof. Joakim Johansen
Han Blyacetat o Blyacetat (II) er en forbindelse dannet av et blyion (PB2+) og to acetationer (CH3COO-). Den kjemiske formelen er (Cho3Coo)2PB eller også PB (velg3Coo)2.
Det er også kjent som "bly sukker" for å ha en søt smak. Imidlertid er det et veldig giftig stoff. Det er et veldig oppløselig krystallinsk fast stoff i vann. Du kan enkelt reagere med hydrogensulfid (h2S) Generering av brun blygsulfid (PBS), som brukes i påvisning av denne giftige gassen i industrielle prosesser.
 Solid bly (ii) acetat. Dormoothemist på engelsk Wikipedia/CC av (https: // creativecommons.Org/lisenser/av/3.0). Kilde: Wikimedia Commons.
Solid bly (ii) acetat. Dormoothemist på engelsk Wikipedia/CC av (https: // creativecommons.Org/lisenser/av/3.0). Kilde: Wikimedia Commons. I eldgamle tider ble det oppnådd med relativt letthet, så den hadde bruk som for øyeblikket er fullstendig forbudt på grunn av toksisiteten til denne forbindelsen.
Blyacetatpulver skal ikke spres i miljøet, da det danner eksplosive blandinger med oksygen. I tillegg er det en kreftfremkallende forbindelse for dyr og mennesker.
Det absorberes i organiske vev lettere enn andre blyforbindelser. Det har en tendens til å bioakkumulere hos levende vesener, så det skal ikke kastes til miljøet.
[TOC]
Struktur
Blyacetatet (ii) har strukturen vist på figuren nedenfor:
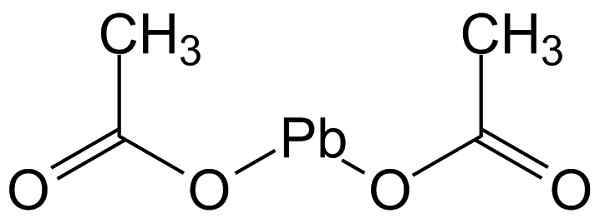 Molekylær struktur av blyacetat (II). Michał Sobkowski/CC By-SA (https: // CreativeCommons.Org/lisenser/by-SA/3.0). Kilde: Wikimedia Commons.
Molekylær struktur av blyacetat (II). Michał Sobkowski/CC By-SA (https: // CreativeCommons.Org/lisenser/by-SA/3.0). Kilde: Wikimedia Commons. Nomenklatur
- Blyacetat (ii)
- Bly diacetate
- Føre etanoat
- Plumboso -acetat
- Bly sukker
- Saturnsalt
Egenskaper
Fysisk tilstand
Krystallinsk fargeløs til hvit.
Molekylær vekt
325 g/mol
Smeltepunkt
280 ºC
Kokepunkt
Ikke koke. Han bryter sammen når han er oppvarmet.
Tetthet
3,25 g/cm3
Løselighet
Veldig løselig i vann: 44,3 g/100 ml ved 20 ° C. Uoppløselig i alkohol.
Ph
En vandig løsning til 5% har en pH på 5,5-6,5.
Kjemiske egenskaper
Når PB (OCOCH3)2 Den oppløses i vann en del er ionisert som følger:
PB (Ococh3)2 → Pb2+ + 2 Ch3COO-
En del av molekylene er imidlertid ikke ionisert og forblir i form:
Ch3COO-PB-OCOCH3.
Når PB -ionen2+ Angi løsning delvis hydrolyser i vann som genererer PB -arten4(ÅH)44+.
Vandig Pb (II) acetatløsninger oppløs blyoksyd (PBO).
Det kan tjene deg: ButenoReagerer med hydrogensulfid (h2S) for å danne en brun bly av bly -sulfid (PBS).
PB (Ococh3)2 + H2S → PBS + 2 CH3COOH
Hvis en vandig ammoniakkoppløsning tilsettes (NH3) Et hvitt bunnfall eller hvitt acetat faststoff av basisk acetat dannes til en bly av blyacetat.
Andre egenskaper
Avgir en lukt som ligner på eddik. Den har en søt smak. Den vanligste kommersielle formen er Pb -trihydrat (CH3Coo)2 •3H2ENTEN.
 Blyacetat trihydrat. Leiem/CC By-SA (https: // CreativeCommons.Org/lisenser/by-SA/4.0). Kilde: Wikimedia Commons.
Blyacetat trihydrat. Leiem/CC By-SA (https: // CreativeCommons.Org/lisenser/by-SA/4.0). Kilde: Wikimedia Commons. Å skaffe
Det kan fremstilles ved å løse opp oksyd eller føre karbonat (II) i konsentrert eddiksyre. Små tynne metalliske blyplater kan også brukes.
PBO + 2 CH3COOH → (CH3Coo)2PB + H2ENTEN
Antikkens bruk
I medisin
Den ble brukt i fortynnet løsning for å påføre den som fjærkre og vasket i betennelser forårsaket av giftig eføy og som en snerpende i kremer. Også for å behandle diaré.
I veterinærbehandlinger
Den ble brukt som en snerpende og beroligende lotion i behandlingen av overfladiske betennelser og blåmerker.
I kosmetikk
Den ble produsert i eldgamle romertiden. Noen kvinner brukte det i ansiktet for å virke bleke, noe som ikke bare var en mote, men et spørsmål om sosial status.
En hvit hudfarge indikerte at kvinnen ikke tilhørte arbeiderklassen, men til de høyeste nivåene i det romerske samfunnet. Og dette skjedde til tross for at datidens leger, som Plinio El Viejo, kjente noen av dens skadelige effekter.
Som søtningsmiddel av drikke
På grunn av sin søte smak ble den brukt i antikken som erstatning for sukker, spesielt i vin og for å blidgjøre og spare frukt.
I flere applikasjoner
Noen av disse bruksområdene gjelder fortsatt, men litteraturen som er konsultert er ikke klart om det:
- I krompigmenter, som en komponent i limfargestoffer, i tørre organiske såper for malerier, lakker og blekk, for eksempel vannavvisende, i anti -bitende maling.
- I prosessen med å skaffe gull av cyanider, for å dekke metaller med bly.
- Som mordant i bomullsfargestoffer, komponent av å fikse bad for å trykke papir med sollys.
- Å behandle markiser og utemøbler og dermed forhindre fjerning av midler som beskytter mot mugg og regnforringelse.
Nåværende bruksområder
I H -deteksjon2S
I visse industrielle prosesser brukes det til å oppdage giftig h2S i gassformige strømmer gjennom en prøvelsesrolle der den fungerer som en indikator. Deteksjonsgrensen er 5 ppm (deler per million).
 Blyacetat (ii) tillater å oppdage h2S i industrikasser slik at denne giftige gassen ikke frigjøres til atmosfæren. Forfatter: Leestilltaolcom. Kilde: Pixabay.
Blyacetat (ii) tillater å oppdage h2S i industrikasser slik at denne giftige gassen ikke frigjøres til atmosfæren. Forfatter: Leestilltaolcom. Kilde: Pixabay. I nyere tester har nanofibras blitt inkorporert sammen med en polymer som resulterer i et nytt deteksjonsmateriale som tillater tilstedeværelse av 400 ppb (deler per milliard) H2S til og med fuktighet på 90%.
Det høye potensialet til dette nanomaterialet som en kolorimetrisk sensor gjør det anvendelig for påvisning av H2S i pusten av mennesker som lider av halitose, hvis rekkevidde er under 1 ppm.
 De nye nanofibrene som inneholder PB (CH3Coo)2 De kan oppdage veldig små mengder h2S i pust. Forfatter: Natalia Ovcharenko. Kilde: Pixabay.
De nye nanofibrene som inneholder PB (CH3Coo)2 De kan oppdage veldig små mengder h2S i pust. Forfatter: Natalia Ovcharenko. Kilde: Pixabay. Ved å få andre forbindelser
Det gjør det mulig å fremstille andre blyforbindelser som karbonat og kromat, bly -salter med høy molekylvekt og antioksidantfettsyrer for gummi.
For ekstern bruk
I følge noen konsulterte kilder, brukes denne forbindelsen fremdeles i hårfargestoffer hvis anvendelsesindikasjoner advarer om at den ikke skal brukes i andre deler av kroppen som er annerledes enn hodebunnen.
Det er også en del av ekstern bruk smertestillende produkter og hudbeskyttere.
I begge tilfeller er det imidlertid ikke nok bevis for å fastslå graden av sikkerhet for disse produktene, så i land som Canada og i den amerikanske delstaten California, har bruken av den i alle typer kosmetikk eller for anvendelse blitt forbudt på huden.
Risiko
For sikkerhet
Det er ikke drivstoff, men det er spredt i miljøet i form av fine partikler kan generere eksplosive blandinger med luften.
Det skal lagres langt fra oksidasjonsforbindelser, sterke syrer og kjemisk aktive metaller, og i områder uten avløp eller tilgang til kloakk som fører til kloakk.
Til helse
Det kan irritere øynene, luftveiene og fordøyelsen, forårsake hodepine, kvalme, oppkast, kolikk, muskelsvakhet, kramper, anfall, lammelse, svimmelhet, tap av bevissthet, koma og til og med død.
Det kan tjene deg: hyposulfurous acidBlyacetat absorberes rundt 1,5 ganger raskere enn andre blyforbindelser.
 Blyacetat påvirker barns hjerne negativt. Forfatter: Pete Lyforth. Kilde: Pixabay.
Blyacetat påvirker barns hjerne negativt. Forfatter: Pete Lyforth. Kilde: Pixabay. En veldig lav blodkonsentrasjon hos barn kan forårsake hyperaktivitet eller nevrokonductuell funksjonshemming, da det gir effekter på nervesystemet. Det kan også produsere anemi og skade på nyrene.
Når det gjelder dyr, har det blitt bevist tilstrekkelig at det er giftig for reproduksjon, kreftfremkallende. Det anslås at mennesker påvirker på samme måte.
For miljøet
Det regnes som et farlig stoff for miljøet, ettersom det er en giftig miljøgifter. Det er veldig skadelig for vannlevende organismer. Spesiell oppmerksomhet bør rettes mot fugler, pattedyr, jordforurensning og vannkvalitet.
Bioakumulering av denne forbindelsen i planter og dyr kan oppstå. Internasjonale økologiske institusjoner tillater sterkt ikke å komme inn i miljøet fordi det er vedvarende.
Historisk forgiftningssak
En av hendelsene som ble studert har vært den av presidenten i USA Andrew Jackson (1767-1845), som gjennomgikk en behandling med "bly sukker", som på den tiden var et tradisjonelt middel med varierte formål.
I 1999 ble det foretatt tiltak for to hårprøver oppnådd i presidentens liv, og det ble funnet at blynivået var veldig høye i begge prøvene, noe som er kompatibelt med symptomene på plumbismen som led.
 Andrew Jackson var beruset av blybaserte rettsmidler. Forfatter: Gordon Johnson. Kilde: Pixabay.
Andrew Jackson var beruset av blybaserte rettsmidler. Forfatter: Gordon Johnson. Kilde: Pixabay. Både brevene deres og deres biograf beskriver at han presenterte symptomer som kvalme, abdominal kramper og lammetisk revmatisme, blant andre. Men etter en stund forlot Jackson behandlingen av blyacetat, så helsen hans ble bedre.
Derfor anslås det at hans død sannsynligvis ikke skyldtes blyforgiftning.
Referanser
- ELLER.S. National Library of Medicine. (2019). Bly (ii) acetat. Gjenopprettet fra Pubchem.NCBI.NLM.NIH.Gov.
- Bly, d.R. (Editor) (2003). CRC Handbook of Chemistry and Physics. 85th CRC Press.
- Bomull, f. Albert og Wilkinson, Geoffrey. (1980). Avansert uorganisk kjemi. Fjerde utgave. John Wiley & Sons.
- Ghazi, a.M. og Millette, J.R. (1964). Lede. Blyacetat. I rettsmedisinsk miljø. Gjenopprettet fra Scientedirect.com.
- Mushak, p. (2011). Bly og folkehelse. I spormetaller og oher forurensninger i misunnelsen. Gjenopprettet fra Scientedirect.com.
- Cha, J.-H. et al. (2018). Underdeler-per-million hydrogensulfid kolorimetrisk sensor: bly achored nanofibers mot halitosediagnose. Anal Chem 2018 7. august; 90 (15): 8769-8775. NCBI kom seg.NLM.NIH.Gov.
- Wikimedia Foundation (2020). Bly (ii) acetat. Innhentet fra.Wikipedia.org.
- Stewart, s. (2015). "Skinnende og dødelig hvit". En rettferdig hudfarge. I historien om toksikologi og miljøhelse. Gjenopprettet fra Scientedirect.com.
- Deppisch, l.M. et al. (1999). Andrew Jacksons eksponering for Mercury and Lead: Poisoned President? Jama 1999 11. august; 282 (6): 569-71. NCBI kom seg.NLM.NIH.Gov.
- « Bly nitratkonstruksjon, egenskaper, innhenting, bruker
- Bly jodstruktur, egenskaper, innhenting, bruk »

