Hjerteautomatisme
- 1079
- 15
- Anders Mathisen
 Hjerteautomatisme er eiendommen som lar hjertet automatisk kunne
Hjerteautomatisme er eiendommen som lar hjertet automatisk kunne Hva er hjerteautomatisme?
Han Hjerteautomatisme Det er muligheten til å vurdere myokardceller for seg selv. Denne egenskapen er unik for hjertet, siden ingen andre kroppsmuskler kan adlyde ordrer diktert av sentralnervesystemet. Noen forfattere anser kronotropisme og hjerteautomatisme som fysiologiske synonymer.
Bare høyere organismer har denne egenskapen. Pattedyr og noen krypdyr er blant levende vesener med hjerteautomatisme. Denne spontane aktiviteten genereres i en gruppe spesialiserte celler som produserer periodiske elektriske svingninger.
Selv om mekanismen som denne pacemaker -effekten begynner, er det kjent at ionekanaler og konsentrasjonen av intracellulært kalsium spiller en grunnleggende rolle i deres operasjon fremdeles er kjent nøyaktig. Disse elektrolytiske faktorene er viktige i dynamikken i cellemembranen, som utløser handlingspotensialer.
For at denne prosessen skal utføres uten endringer, er erstatning av de anatomiske og fysiologiske elementene viktig. Det komplekse nettverket av noder og fibre som produserer og utfører stimulansen gjennom hele hjertet, må være sunt å fungere ordentlig.
Hjerteautomatisme anatomi
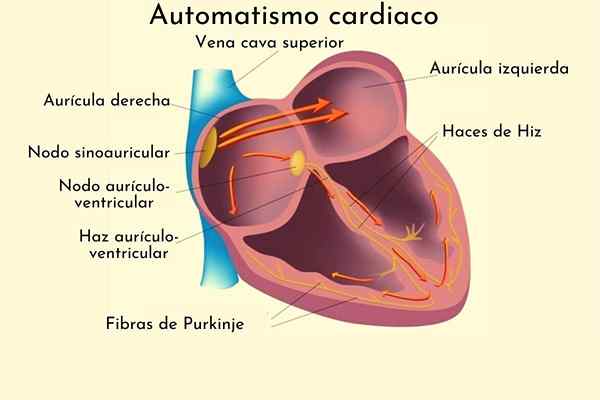
Hjerteautomatisme har en veldig intrikat og spesialisert gruppe stoffer med presise funksjoner. De tre viktigste anatomiske elementene i denne oppgaven er: bihule (eller sateoaurikulær), atrioventrikulær eller atrikkel-ventrikulær node, og Purkinje-fibernettet, hvis viktige egenskaper er beskrevet nedenfor:
Sinus nodule
Sinus, nodeknute eller Sinouauricular Nodule er den naturlige pacemakeren i hjertet. Den anatomiske beliggenheten ble beskrevet mer enn et århundre av Keith og Flack, og plasserte den i lateral og øvre region av høyre atrium. Dette området kalles venøs bihule og er relatert til inngangsdøren til den øvre vena cava.
Kan tjene deg: Acromion: Kjennetegn, typer, funksjon, patologierNoden, men er også beskrevet av flere forfattere som en struktur i form av banan, bue eller fusiform. Andre gir det ganske enkelt ikke en presis måte og forklar at det er en gruppe spredte celler i et mer eller mindre avgrenset område. Det mest vågale beskriver til og med hode, kropp og hale, som bukspyttkjertel.
Histologisk er det sammensatt av fire forskjellige typer celler: pacemaker, overgang, arbeid eller kardiomyocytter og Purkinje.
Alle disse cellene som utgjør sinusnodulen, men sateoaurikulær eller en natur.
Atrioventrikulær eller atrikkel-ventrikulær node
Også kjent som atrioventrikulær node (A-V-node) eller Aschooff-Tawara-nodule, den ligger i interatrial septum, nær åpningen av koronar sinus. Det er en veldig liten struktur, med maksimalt 5 mm på en av aksene, og er plassert i midten eller litt orientert mot det øvre toppunktet av Koch -trekanten.
Treningen hans er svært heterogen og sammensatt. Prøver å forenkle dette faktum, har forskere prøvd å oppsummere cellene som komponerer det i to grupper: kompakte celler og overgangsceller. Sistnevnte har en mellomstørrelse mellom arbeidet og bihulepacemakere.
Purkinje -fibre
Også kjent som Purkinje Fabric, skylder navnet til den tsjekkiske anatomisten Jan Evangelist Purkinje (1787-1869), som oppdaget det i 1839. Den er fordelt over den ventrikulære muskelen under endokardveggen. Dette stoffet er faktisk et sett med spesialiserte hjertemuskelceller.
Det kan tjene deg: bagasjeromsmuskler og dens egenskaper (med bilder)Den subendokardiale plottet til Purkinje har en elliptisk fordeling i begge ventrikler. Under all sin rute genereres forgreninger som trenger inn i ventrikulære vegger.
Disse grenene kan bli funnet med hverandre, noe som forårsaker anastomose eller forbindelser som hjelper deg med å distribuere den elektriske impulsen bedre.
Hvordan oppstår hjerteautomatisme?
Hjerteautomatisme avhenger av handlingspotensialet som genereres i muskelcellene i hjertet.
Dette handlingspotensialet avhenger av hele det elektriske ledningssystemet til hjertet som ble beskrevet i forrige seksjon, og den celleioniske balansen. Når det gjelder elektriske potensialer, er det variabel funksjonelle belastninger og spenninger.
Hjertehandlingspotensialet har 5 faser:
Fase 0:
Det er kjent som rask depolarisasjonsfase og avhenger av åpningen av raske natriumkanaler. Natrium, et positivt ion eller kation, kommer inn i cellen og endrer brått membranpotensialet, og beveger seg fra en negativ belastning (-96 mV) til en positiv belastning (+52 mV).
Fase 1:
I denne fasen oppstår lukkingen av de raske natriumkanalene. Det oppstår når du endrer membranspenningen og ledsages av en liten repolarisering på grunn av klor- og kaliumbevegelser, men beholder den positive belastningen.
Fase 2:
Kjent som Plateau eller "Plateau". På dette stadiet er det et positivt membranpotensial uten viktige endringer, takket være balansen i kalsiumbevegelse. Imidlertid er det sakte ionebytte, spesielt kalium.
Fase 3:
I løpet av denne fasen skjer den raske repolarisasjonen. Når de raske kaliumkanalene åpnes, forlater det interiøret i cellen, og å være et positivt ion membranpotensialet endres mot en voldsomt negativ belastning. På slutten av dette stadiet er et membranpotensial mellom -80 mV og -85 mV nådd.
Det kan tjene deg: inklFase 4:
Hvilepotensial. På dette stadiet forblir cellen rolig til den er aktivert av en ny elektrisk impuls og en ny syklus begynner.
Alle disse stadiene blir oppfylt automatisk, uten ytre stimuli. Derfra navnet på Hjerteautomatisme. Ikke alle hjerteceller oppfører seg på samme måte, men fasene er vanligvis vanlige blant dem. For eksempel mangler bihule-nodule-handlingspotensialet.
Denne mekanismen påvirkes av alle variablene som endrer hjertekronotropisme. Visse hendelser som kan betraktes som normal (trening, stress, søvn) og annen patologisk eller farmakologisk.
Referanser
- Mangoni, Matteo og Nargeot, Joël (2008). Genesis and Regulation of the Heart Automaticity. Fysiologiske anmeldelser, 88 (3): 919-982.
- Ikonnikov, Greg og Yelle, Dominique (2012). Fysiologi av hjerteatferd og kontraktilitet. McMaster Pathophysiology Review, Gjenopprettet fra: Pathophys.org
- Anderson, r. H. og samarbeidspartnere (2009). Anatomi av hjertet før systemet. Klinisk anatomi, 22 (1): 99-113.
- Ramirez-Ramirez, Francisco Jaffet (2009). Hjertefysiologi. MD Medical Magazine, 3 (1).
- Katzung, Bertram G. (1978). Automatisk i hjerteceller. Livsvitenskap, 23 (13): 1309-1315.
- Wikipedia (2018). Hjertehandlingspotensial. Hentet fra: i.Wikipedia.org

