Kalsiumkarbonatstruktur, egenskaper, formasjon, bruk

- 4531
- 255
- Oliver Christiansen
Han kalsiumkarbonat Det er en uorganisk forbindelse hvis kjemiske formel er Caco3. Det finnes hovedsakelig i mineraler som kalsitt og aragonitt. På samme måte komponerer kalksteinen, en sedimentær bergart der Calcita -mineralet er til stede.
Dette viktige metallkarbonatet oppnås industrielt ved ekstraksjon og sliping av mineralene som inneholder det; For dette formål brukes marmor hovedsakelig. En annen prosess ligger i bruken av kalsiumoksyd, som blir kalsiumhydroksyd, utfellende kalsiumkarbonat ved tilsetning av karbondioksid. På denne måten oppnås krystaller fra et bredt spekter av størrelser.
 Snegleskallet er hovedsakelig sammensatt av kalsiumkarbonat. Kilde: Pixabay.
Snegleskallet er hovedsakelig sammensatt av kalsiumkarbonat. Kilde: Pixabay. De kan også brukes til Caco Industrial Production3, I liten skala er skjellene til muslingene, eggeskallene og østersskallene der det er til stede.
Kalsiumkarbonat som er til stede i kalkstein blir oppløst av karbondioksid i vann, og genererer kalsiumbikarbonat. Denne handlingen kan forårsake hulene og er en årsak til alkalinering av vann; Hendelse av stor betydning i opprettholdelsen av livet i det.
Det har blitt brukt i konstruksjon og utdyping av skulpturer; Eksempler på dette er partneren til Athen, katedralen i Krakow og skulpturen til Abraham Lincoln i Washington. Imidlertid har mottakeligheten for surt regn redusert bruken i konstruksjonen.
Kalsiumkarbonat har hatt flere applikasjoner i bransjen som et plast- og papirfyllingsmateriale. I medisin har det blitt brukt til å kontrollere gastrisk surhet; som kostholds kalsiumtilskudd; For å kontrollere fosfatia hos pasienter med kronisk nyresvikt osv.
[TOC]
Struktur
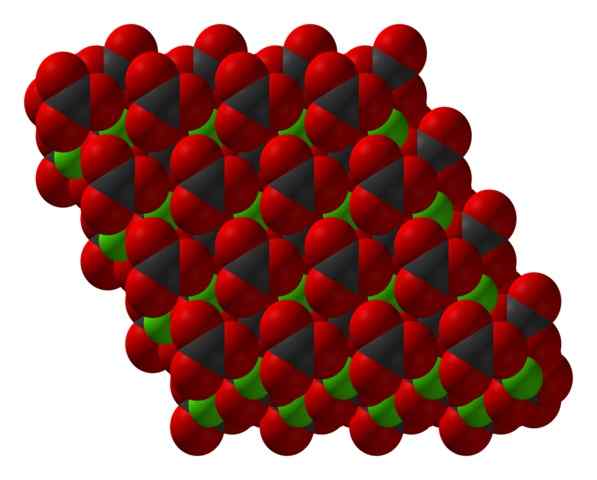 Chanco3 krystallinsk struktur representert med en romfyllmodell. Kilde: CCOIL [CC BY-SA 3.0 (https: // creativecommons.Org/lisenser/by-SA/3.0)]
Chanco3 krystallinsk struktur representert med en romfyllmodell. Kilde: CCOIL [CC BY-SA 3.0 (https: // creativecommons.Org/lisenser/by-SA/3.0)] Kalsiumkarbonatformelen, Caco3, indikerer at andelen mellom CA -ioner2+ og co32- Det er 1: 1; det vil si for hver CA2+ Det er en CO32- av motstykke som samhandler elektrostátisk med ham. Dermed ender den ioniske bindingen med å ha disse ionene for å danne strukturelle mønstre som definerer en krystall.
I det overlegne bildet vises strukturen til Caco3. Grønne kuler tilsvarer CA -kationer2+, og de røde og svarte kulene til co -anionene32-. Merk at strukturen ser ut til å være dannet av flere lag: et av kalsium, og et annet karbonat; Noe som betyr at det krystalliseres i en kompakt sekskantet struktur.
Det kan tjene deg: Ammonium Chloride (NH4CL)Denne sekskantede fasen (ß-CACO3) Tilsvarer en polymorf. Det er to andre: Ortorrombic (λ-Caco3) og en enda tett sekskantet (μ-CACO3). Det nedre bildet hjelper deg med å visualisere den glade sekskanten bedre:
 Sekskantet struktur av kalsitt. Materialsionist på engelsk Wikipedia [CC BY-SA 3.0 (https: // creativecommons.Org/lisenser/by-SA/3.0)]
Sekskantet struktur av kalsitt. Materialsionist på engelsk Wikipedia [CC BY-SA 3.0 (https: // creativecommons.Org/lisenser/by-SA/3.0)] Avhengig av temperaturen (og for dette saltet blir imidlertid trykket) ionene i deres vibrasjoner omjustert til andre strukturer; Dette er de nevnte polymorferene (β, λ og μ).
Ettersom de høres ikke godt kjent, med mindre de er nevnt med sine mineralogiske navn i en neste seksjon.
Proteinhardhet
Cacos krystaller3 De er ikke alene: de kan være vertskap for urenheter som andre metallkationer som farger dem i farger; o proteiner, som inkluderer en organisk matrise som på en eller annen måte bidrar til dens naturlige hardhet.
Proteiner reduserer spenningen som krystaller opplever fra hverandre før et trykk eller påvirkning. Som? Når det er ispedd mellom krystallene, fungerte det som om det var en "pute" (ligner på murstein-sement-lady).
Det er grunnen til at denne forbindelsen eller mineral. Det har vært en inspirasjonskilde for de som er dedikert til å utvikle nye materialer.
Egenskaper
Andre navn
-Aragonitt
-Calcito
-Volterite
-Kalsiummelk
-Tavle
-Marmor
Molmasse
100.086 g/mol.
Fysisk beskrivelse
Hvitt støvtoalett.
Smak
I likhet med kritt, smakløs.
Fusjons- og kokepunkter
Det brytes sammen fordi den slipper CO2 før til og med smelter eller koker.
Løselighet
Praktisk talt uoppløselig i vann og alkohol. Det er oppløst med brus i fortynnet eddik og saltsyrer. Hydroksider reduserer imidlertid løseligheten deres. I mellomtiden øker ammoniumsalter og karbondioksid løseligheten av kalsiumkarbonat i vann.
Tetthet
2,7 til 2,95 g/cm3.
Nedbrytning
Rundt 825 ºC er brutt ned i kalsiumoksyd (kalk) og karbondioksid (CO2).
Ph
8 til 9
Brytningsindeks
-1.7216 til 300 nm og 1 6584 til 589 nm (Calcita).
-1.5145 til 300 nm og 1 4864 til 589 nm (aragonitt).
Inkompatibiliteter
Med syrer, aluminium og ammoniumsalter.
Fusion entalpi
36 kJ/mol ved 800 ºC (kalsitt).
Kan tjene deg: molaritet: konsentrasjon, enheter, beregning, øvelserLøselighetsproduktkonstant
3.36 · 10-9 ved 25 ºC.
Hardhet
-3.0 (kalsitt)
-3.5 - 4.0 (aragonitt) på MOHS -skalaen.
Faseoverganger
Aragonitten er metastabil og endres irreversibelt til kalsitt når den varmer den i tørr luft til 400 ºC.
Reaktivitet
Kalsiumkarbonat reagerer med syrer, frigjør karbondioksid, ionisk kalsium og vann.
Kalsiumkarbonat er kombinert med mettet vann med karbondioksid, tilsvarer kullsyre (H2Co3), For å danne kalsiumbikarbonat.
Opplæring
Kritt, marmor og kalkstein, de to første mineralene og et steinete materiale den tredje, inneholder kalsiumkarbonat og er av sedimentær opprinnelse, de antas å bli dannet ved sedimentasjon av snegler i millioner av år av år.
PH kan være den viktigste faktoren i dannelsen av polymorfer ved en temperatur på 24 ° C. Vaterita er hovedproduktet i en rekke pH mellom 8,5 og 10; Aragonitt er pH 11; og kalsitten til ph> 12.
Det er også kjent at mange ferskvannsalgaer bygger kalsittkrystaller når de vokser i et kalsiummettet miljø. I tillegg er mikroalger i stand til å forårsake kalsiumkarbonatutfelling.
Kalsiumkarbonatformer
På bildene nedenfor vil de tre hovedformene eller polymorferene bli vist for kalsiumkarbonat:
 Calcita Crystal. Kilde: Foreldre Géry [Public Domain]
Calcita Crystal. Kilde: Foreldre Géry [Public Domain] Aragonittkrystall. Kilde: Battistini Riccardo [CC BY-SA 4.0 (https: // creativecommons.Org/lisenser/by-SA/4.0)]
Aragonittkrystall. Kilde: Battistini Riccardo [CC BY-SA 4.0 (https: // creativecommons.Org/lisenser/by-SA/4.0)] Vaterita -krystaller. Kilde: Rob Lavinsky, Irocks.COM-CC-BY-SA-3.0 [CC By-SA 3.0 (https: // creativecommons.Org/lisenser/by-SA/3.0)]
Vaterita -krystaller. Kilde: Rob Lavinsky, Irocks.COM-CC-BY-SA-3.0 [CC By-SA 3.0 (https: // creativecommons.Org/lisenser/by-SA/3.0)]
Overfra og ned er kalsitt-, aragonitt- og vaterita -polymorfer. Legg merke til forskjellen mellom morfologien til krystaller (fargen er typisk for dens opprinnelse og egenskaper i miljøene).
Vaterita er mer ugjennomsiktig enn kalsitten, og sistnevnte blir enda fullstendig. I mellomtiden ligner aragonittkrystallene små langstrakte monolitter.
Hvis prøver av disse tre polymorfene blir observert under det elektroniske mikroskopet, deres krystaller (av gråaktige toner fordi teknikken ikke tillater fargeoppløsning), vil de samme morfologiene bli funnet som i makroskopiske skalaer; det vil si ved første øyekast.
Blant disse tre polymorfene er kalsitten den mest tallrike og stabile, etterfulgt av aragonitten, og til slutt Vaterita, den sjeldneste av formene til Caco3
Kan tjene deg: Kalorimetri: Hvilke studier og applikasjonerapplikasjoner
Industriister
Kalsiumkarbonat øker motstanden mot torsjon og trekkraft av syntetisk og naturgummi, og opprettholder fleksibiliteten. Det brukes i byggebransjen som sement ingrediens og som råstoff for kalk. Bruken er blitt redusert fordi det er skadet av surt regn.
Kalsiumkarbonat brukes i jernrensing. I form av kalk eliminerer svoveldioksid som er til stede i metallet. Rengesukkerrensing brukes. Den ble brukt som kritt for skifer, men har blitt erstattet av gipsen for denne applikasjonen.
Kalsiumkarbonat blandes med kittet som brukes i plassering av glass. Ground brukes som fyllingsmateriale i den mikroporøse filmen som brukes i bleier. Det brukes også som fyllingsmateriale i plast som PVC. I tillegg øker styrken til plast.
Kalsiumkarbonat brukes til å øke dekningskapasiteten til maleriene. Det brukes som papirfyllingsmateriale fordi det er billigere enn trefiber, og kan representere mer enn 10% av papiret.
Leger
Det brukes som et antacida for å bekjempe gastrisk hyperaciditet og lindre fordøyelsesbesvær. Det brukes som kalsiumtilskudd og i behandling og forebygging av osteoporose. Det brukes i behandlingen av hyperfosfatia hos pasienter med kronisk nyresvikt.
Det har blitt brukt for å redusere de uønskede effektene av proteaseinhibitorer som ble brukt i behandlingen av HIV, og observerer hos pasienter en reduksjon i diaré.
Det gir en reduksjon i blodtrykk hos gravide med hypertensjon og preeklampsi, siden begge kan være assosiert med en økning i kalsium etterspørsel på grunn av fosterets tilstedeværelse.
Andre
Kalsiumkarbonat brukes i jordbruk som gjødsel og for å bekjempe jordens surhet. Det brukes som konserveringsmiddel, fargeholder og bekrefter mat.
I tillegg er det en ingrediens i tannkrem, og fungerer som slitende i støv i rengjøring og vasking.
Referanser
- Shiver & Atkins. (2008). Uorganisk kjemi. (Fjerde utgave). Mc Graw Hill.
- Wikipedia. (2019). Karbonat kalsium. Hentet fra: i.Wikipedia.org
- Nasjonalt senter for bioteknologiinformasjon. (2019). Karbonat kalsium. PubChem -database., CID = 10112. Gjenopprettet fra: Pubchem.NCBI.NLM.NIH.Gov
- Kai-Yin Chong, Chin-Hua Chia og Sarani Zakaria. (2014). Polymorfer kalsiumkarbonat ved temperaturreaksjon. AIP Conference Proceedings 1614, 52; gjør jeg.org/10.1063/1.4895169
- Greg Watry. (1. november 2016). Å oppdage hvordan karbonatkrystaller får styrke. Fordel forretningsmarkedsføring. Gjenopprettet fra: rdmag.com
- Amerikanske elementer. (2019). Karbonat kalsium. Hentet fra: Amerikanementer.com
- Elsevier. (2019). Karbonat kalsium. Scientedirect. Hentet fra: Scientedirect.com
- Kjemisk bok. (2017). Karbonat kalsium. Gjenopprettet fra: ChemicalBook.com

