Ketogenese typer kropper, syntese og nedbrytning
- 1208
- 151
- Prof. Oskar Aas
De ketogenese Det er prosessen der acetoacetat, ß-hydroksybutirat og aceton oppnås, som sammen kalles ketonlegemer. Denne komplekse og fint regulerte mekanismen utføres i mitokondrier, fra katabolismen av fettsyrer.
Å skaffe ketonlegemene finner sted når kroppen er utsatt for uttømmende perioder med faste. Selv om disse metabolittene for det meste blir syntetisert i leverceller, blir de funnet som en viktig energikilde i variert vev, for eksempel skjelettmuskel og i hjerte og cerebralt vev.
 Kilde: Sav Vas [CC0]
Kilde: Sav Vas [CC0] Β-hydroxibutirat og acetoacetat er metabolitter som brukes som underlag i hjertemuskel og nyrebark. I hjernen blir ketonlegemer viktige energikilder når kroppen har uttømt glukosereservatet.
[TOC]
Generelle egenskaper
Ketogenese anses som en veldig viktig fysiologisk eller metabolsk rute. Generelt utføres denne mekanismen i leveren, selv om det er vist at den kan utføres i andre vev som er i stand til å metabolisere fettsyrer.
Dannelsen av ketonlegemer er den viktigste metabolske avledningen av acetyl-CoA. Denne metabolitten oppnås fra den metabolske ruten kjent som ß-oksidasjon, som er nedbrytningen av fettsyrer.
Tilgjengeligheten av glukose i vevene der ß-oksidasjon skjer, bestemmer den metabolske destinasjonen til acetyl-CoA. I spesielle situasjoner er oksiderte fettsyrer rettet nesten utelukkende til syntesen av ketonlegemer.
Typer og egenskaper til ketonlegemer
Den viktigste ketoniske kroppen er acetoacetat eller acetoeddiksyre, som for det meste er syntetisert i leverceller. Fra acetoacetat er de andre molekylene som utgjør ketonlegemene avledet.
Reduksjon av acetoeddiksyre gir opphav til D-ß-hydroksybutirat, den andre ketoniske kroppen. Aceton er en vanskelig forbindelse for å nedbryte og produseres ved en spontan dekarboksyleringsreaksjon av acetoacetat (så det krever ikke intervensjon av noe enzym), når det er til stede i høye konsentrasjoner i blod.
Kalveren av ketonlegemer er arrangert av konvensjonen, siden strengt tatt ß-hydroksybutirat ikke har en ketonfunksjon. Disse tre molekylene er oppløselige i vann, noe som letter deres blodtransport. Hovedfunksjonen er å gi energi til visse vev som skjelett- og hjertemuskulatur.
Enzymene som er involvert i dannelsen av ketonlegemer er hovedsakelig i leveren og nyrene, noe som forklarer at disse to stedene er hovedprodusentene av disse metabolittene. Syntesen forekommer bare og utelukkende i mitokondriell matrise av celler.
Det kan tjene deg: Sporulering: I planter, i sopp og i bakterierNår disse molekylene er blitt syntetisert, går de til blodomløpet som adresserer vevene som krever dem, hvor de brytes ned til acetyl-CoA.
Syntese av ketonlegemer
Betingelser for ketogenese
Den metabolske destinasjonen til acetyl-CoA fra ß-oksidasjon avhenger av organismens metabolske krav. Dette oksideres til CO2 og h2Eller ved hjelp av sitronsyresyklusen eller syntesen av fettsyrer, hvis metabolismen av lipider og karbohydrater er stabil i kroppen.
Når kroppen trenger karbohydrater, brukes oksalacetat til glukoseproduksjon (glukoneogenese) i stedet for å starte sitronsyresyklusen. Dette skjer, som nevnt, når kroppen har en viss manglende evne til å oppnå glukose, i tilfeller som langvarig faste eller tilstedeværelse av diabetes.
På grunn av dette brukes acetyl-CoA som følge av oksidasjon av fettsyrer for produksjon av ketonlegemer.
Mekanisme
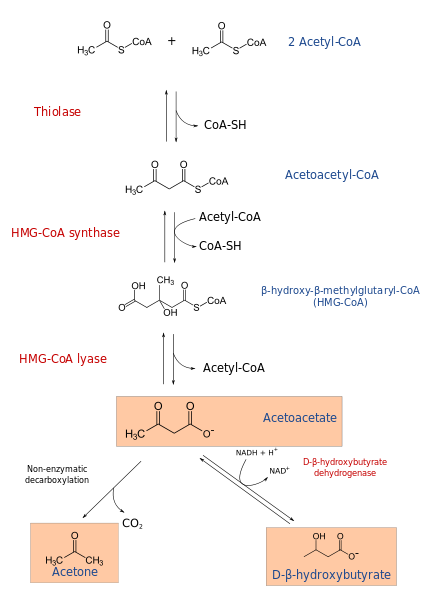
Ketogeneseprosessen begynner fra produktene fra ß-oksidasjon: acetacetyl-CoA eller acetyl-CoA. Når underlaget er acetyl-CoA, består det første trinnet av kondensasjon av to molekyler, acetyl-CoA transferase-reaksjon, for å produsere acetacetyl-CoA.
Acetacetyl-CoA blir kondensert med en tredje acetyl-CoA ved virkningen av HMG-CoA-syntasen, for å produsere HMG-CoA (ß-hydroksy-p-metylglutaril-CoA). HMG-CoA blir nedbrutt til acetoacetat og acetyl-CoA ved HMG-CoA Liasa-handling. På denne måten oppnås den første ketoniske kroppen.
Acetoacetat reduseres til ß-hydroksybutirat ved intervensjon av β-hydroksybutiratdehydrogenase. Denne reaksjonen avhenger av NADH.
Det viktigste ketoniske acetoacetatlegemet er en ß-metoacid, som opplever ikke-enzymatisk dekarboksylering. Denne prosessen er enkel og produserer aceton og co2.
Denne reaksjonsserien resulterer dermed i ketonlegemer. Disse å være oppløselige i vann kan transporteres på en enkel måte gjennom blodsirkulasjonen, uten behov for å forankre til en albuminstruktur, som tilfellet er fettsyrer som er uoppløselige i vandig medium.
Ss-oksidasjon og ketogenese er relatert
Fettsyremetabolisme produserer underlag for ketogenese, så disse to måtene er funksjonelt relatert.
Acetoacetyl-CoA er en hemmer av metabolisme av fettsyrer, siden den stopper aktiviteten til acyl-CoA dehydrogenase som er det første enzymet av ß-oksidasjon. I tillegg utøver den også hemming på acetyl-CoA-overføring og HMG-CoA-syntase.
HMG-CoA-syntaseenzymet, underlagt CPT-I (enzymet involvert i produksjon av acylkarnitin i ß-oksidasjon), representerer en viktig regulatorisk rolle i dannelsen av fettsyrer.
Det kan tjene deg: Flora og Fauna av Zacatecas: Mer representative arterRegulering av ß-oksidasjon og dens virkning på ketogenese
Organismefôring regulerer et komplekst sett med hormonelle signaler. Karbohydrater, aminosyrer og lipider som konsumeres i kostholdet blir avsatt i form av triacylglyceroles i fettvevet. Insulin, et anabole hormon, griper inn i syntesen av lipider og dannelse av triacylglyceroles.
På mitokondrielt nivå styres ß-oksidasjon av inntreden og deltakelse av noen underlag i mitokondriene. Enzymet CPT I syntetiserer karnitin acyl fra acil cytosolisk acil.
Når kroppen mates, øker acetyl-CoA karboksylase og citrat nivåene av CPT I, mens den reduserer fosforylering (syklisk AMP-avhengig reaksjon).
Dette forårsaker en ansamling av malonil COA, som stimulerer syntesen av fettsyrer og blokkerer oksidasjonen, og forhindrer at en meningsløs syklus blir generert.
Når det -Coa.
Nedbrytning
Ketonlegemene spredte seg utenfor cellene der de ble syntetisert og transporteres til perifert vev ved blodomløpet. I disse vevene kan de oksideres gjennom syklusen av trikarboksylsyrer.
I perifert vev oksyder β-hydroksybutirat til acetoacetat. Deretter aktiveres det nåværende acetoacetatet ved virkningen av 3-ZOA transferase-enzymet.
Succinil-CoA fungerer som en COA-donor som blir suksinat. Aktivering av acetoacetat skjer for å forhindre succinyl-CoA.
Den resulterende aceoacetyl-CoA lider av et tiolitisk brudd som produserer to acetyl-CoA-molekyler som er inkorporert i syklusen av trikarboksylsyrer, bedre kjent som Krebs-syklus.
Leverceller mangler 3-cotoacil-CoA-overføring, og forhindrer at denne metabolitten blir aktivert i disse cellene. På denne måten er det garantert at ketonlegemene ikke oksiderer seg i cellene der de ble produsert, men at de kan overføres til vevene der deres aktivitet er nødvendig.
Medisinsk relevans av ketonlegemer
I menneskekroppen kan høye konsentrasjoner av ketonlegemer i blodet forårsake spesielle forhold som kalles acidose og ketonemi.
Kan tjene deg: sfingomyeline: hva er, struktur, funksjoner, synteseProduksjonen av disse metabolittene tilsvarer katabolismen av fettsyrer og karbohydrater. En av de vanligste årsakene til en tilstand av patologisk ketogenese er den høye konsentrasjonen av eddikdikarbonatiserte fragmenter som ikke brytes ned på oksidasjonsveien til trikarboksylsyrer.
Som en konsekvens er det en økning i nivåene av blodketonlegemer over 2 til 4 mg/100 N og deres tilstedeværelse i urin. Dette oversettes til forstyrrelsen av mellomliggende metabolisme av disse metabolittene.
Enkelte defekter i hypofyse neuroglandulære faktorer som regulerer nedbrytning og syntese av ketonlegemene, sammen med lidelser i hydrokarbonmetabolisme, er årsaken til tilstanden til hypercetonemia.
Diabetes mellitus og akkumulering av ketoniske kropper
Diabetes mellitus (type 1) er en endokrin sykdom som forårsaker en økning i produksjonen av ketonlegemer. Insulin utilstrekkelig produksjon deaktiverer glukose til musklene, leveren og fettvevet, og akkumulerer dermed i blod.
Celler i fravær av glukose begynner prosessen med glukoneogenese og nedbrytning av fett og proteiner for å gjenopprette deres metabolisme. Som en konsekvens avtar oksalacetatkonsentrasjoner og øker oksidasjon av lipider.
En acetyl-CoA-akkumulering oppstår, som i mangel av oksalacetat ikke kan følge stien til sitronsyre, og deretter forårsake de høye produksjonene av ketonlegemene, karakteristisk for denne sykdommen.
Akkumulering av aceton oppdages av dens tilstedeværelse i urinen og i pusten fra mennesker som presenterer denne tilstanden, og er faktisk et av symptomene som indikerer manifestasjonen av denne sykdommen.
Referanser
- Blázquez Ortiz, C. (2004). Ketogenese i astrocytter: Karakterisering, regulering og mulig cytoprotective papir (Avhandling Doktor, Complutense University of Madrid, Publications Service).
- Devlin, t. M. (1992). Biokjemiets lærebok: med kliniske korrelasjoner.
- Garrett, r. H., & Grisham, C. M. (2008). Biokjemi. Thomson Brooks/Cole.
- McGry, J. D., Mannaerts, g. P., & Foster, D. W. (1977). En mulig rolle for malonyl-CoA i reguleringen av leverfettsyreoksidasjon og ketogenese. Journal of Clinical Investigation, 60(1), 265-270.
- Melo, v., Ruiz, v. M., & Cuamatzi, eller. (2007). Biokjemi av metabolske prosesser. REVERTE.
- Nelson, d. L., Lehninger, a. L., & Cox, m. M. (2008). Lehninger prinsipper for biokjemi. Macmillan.
- Pertierra, a. G., Gutiérrez, ca. V., & Andre, c. M. (2000). Grunnleggende om metabolsk biokjemi. Redaksjonell Tébar.
- Voet, d., & Voet, j. G. (2006). Biokjemi. Ed. Pan -American Medical.
- « Kontinental frokost hva som er og hvilke matvarer det inkluderer?
- Kalsiumperoksyd (CAO2) egenskaper, risikoer og bruk »

