Klorsyre (Hclo2)
- 3131
- 568
- Theodor Anders Hopland
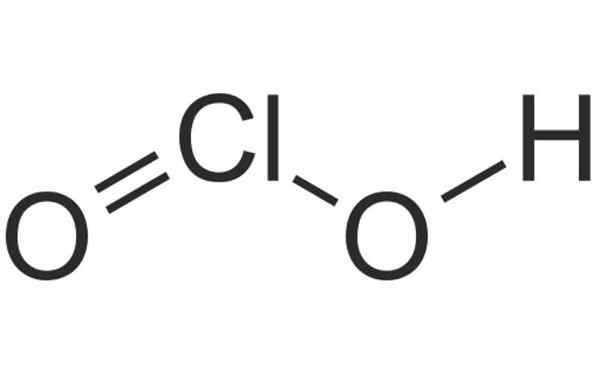
 Kjemisk struktur av klorsyre. Kilde: HBF878, Wikimedia Commons
Kjemisk struktur av klorsyre. Kilde: HBF878, Wikimedia Commons Hva er Chloro?
Han Klorsyre Det er en uorganisk forbindelse av Hclo -formelen2. Denne syren er en av oksacidsyrene i klor, hvor den finnes med oksidasjonstilstand 3+.
Selv om syre er vanskelig å oppnå i rent stoff, er den konjugatbasen avledet fra disse syrene, klorittionen, stabil. Et eksempel på et salt av denne anionen er natriumkloritt. Dette og andre relaterte salter brukes noen ganger i produksjonen av klordioksid.
Klorsyre er en svak syre. Det rene stoffet er ustabilt, uforholdsmessig med hypoklorsyre (oksidasjonsstatus CL +1) og klorsyre (oksidasjonstilstand CL +5):
2hclo2 → Hclo + HClo3
Klorosyre oppnås, sammen med klorisk syre, i nedbrytningen av den vandige klordioksidløsningen.
Klorosyreløsningen ble først oppnådd ved å redusere klorinsyre med tartarsyre, men hovedmetoden for å oppnå denne syren er å behandle en suspensjon av bariumklorid med svovelsyre:
Ba (clo2)2 + H2SW4 → Baso4 + 2hclo2
Klorsyre er et kraftig oksidasjonsmiddel, selv om det.
Klor er det eneste halogenet som danner en isolert formel syre hxo2. Verken Bromous Acid eller Jodosesyre er blitt isolert. Noen salter av spøksyre, vitser er kjent, men bortsett fra som mellommenn i reaksjoner, er det ingen Yoditos -salter.
Fysiske og kjemiske egenskaper
- Klorsyre, når det er mulig å isolere, er en fargeløs væske uten karakteristisk aroma.
Det kan tjene deg: Cycloalcinoer- Forbindelsen har en molekylvekt på 68.456 g/mol. Den har et kokepunkt (beregnet) på 502,07 ° C og en 1 × 10 (beregnet) vannløselighet6 mg/l.
- Hclo2 Det er ustabilt på grunn av dissutasjonsreaksjonen (eller uforholdsmessig) å produsere klorisk og hypoklorsyre, lik den for brom og jodanaloge syrer:
2hclo2 → Hclo + HClo3
- Klorsyre regnes som en svak syre, selv om dens dissosiasjonskonstant er i størrelsesorden 1 x 10-2, Hva gjør det ikke så svakt som andre syrer som har en PKA på 1,96.
Risiko
Klorsyre er en ustabil forbindelse og et sterkt oksidasjonsmiddel som er uforenlig med reduksjonsmidler og alkalier.
Klorosyre er irriterende i tilfelle kontakt med huden og øynene, og er farlig i tilfeller av inntak og innånding.
I tilfelle øyekontakt, må du bekrefte om kontaktlinser brukes og fjerne dem umiddelbart. Øynene skal skylles med rennende vann i minst 15 minutter, og holde øyelokkene åpne. Kaldt vann kan brukes, men ikke et øyesalve.
Hvis kjemikaliet kommer i kontakt med klærne, beholder det så raskt som mulig, og beskytter egne hender og kropp. Plasser offeret under en sikkerhetsdusj.
Hvis kjemikaliet akkumuleres i offerets utsatte hud, for eksempel hendene, vaskes huden forurenset med rennende vann og ikke -slimete såpe mykt og forsiktig.
Kaldt vann kan brukes. Hvis irritasjon vedvarer, må du søke lege. Vask forurensede klær før du bruker det igjen.
Kan tjene deg: fosfatgruppeHvis hudkontakt er alvorlig, bør den vaskes med en desinfiserende såpe og dekke huden forurenset med en antibakteriell krem.
I tilfelle innånding, bør offeret få lov til å stå i et godt ventilert område. Hvis innånding er alvorlig, må offeret evakueres til et trygt område så snart som mulig. Løse tette klær, for eksempel skjortehals, belter eller slips.
Hvis offeret er vanskelig å puste, må oksygen administreres. Hvis offeret ikke puster, blir det laget en gjenopplivning av munnen. Når du alltid tar i betraktning at det kan være farlig for personen som gir hjelp til å gi munn til munnen gjenopplivning når det inhalerte materialet er giftig, smittsomt eller etsende.
Ved inntak induserer det ikke oppkast. Løsne de stramme klærne. Hvis offeret ikke puster, kan du gjenopplive munnen. I alle tilfeller bør det søkes øyeblikkelig legehjelp.
applikasjoner
- Det er utført studier der metastabile oppløsninger av klorinsyre/kloroksyd som oral skylling for plate reduksjon.
Studien ble gjort til en gruppe på 18-27 år frivillige. Effekten på utviklingen av platen og spyttbakterietallet ble testet, og oppnådde en reduksjon på opptil 34,5% reduksjon i tannplatens score sammenlignet med en placebogruppe.
- Klorsyre er involvert i fremstilling av natriumsyrekloritt, som har antimikrobielle egenskaper og er designet for bruk hovedsakelig som en spray eller en nedsenkningsløsning for fjærkre, kjøtt, grønnsaker, frukt og marin mat. Det brukes også i korralfuglkjølende vann.
Kan tjene deg: degenererte orbitaler- Natriumsyrekloritt produseres ved tilsetning av matkvalitetssyre (for eksempel sitronsyre, fosforsyre, saltsyre, hjulesyre eller hydrogensulfatsulfat) til en vannaktig oppløsning av natriumkloritt (NaClo2).
Kombinasjonen av syre med natriumklorittoppløsningen resulterer i klorittkonvertering til en klormålersyre (Hclo2).
NaClo2 + H+ ⇌ Hclo2 + Na+
Denne løsningen kan deretter danne en blanding med kloritt (CLO2-), klordioksid (CLO2) og klorid (CLM). Reaksjonen genererer en oksidativ løsning med oksychlored arter med antimikrobielle egenskaper.
- Natriumsyrekloritt er designet for å brukes som en del av en integrert tilnærming fokusert på å kontrollere mikrobielle belastninger i mat.
Natriumsyre klorittoppløsning virker for å redusere antall patogener (for eksempel, Escherichia coli, OG. Coli o157: h7, Salmonella spp., Campylobacter spp., og Listeria monocytogenes).
Referanser
- Klorsyre. Gjenopprettet fra EBI.Ac.Storbritannia.
- Nasjonalt senter for bioteknologiinformasjon. Gjenopprettet fra Pubchem.

