Sulfanilsyrestruktur, egenskaper, syntese, bruk
- 2349
- 355
- Mathias Aas
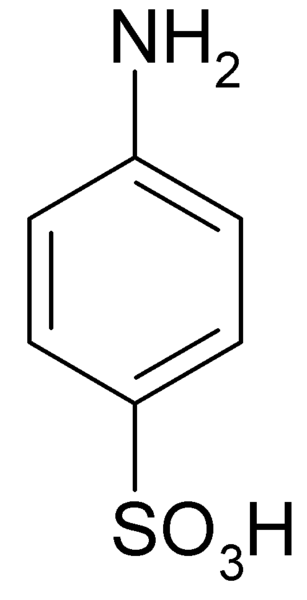
Han Sulfanilsyre Det er en krystallinsk forbindelse hvis molekyl dannes av en benzenring som en grunnleggende gruppe samtidig er forent (-NH2) og en syregruppe (-so3H). Den kjemiske formelen er NH2C6H4SW3H.
Det er også kjent som 4-aminobencenosulfonsyre. Det er utarbeidet ved sulfonering av anilin i stillingen for. Krystallene hans er hvite eller hvite grooves. Dens oppførsel er mer lik den for et salt enn for en organisk forbindelse med NH -grupper2 Bjørn3H. Derfor er det uoppløselig i de fleste organiske løsningsmidler.
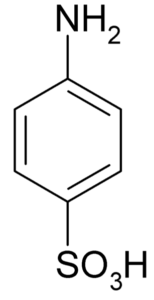 Molekylær formel av sulfanilsyre eller 4-amynobenzeulfonsyre. Klaus Hoffmeier [Public Domain]. Kilde: Wikipedia som oss
Molekylær formel av sulfanilsyre eller 4-amynobenzeulfonsyre. Klaus Hoffmeier [Public Domain]. Kilde: Wikipedia som oss En av hovedbrukene er i syntesen av fargestoffer, da det lett danner et diazokomponert som er råstoff for den applikasjonen.
Både sulfanylyre og dens derivater har blitt brukt som antibakterielle midler. Det brukes i syntesen av mucolytiske forbindelser, siden de har evnen til å redusere viskositeten til slimet eller veldig tyktflytende biologiske væsker.
Det brukes også i papirindustrien og i formler for graveringer eller litografier. Det er en del av harpikser som brukes i betongblandinger eller mørtel for å tillate dem å opprettholde sin flyt i lang tid, uten å påvirke den endelige innstillingstiden.
Det er en xenobiotisk metabolitt, dette betyr at den ikke er naturlig produsert av levende vesener. Det er irriterende hud, øyne og slimete. I tillegg kan du forurense miljøet.
[TOC]
Struktur
Sulfanilsyre har hvite krystaller dannet av ortorrombiske eller monokliniske ark. Dets monohydrat krystalliserer seg i vann i form av ortorrombiske ark. Hvis krystallisering gjøres veldig sakte, krystalliserer du dihydrat. Monohydratet blir vannfri når det er omtrent 100 ºC.
Nomenklatur
- Sulfanilsyre.
- P-amynobenosulfonsyre.
- 4-amybonzefonsyre.
Egenskaper
Fysisk tilstand
Hvit eller hvit krystallinsk faststoff.
Molekylær vekt
173,19 g/mol.
Smeltepunkt
Det brytes ned til omtrent 288 ºC uten å smelte. Det rapporteres også til> 320 ºC.
Tetthet
1,49 g/cm3
Løselighet
Nesten uoppløselig i vann: 10,68 g/l ved 20 ºC.
Uoppløselig i etanol, benzen og eter. Litt løselig i varm metanol.
Løselig i vandige basisløsninger. Uoppløselig i vandige mineralsyreoppløsninger. Løselig i konsentrert saltsyre.
Kjemiske egenskaper
Egenskapene skiller seg fra de til andre amin- eller sulfonerte forbindelser, og er lik de av et salt. Dette er fordi strukturen inneholder gruppene -NH3+ Og så3-, Hva gir det egenskaper ved dipolion.
Kan tjene deg: overmettet løsningDen inneholder en syregruppe og en grunnleggende gruppe i motsatte poler av samme molekyl. Men hydrogenionet er knyttet til nitrogen i stedet for oksygen fordi gruppen -NH2 Det er en sterkere base enn gruppen -så3-.
Fordi det er et dipolion presenterer et høydepunkt for fusjon og uoppløselighet i organiske løsningsmidler.
Sulfanilsyre er oppløselig i alkalisk løsning fordi OH -hydroksydion-, Å være sterkt grunnleggende, starter et hydrogenion (h+) av den svake grunnleggende gruppen -NH2, danner p-aminobencenosulfonateion, som er vannløselig.
I syreoppløsningen endres ikke sulfanylsyrestrukturen, derfor forblir den uoppløselig.
Andre egenskaper
Når den er oppvarmet til nedbrytningen hans, avgir giftige damper av nitrogen- og svoveloksider.
Sulfanylyreeksponering kan føre til symptomer som hudirritasjon, øyne og slimhembraner. Det er en etsende sammensatt.
Syntese
Det tilberedes ved å reagere anilin med svovelsyre (h2SW4) ved høye temperaturer. Opprinnelig dannes det anilinske syresulfatsaltet, som når oppvarming ved 180-200 ºC blir omorganisert for å danne ringen erstattet på plass for, fordi det er det mest stabile produktet.
For å tilberede den med en høy grad av renhet, utføres sulfoneringen av en blanding av anilinen og sulfolano med h h2SW4 ved 180-190 ºC.
applikasjoner
I fargeleggingsbransjen
Sulfanylyre brukes i syntese eller fremstilling av flere fargestoffer, for eksempel metyloransje og tartrazin. For dette er det diazotisert, genererer diazotisert sulfanylyre.
Det er viktig å fremheve at tartrazin har blitt brukt som en fargelegging i mat. Men når den er inntatt, genererer det visse metabolitter i den menneskelige organismen, inkludert sulfanylyre, som er mulig ansvarlige for dannelsen av reaktive oksygenarter. Disse kan påvirke nyre (nyrer) eller levervev (lever).
 Karameller med gult fargestoff. David Adam Kess [CC By-SA 4.0 (https: // creativecommons.Org/lisenser/by-SA/4.0)]. Kilde: Wikipedia Commons
Karameller med gult fargestoff. David Adam Kess [CC By-SA 4.0 (https: // creativecommons.Org/lisenser/by-SA/4.0)]. Kilde: Wikipedia Commons I analytisk kjemi
Det brukes som et reagens i bestemmelsen av flere kjemiske forbindelser, inkludert nitritter.
I medisin som et antibakterielt middel
Sulfanylamid, avledet fra sulfanylyre, har anvendelse i legemiddelindustrien fordi den har antibakteriell aktivitet.
I menneskekroppen forveksler bakterier den med p-aminobenzosyre som er en essensiell metabolitt. Denne substitusjonen fører til at bakterier ikke blir reprodusert og dør.
Kan tjene deg: hydrogen: historie, struktur, egenskaper og bruk Bakterie. Raman Oza -bilde. Kilde: Pixabay
Bakterie. Raman Oza -bilde. Kilde: Pixabay En annen avledet fra sulfanylyre, oppnådd ved kondens med andre forbindelser, har også antibakterielle egenskaper, som er basert på dens evne til å fortrenge folsyre (medlem av vitaminkomplekset b).
Denne forbindelsen kan tas oralt, injisert intravenøst eller påføres eksternt i en salve.
I medisin som et mucolytisk middel
Et sulfanylsyrerivat som har mucolytisk aktivitet er blitt brukt. Dette er at den presenterer licueFactiva slimaktivitet, for å løse opp slimet eller veldig tyktflytende biologiske væsker.
Forbindelsen kan brukes til å produsere slim produsert av et vev på grunn av patologiske forhold. For eksempel overbelastningen av luftveiene eller det fra vaginal kanal, blant andre.
Når det gjelder slim av flytning i luftveiene, administreres produktet ved innånding, dråper i nesen, dugg, aerosoler eller forstøvere. Det er en behandling som gjelder mennesket eller pattedyr. Det er en kraftigere forbindelse enn cysteinbasert.
 Påføring av nesedråper for kulde. Thorsten Frenzel -bilde. Kilde: Pixabay
Påføring av nesedråper for kulde. Thorsten Frenzel -bilde. Kilde: Pixabay Det brukes også på laboratoriet når det er ønsket å redusere viskositeten til biologiske væsker for å lette analytiske bestemmelser.
I bioanalyselaboratorier
Diazotisert sulfanylsyre (et derivat som er fremstilt ved å reagere sulfanylsyre med natriumnitritt) brukes i bilirubinbestemmelse.
Bilirubin er et gult pigment som finnes i galle. Overskuddet av blod bilirubin er en konsekvens av leversykdommer, hematologiske lidelser (eller blod) eller lidelser i galleveiene.
For å måle mengden blod bilirubin, blir dialysen avledet fra sulfanylsyre med bilirubin reagert for å danne azobilirubinkomplekset, hvis farge måles intensiteten med et kolorimeter eller et spektrofotometer. På denne måten bestemmes blodet bilirubininnholdet i blod.
I papirindustrien
Sulfanilsyre lar deg syntetisere en papirpolering, det vil si en forbindelse som gir optisk lysstyrke eller hvitt utseende, siden nøytraliserer den gule fargen på naturlig eller ikke-sporet papir.
 White Paper Notebook. Kilde: Pexels
White Paper Notebook. Kilde: Pexels Det har fordelen i forhold til andre forbindelser, siden den kan brukes i relativt høye konsentrasjoner for å behandle papirmasse under lave pH -forhold, uten å øke papirgult.
Kan tjene deg: ammoniumsulfatResultatet er beviselig når papiret blir observert med UV -lys (ultrafiolett), der fluoresce mye mer enn når andre forbindelser brukes, og med synlig lys observeres det at graden av gulaktig er veldig lav.
Den er veldig løselig i vann, slik at den kan bruke i mer konsentrerte løsninger. Det kan brukes i alle typer papirer, inkludert papiret produsert med bakkemasse, sulfittmasse eller annen prosess.
I inntrykk, graveringer eller litografier
Sulfanilsyre fungerer som en forsuring i konsentrerte løsninger for litografi, uten å presentere problemene med andre syrer som fosfor, å være mindre giftig og mindre forurensende enn sistnevnte enn sistnevnte.
I konstruksjonsmaterialer
Vandig melamin-formaldehydharpiksoppløsninger modifisert med sulfanylyre er testet spesifikt (betong), mørtel eller sementpasta. Hensikten har vært å redusere vanninnholdet og forhindre at reduksjonen i blandingen av blandingen med tidenes gang, uten innstillingstiden reduseres.
Betong eller mørtel som er utarbeidet med disse løsningene er veldig effektiv om sommeren, når nedgangen i flyt over tid utgjør et problem.
Med disse løsningene, hvis mørtelen eller betongen er utarbeidet og av en eller annen grunn må den få lov til å hvile, kan sementsammensetningen lett slippes ut i muggsopp eller lignende, siden den ikke har mistet flyt over tid.
 Betongutladning. Igor Image Ovsyannykov. Kilde: Pixabay
Betongutladning. Igor Image Ovsyannykov. Kilde: Pixabay Referanser
- WINDHOLZ, m. et al. (redaktører) (1983). Merck -indeksen. Et leksikon av kjemikalier, drarugs og biologiske. Tiende utgave. Merck & co., Inc.
- Kirk-Ohmer (1994). Encyclopedia of Chemical Technology. Volum 2. Fjerde utgave. John Wiley & Sons.
- National Library of Medicine. (2019). Sulfanilsyre. Gjenopprettet fra: Pubchem.NCBI.NLM.NIH.Gov
- Urist, h. og Martin, G.J. (1950). Sulfanilinsyrederivater. USAs patentnr. 2.504.471. Tildelere til National Drug Company. 18. april 1950.
- Villaume, Frederick G. (1964). Brightcar -sammensetning for papir avslått fra metanil og sulfanilinsyre. USAs patentnr. 3.132.106. 5. mai 1964.
- Martin, Tellis A. Og spis, William t. (1979). Benzosyrederivat og benzenesulfonsyre mucolytisk prosess. USAs patentnr. 4.132.802. 2. januar 1979.
- Druker, l.J. og Kincaid, r.B. (1979). Litografisk fontene konsentrat. USAs patentnr. 4.150.996. 24. april 1979.
- Shull, Bruce C. (1983). Bilirubinanalyse. USAs patentnr. 4.404.286. 13. september 1983.
- Uchida, J. et al. (2001). Prosess for å fremstille en vandig løsning av sulfanilsyre modifisert melamin-formaldehydharpiks og en sementsammensetning. USAs patentnr. 6.214.965 B1. 10. april 2001.
- Corradini, m.G. (2019). Volum 1. I Encyclopedia of Food Chemistry. Gjenopprettet fra Scientedirect.com.

