Dodecil natriumsulfat (SDS) struktur, egenskaper, bruk
- 1001
- 48
- Magnus Sander Berntsen
Han Natriumsulfat dodecyl (SDS), er et anionisk, syntetisk og amfifyllisk organisk salt. Den apolare og hydrofobe delen tilsvarer hydrokarbonkjeden; Mens den polare og hydrofile delen skyldes sulfat, med negativ belastning.
SDS er et overflateaktivt middel: dets molekyler er plassert på overflaten av vandige oppløsninger, og gir en reduksjon i overflatespenning. Denne funksjonen tillater bruk i sjampo, tannkremer, såper og andre artikler av personlig pleie og rengjøring av hjemmet.
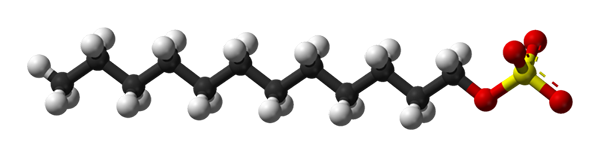
 Natriumsulfat dodekilstruktur. Kilde: Benjah-BMM27 via Wikipedia.
Natriumsulfat dodekilstruktur. Kilde: Benjah-BMM27 via Wikipedia. Natriumsulfat -dodecyl binder seg til protein og produserer sin utfoldelse, og får en langstrakt form. Sulfatgruppene blir utsatt for vann, og får negative belastningsproteiner, hvis antall er proporsjonalt med molekylvekten til dem.
Av denne grunn tillater SDS bestemmelse av molekylvektene til proteiner gjennom elektroforese i polyakrylamid.
Selv om en mulig kreftfremkallende effekt av SDS er mistenkt, er det ikke blitt demonstrert endelig at det er slik. SDS kan produsere, som andre vaskemidler, irritasjon av hud og øyne.
[TOC]
SDS -struktur
I det første bildet ble SDS -molekylet vist med en kuler og bars -modell. Som det kan sees, har den en hydrofob og apolar karbonhale (svart og hvitt kuler); Og samtidig et polært hode, takket være tilstedeværelsen av gruppen -så4- (Gule og røde kuler).
Selv om det ikke er vist, bør det være en lilla sfære som representerer NA -kationen+, Rett ved siden av gruppen -så4-, samhandle elektrostatisk.
Når det er sagt, forstås det med det blotte øye hvorfor denne forbindelsen er amfifyllisk; og også en anionisk spenning, siden belastningen på SDS er negativ og kan tiltrekke andre kationer i tillegg til NA+.
Molekylet gir det falske inntrykk av å være stivt, en fast lineær struktur. Imidlertid er det motsatt. SD -ene kan sammenlignes med en "orm", hvis karbonhale presenterer flere vibrasjoner og rotasjoner av de enkle koblingene. Dette gjør ham i stand til å ta i bruk forskjellige konformasjoner eller bretter i midten; I vann, for eksempel.
Krystaller
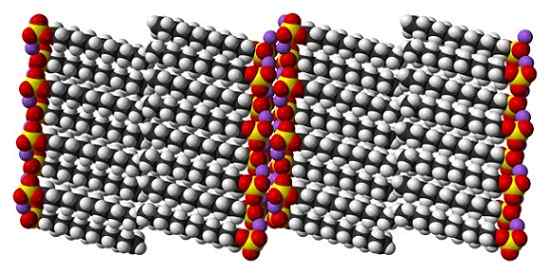 Krystallstruktur av dodecylnatriumsulfat. Kilde: Benjah-BMM27 [Public Domain]
Krystallstruktur av dodecylnatriumsulfat. Kilde: Benjah-BMM27 [Public Domain] Selv om det er sant at natriumsulfatdodecyl er et dynamisk molekyl, har det i fast tilstand ikke behov for å bevege seg for mye, og oppføre seg som en "enkel" bar. Og slik er hvert molekyl eller stang plassert på en slik måte at interaksjonene mellom kullsyreholdige køer og samtidig øker de i deres ioniske belastninger.
Kan tjene deg: natriumkloritt (NaClo2): Struktur, egenskaper, bruksområder, risikoResultatet er dannelsen av en monoklinisk krystall, der SDS -molekyler pakkes i flere barsøyler (øvre bilde). De intermolekylære kreftene som forener dem er slike, at disse krystallene krever en temperatur på 206 ºC for å smelte væskefasen.
Miceller
Utenfor komforten med krystallene kan SDS -molekylet ikke lenger forbli fortsatt; Begynn å vri halen for å øke eller redusere interaksjoner med det ytre miljøet.
Hvis dette mediet er vann, oppstår et fenomen som kalles micellaformasjon: karbon og hydrofobe haler binder seg til å omgi seg, mens polare hoder, grupper -så4-, De forblir på overflaten som samhandler med H -molekyler2ENTEN.
Deretter skaffer Micella seg en obligatorisk ellipsoid morfologi (som jord, men mer knust). I krystallen er de som barblokker, og i et vandig medium som ellipsoide miceller. Hva om mediet var olje? Myce ville bli investert: de polare hodene så4- De ville gå til kjernen, mens karbonatiserte haler ville bli utsatt for olje.
Egenskaper
Navn
- Natrium dodecilsulfate (SDS).
- Natrium Laurilsulfate (SLS).
Molekylær formel
C12H25ENTEN4Sna.
Molmasse
288,378 g/mol.
Fysisk beskrivelse
Flere presentasjoner: tørt støv, flytende eller fuktig fast stoff. Krystallene har en hvit eller kremet farging.
Lukt
Farlukt av fettstoffer, toalett.
Smeltepunkt
206 ºC.
Vannløselighet
1 · 105 mg/l. 1 g oppløst i 10 ml av en opalescerende løsning.
Tetthet
1,01 g/cm3.
Stabilitet
Det er stabilt under de anbefalte lagringsforholdene.
Nedbrytning
Når det er oppvarmet til nedbrytning avgir en hvit røyk av svoveloksyd og natriumoksyd.
Overflatespenning
39,5 dynas/cm ved 25 ºC.
Kritisk molekonsentrasjon
Er 8,2 mm i rent vann ved 25 ° C.
applikasjoner
Personlig pleie og rengjøring hjemme
Sulfat -dodecyl er et overflateaktivt middel som brukes i mange produkter, for eksempel toalettsåper, skumbad, barberhøvelkremer, etc. Det brukes også til å fjerne flekker fra vanskeligheter med å slette, i rengjøring av gulv og bad, furry av kjøkkenartiklene, etc.
Kan servere deg: olje eller benzineeter: formel, struktur, brukVeterinær og menneskelig medisin
Det brukes som et avvisende lopper og flått, til stede i dyr. Det brukes også som fuktighetskrem i noen antibiotika, for oral eller aktuell bruk.
SDS er mikrobicid mot virus med innpakning, for eksempel HIV, type 1 og 2, og herpesen Simple Herpes Virus (HSV-2). Det virker også på virus uten innpakning: papillomavirus, reovirus, rotavirus og poliovirus. Denne bruken er imidlertid ikke godkjent.
Bruken av SDS har blitt foreslått som en vaginal dusj som gir beskyttelse mot seksuelt overført virus. I morsmelkbehandling for å eliminere eller redusere muligheten for HIV -overføring via amming.
I tillegg til den antivirale virkningen, virker SDS på patogene bakterier og sopp. SDS eliminerer medikamentresistens og seksuelle motstandsfaktorer fra E. coli; og blokkerer veksten av mange positive grambakterier.
På laboratoriet
SDS binder seg til proteiner som forårsaker denaturering, gir negative belastninger og en konformasjonsendring. Dette tillater bestemmelse av molekylvekter gjennom elektroforese i polyakrylamid.
SDS brukes også i fremstilling av hjernevevsprøver for bruk i optisk mikroskopi. Det brukes også i fremstilling av blodprøver for antall erytrocytter.
SDS brukes i rensing av nukleinsyrer, på grunn av deres evne til å oppløse membranene og deres hemmende virkning på aktiviteten til Arnasa og DNAASA -enzymer.
I tillegg brukes SDS i karakteriseringen av kvartære ammoniumforbindelser.
Mattilsetningsstoff
SDS brukes som en emulgator og matfortykning. Forbedrer stabilitet og tekstur av bakte produkter. I tillegg brukes det som et hjelpemiddel i tørkede eggprodukter.
Kan tjene deg: sinknitrat: struktur, egenskaper, innhenting, brukIndustri
SDS brukes i galvanoplastikkindustrien, spesielt nikkel og sink; som emulgering og gjennomtrengende lakk og malerifjerner; i formuleringen av eksplosiver støpt ved injeksjon; og i solide raketter som skumming.
Risiko
SDS konstant eksponering kan forårsake hudhyperplasi hos marsvin. Kanin og mennesker er mindre utsatt for disse skadene. Direkte kontakt med SDS i en konsentrasjon ≤ 20%, kan forårsake moderat betennelse og hudirritasjon.
På den annen side kan langvarig eksponering for SDS produsere dermatitt, med tegn på rødhet, hevelse og dannelse.
SDS kan produsere ved kontakt med øyne irritasjon. Det kan også være veldig reaktivt hos noen mennesker, og forårsake irritasjon i luftveiene og luftveiene og luftveiene.
Sjelden kan inntak av SDS forårsake kaustiske lesjoner. Men det har blitt rapportert hos barn som har inntatt SDS, rikelig oppkast av rask utvikling, CNS -depresjon og luftveisnød.
Ingen bevis for genotoksisitet eller teratogen virkning er funnet i SDS. Hos 242 pasienter med eksematøs dermatitt ble 6,4 % av pasientene med allergi funnet, tilskrives bruk av SDS.
Referanser
- Strukturelle data fra l. TIL. Smith, r. B. Hammond, k. J. Roberts, d. Maskin, g. McLeod (2000). Bestemmelse av krystallstruptet av vannfri natriumdodecylsulfat ved bruk av en kombinasjon av sychrotronstrålingspulver diffraksjon og molekylær modelleringsteknikk. Journal of Molecular Structure 554 (2-3): 173-182. Doi: 10.1016/S0022-2860 (00) 00666-9.
- Wikipedia. (2019). Natriumdodecylsulfat. Hentet fra: i.Wikipedia.org
- Nasjonalt senter for bioteknologiinformasjon. (2019). Natriumdodecylsulfat. PubChem -database. CID = 3423265. Gjenopprettet fra: Pubchem.NCBI.NLM.NIH.Gov
- Hammouda f. (2013). Temperatureffekt på nanostrukturen til SDS -miceller i vann. Journal of Research of the National Institute of Standards and Technology, 118, 151-167. Doi: 10.6028/JRES.118.008
- Elsevier. (2019). Natriumdodecylsulfat. Science Direct. Hentet fra: Scientedirect.com
- Kumar, s., TheJajenuo, J. K. og Tsipila, t. (2014). Toksikologiske effekter av natriumdodecylsulfat. Journal of Chemical and Pharmaceutical Research 6 (5): 1488 - 1492.
- Toksikologi datanettverk. (s.F.). Sodium lauryl sulfat. Toxnet. Gjenopprettet fra: Toxnet.NLM.NIH.Gov

